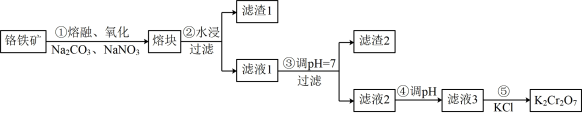
1 . 铬铁矿的主要成分为FeO-Cr2O, 制备K2Cr2O7流程如图所示:
(1)基态Cr原子价电子轨道分布图为__________ ,铬位于元素周期表中__________ 区。
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是__________ ,中心离子的配位数为_________ 。
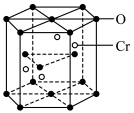
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=__________ g/cm3。 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为__________ ,该步骤不能使用陶瓷容器,原因是__________ 。
(5)步骤④调滤液2的pH使之变__________ (填“大”或“小”)。原因是__________ (用离子方程式表示)。
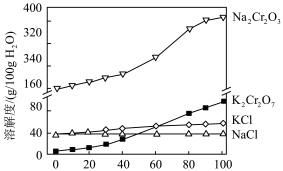
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是__________ ,冷却到__________ (填标号)得到的K2Cr2O7固体产品最多。
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于__________ mol/L。
(1)基态Cr原子价电子轨道分布图为
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=
 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为(5)步骤④调滤液2的pH使之变
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于
您最近半年使用:0次
2 . 乙二醇锑[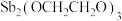 ]是一种白色晶状粉末,可用作聚酯缩聚催化剂,其生产工艺流程如图:
]是一种白色晶状粉末,可用作聚酯缩聚催化剂,其生产工艺流程如图:

下列说法正确的是
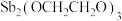 ]是一种白色晶状粉末,可用作聚酯缩聚催化剂,其生产工艺流程如图:
]是一种白色晶状粉末,可用作聚酯缩聚催化剂,其生产工艺流程如图:
下列说法正确的是
A.“煅烧”过程中每生成 氧化产物转移 氧化产物转移 电子 电子 |
B.“醇化”反应方程式为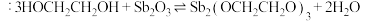 |
C.增大乙二醇的用量和移走水均可提高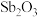 的平衡转化率 的平衡转化率 |
D.可用原子光谱检验产品中的乙二醇基( ) ) |
您最近半年使用:0次
3 . 回答下列问题:
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性___________ 。
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图:___________ (用离子符号表示)。
②上述流程中,试剂c为___________ (写化学式)。
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
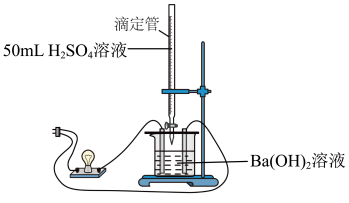
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入一定浓度的Ba(OH)2溶液,逐滴滴加H2SO4溶液直至过量,边滴边振荡 | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、
 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图: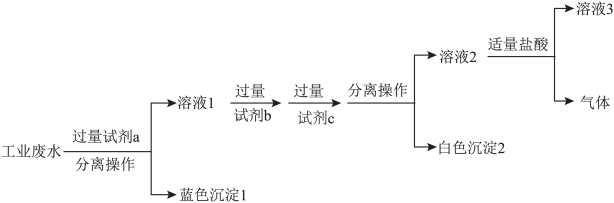
②上述流程中,试剂c为
您最近半年使用:0次
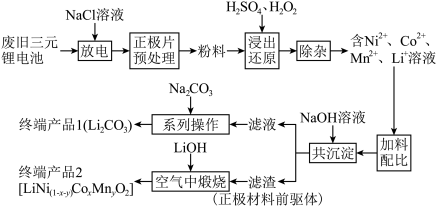
4 . 随着新能源汽车的不断发展,从经济价值、环境保护等多重背景下考虑,废旧锂离子电池中的锂、镍、钴、锰金属的回收利用已经刻不容缓。某科研团队对废旧三元锂电池进行处理,工艺如图所示:
a.正极片预处理后的粉料中主要成分与终端产品2相同,均为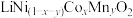 ,且其中所含镍、钴、锰的化合价均为+3价。粉料中杂质主要为
,且其中所含镍、钴、锰的化合价均为+3价。粉料中杂质主要为 。
。
b.碳酸锂微溶于水,其溶解度随温度升高而减小。
(1)旧电池拆解前进行放电处理有利于锂在正极的回收,其原因是___________ 。
(2)写出粉料中的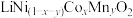 通过“浸出还原”得到含
通过“浸出还原”得到含 、
、 、
、 、
、 的化学反应方程式:
的化学反应方程式:___________ 。
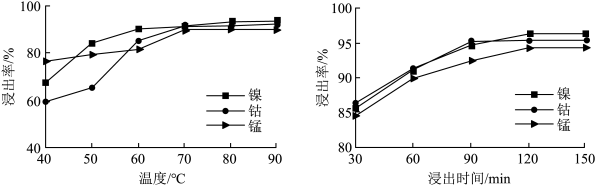
(3)温度、浸出时间对镍、钴、锰浸出率的影响如下图所示。根据图中信息,应选择的温度为___________ ℃,浸出时间为___________ min。除温度和时间外,写出另外一种影响浸出率的因素:___________ 。___________ 。
(5)“共沉淀”后的滤液中含有大量 ,加碳酸钠后,对溶液采用如下“系列操作”可得到终端产品1:
,加碳酸钠后,对溶液采用如下“系列操作”可得到终端产品1:___________ 、___________ 、洗涤、干燥。检验沉淀是否洗涤干净的操作是___________ 。
(6)已知 、
、 、
、 三种物质的
三种物质的 分别为
分别为 、
、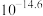 、
、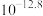 ,共沉淀时,使构成三元材料的金属离子均完全沉淀(溶液中离子浓度
,共沉淀时,使构成三元材料的金属离子均完全沉淀(溶液中离子浓度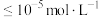 ),则pH至少应调至
),则pH至少应调至___________ 。
a.正极片预处理后的粉料中主要成分与终端产品2相同,均为
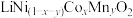 ,且其中所含镍、钴、锰的化合价均为+3价。粉料中杂质主要为
,且其中所含镍、钴、锰的化合价均为+3价。粉料中杂质主要为 。
。b.碳酸锂微溶于水,其溶解度随温度升高而减小。
(1)旧电池拆解前进行放电处理有利于锂在正极的回收,其原因是
(2)写出粉料中的
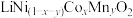 通过“浸出还原”得到含
通过“浸出还原”得到含 、
、 、
、 、
、 的化学反应方程式:
的化学反应方程式:(3)温度、浸出时间对镍、钴、锰浸出率的影响如下图所示。根据图中信息,应选择的温度为
(5)“共沉淀”后的滤液中含有大量
 ,加碳酸钠后,对溶液采用如下“系列操作”可得到终端产品1:
,加碳酸钠后,对溶液采用如下“系列操作”可得到终端产品1:(6)已知
 、
、 、
、 三种物质的
三种物质的 分别为
分别为 、
、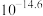 、
、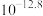 ,共沉淀时,使构成三元材料的金属离子均完全沉淀(溶液中离子浓度
,共沉淀时,使构成三元材料的金属离子均完全沉淀(溶液中离子浓度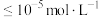 ),则pH至少应调至
),则pH至少应调至
您最近半年使用:0次
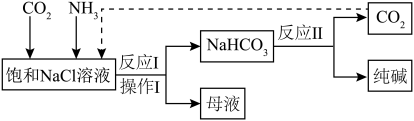
5 . 已知“氨碱法”的部分工艺流程如下: 转化为
转化为 ,再加入NaCl细粉的方式获得
,再加入NaCl细粉的方式获得 晶体,从而提高了母液的利用率。下列有关“联合制碱法”说法正确的是
晶体,从而提高了母液的利用率。下列有关“联合制碱法”说法正确的是
 转化为
转化为 ,再加入NaCl细粉的方式获得
,再加入NaCl细粉的方式获得 晶体,从而提高了母液的利用率。下列有关“联合制碱法”说法正确的是
晶体,从而提高了母液的利用率。下列有关“联合制碱法”说法正确的是A.母液中存在的主要离子有: 、 、 、 、 、 、 |
B.反应1析出的 晶体表面附有的 晶体表面附有的 可以通过加热除去 可以通过加热除去 |
C.向母液中加入NaCl细粉时发生的反应: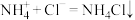 |
D.将析出 晶体后的溶液蒸发浓缩、冷却结晶,可获得更多的 晶体后的溶液蒸发浓缩、冷却结晶,可获得更多的 晶体 晶体 |
您最近半年使用:0次
解题方法
6 . 柱色谱法包含两个相,一个是固定相,一个是流动相。当两相相对运动时,反复多次地利用混合物中所含各组分分配平衡性质的差异,最后达到彼此分离的目的。茉莉醛(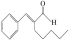 )是一种合成香料、制备苯莉醛的工艺流程如图所示。下列说法正确的是
)是一种合成香料、制备苯莉醛的工艺流程如图所示。下列说法正确的是
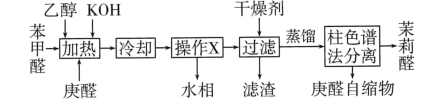
| A.乙醇的主要作用是助溶剂 |
| B.操作X为过滤 |
| C.可将最后两步“蒸馏”和“柱色谱法分离” 替换为“真空减压蒸馏” |
| D.可采用与浓硫酸共热的方法来除去产品中少量的庚醛自缩物 |
您最近半年使用:0次
名校
解题方法
7 . 某同学设计如下方案从粗食盐水中除去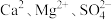 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:
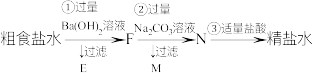
以下说法不正确的是
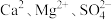 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验: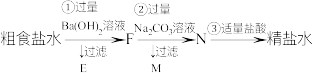
以下说法不正确的是
A.E中主要有 和 和 ,也可能有一些 ,也可能有一些 |
B.②中加入过量 溶液的主要目的是为了除去 溶液的主要目的是为了除去 |
| C.N溶液呈碱性 |
D.③目的是除去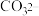 和 和 |
您最近半年使用:0次
解题方法
8 . 抗血栓药物氯吡格雷的重要中间体之一“2―噻吩乙醇”( )的制备步骤如下:
)的制备步骤如下: ,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
按要求回答下列问题:
(1)步骤ⅰ中液体X可以选择_______ 。
a.水 b.甲苯 c.乙醇 d.苯酚
(2)写出步骤ⅰ制2-噻吩钠的化学方程式为_______ 。
(3)步骤ⅱ,加入溶液的方式为________ (填“缓慢加入”或“一次性加入”)。
(4)写出步骤ⅲ中用盐酸调节pH的化学方程式:________ 。加入无水 的作用为
的作用为___________ 。
(5)步骤ⅲ中⑤的操作的名称为_______ ;写出选择此分离提纯方法的理由是_______ 。
(6)产品“2―噻吩乙醇”( )的产率为
)的产率为_______ (用含m、n的代数式表示)。
(7)某次平行实验所得产品质量比ng低些,写出其中一种可能的原因:_______ 。
 )的制备步骤如下:
)的制备步骤如下: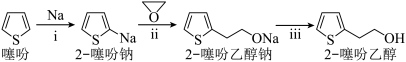
ⅱ.制噻吩乙醇钠:降温至−10℃,加入稍过量的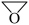 的四氢呋喃溶液,反应30min(四氢呋喃
的四氢呋喃溶液,反应30min(四氢呋喃 是有机溶剂,沸点66℃,可防止因反应放热而导致温度过高而引发副反应)。
是有机溶剂,沸点66℃,可防止因反应放热而导致温度过高而引发副反应)。
 ,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。按要求回答下列问题:
(1)步骤ⅰ中液体X可以选择
a.水 b.甲苯 c.乙醇 d.苯酚
(2)写出步骤ⅰ制2-噻吩钠的化学方程式为
(3)步骤ⅱ,加入溶液的方式为
(4)写出步骤ⅲ中用盐酸调节pH的化学方程式:
 的作用为
的作用为(5)步骤ⅲ中⑤的操作的名称为
(6)产品“2―噻吩乙醇”(
 )的产率为
)的产率为(7)某次平行实验所得产品质量比ng低些,写出其中一种可能的原因:
您最近半年使用:0次
9 . 某工业废水中存在大量的 、
、 、
、 和
和 ,欲除去废水中的
,欲除去废水中的 和
和 ,设计工艺流程如下:
,设计工艺流程如下:
 、
、 、
、 和
和 ,欲除去废水中的
,欲除去废水中的 和
和 ,设计工艺流程如下:
,设计工艺流程如下:
| A.加入试剂a,可观察到溶液A中有白色沉淀生成 |
B.加入试剂b,发生反应的离子方程式为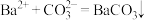 |
| C.试剂c为盐酸 |
D.溶液C中只含有 、 、 、 、 |
您最近半年使用:0次
10 . 天青石主要成分是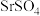 ,还含有少量
,还含有少量 及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备
及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备 的工艺流程如下:
的工艺流程如下: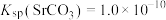 ,
,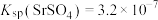
下列说法错误的是
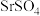 ,还含有少量
,还含有少量 及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备
及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备 的工艺流程如下:
的工艺流程如下: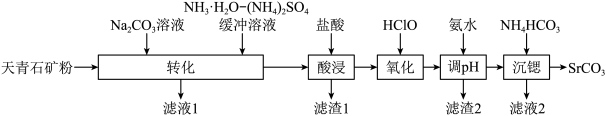
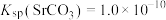 ,
,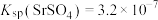
下列说法错误的是
A.加入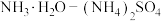 缓冲溶液可使 缓冲溶液可使 转化为 转化为 |
| B.钡、硅元素分别在“酸浸”和“调pH”工序除去 |
| C.若去掉“氧化”工序,“调pH”时消耗氨水量增大 |
D.将92g 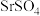 投入到1L 投入到1L  溶液中,反应后 溶液中,反应后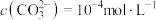 时, 时,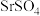 的转化率为32%(忽略溶液体积变化) 的转化率为32%(忽略溶液体积变化) |
您最近半年使用:0次



