1 . 钌(Ru)是地球上丰度最小的元素,钌的产品广泛应用于电子、航空航天、化工等领域。从某种失效的钌催化剂(主要成分为Ru、ZnO、 、有机物等)中回收钌的工艺流程如下:
、有机物等)中回收钌的工艺流程如下: 的沸点为40℃,温度高于108℃分解。②氧化性:
的沸点为40℃,温度高于108℃分解。②氧化性: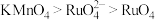
(1)“煅烧”的目的是___________ 。
(2)“氧化”过程需在650℃下熔融反应5小时。
①单质Ru被氧化为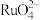 的化学方程式为
的化学方程式为___________ 。
② 固体过量会导致钌的回收率降低,原因是
固体过量会导致钌的回收率降低,原因是___________ 。
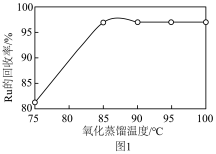
(3)“氧化蒸馏”时,测得钌的回收率随温度变化曲线如图1所示。工业上保证钌回收率较高的情况下,选择在95℃进行氧化蒸馏的原因是___________ 。___________ 。
(5)钌多活性位点催化剂(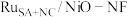 )可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
)可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。___________ 。
②催化剂的活性位点在催化过程中的主要作用是___________ 。
③分析图2-a推测 的“吸附解离”主要发生在
的“吸附解离”主要发生在___________ (填“钌原子”、“钌团簇”或“NiO”)位点上,若有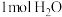 参与该过程,则变化的能量为
参与该过程,则变化的能量为___________ kJ(保留1位小数:已知: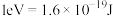 )。
)。
④分析图2-b并说明 的脱附主要发生在NiO表面的原因
的脱附主要发生在NiO表面的原因___________ 。
 、有机物等)中回收钌的工艺流程如下:
、有机物等)中回收钌的工艺流程如下: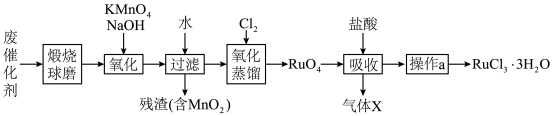
 的沸点为40℃,温度高于108℃分解。②氧化性:
的沸点为40℃,温度高于108℃分解。②氧化性: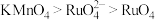
(1)“煅烧”的目的是
(2)“氧化”过程需在650℃下熔融反应5小时。
①单质Ru被氧化为
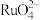 的化学方程式为
的化学方程式为②
 固体过量会导致钌的回收率降低,原因是
固体过量会导致钌的回收率降低,原因是(3)“氧化蒸馏”时,测得钌的回收率随温度变化曲线如图1所示。工业上保证钌回收率较高的情况下,选择在95℃进行氧化蒸馏的原因是
(5)钌多活性位点催化剂(
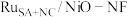 )可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
)可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
②催化剂的活性位点在催化过程中的主要作用是
③分析图2-a推测
 的“吸附解离”主要发生在
的“吸附解离”主要发生在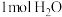 参与该过程,则变化的能量为
参与该过程,则变化的能量为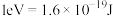 )。
)。④分析图2-b并说明
 的脱附主要发生在NiO表面的原因
的脱附主要发生在NiO表面的原因
您最近一年使用:0次
解题方法
2 . 以碲铜废料(主要含 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下: 和二元弱酸
和二元弱酸
②
下列说法错误的是
 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下: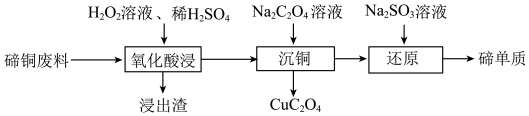
 和二元弱酸
和二元弱酸
②

下列说法错误的是
A.“氧化酸浸”时, 作氧化剂 作氧化剂 |
B.“沉铜”时,需加过量 |
C.螯合物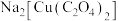 中Cu(Ⅱ)的配位数为4 中Cu(Ⅱ)的配位数为4 |
D.“还原”时,发生的主要反应为 |
您最近一年使用:0次
解题方法
3 . 从硝酸铜和硝酸银的混合溶液中回收铜和银的流程如图所示。

| A.试剂Ⅰ可以是稀盐酸或稀硫酸 |
| B.流程中涉及的反应均是氧化还原反应 |
C.生成银氨溶液的离子方程式为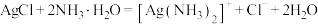 |
D.若试剂Ⅱ是甲醛, 甲醛参加反应最多生成 甲醛参加反应最多生成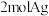 |
您最近一年使用:0次
4 . 焦锑酸钠 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。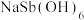 难溶于水。
难溶于水。
②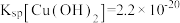 ,
, 。
。
回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是_______ ,“浸渣”的主要成分是_______ (填“ ”或“CuS”)。
”或“CuS”)。
(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为_______ 。
(3)“氧化”时,溶液中的 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式_______ 。
(4)“滤液”的主要成分是_______ 。
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定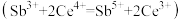 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。
①硫酸肼的作用是_______ 。
②产品的纯度为_______ [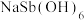 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。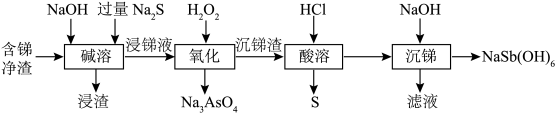
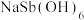 难溶于水。
难溶于水。②
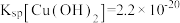 ,
, 。
。回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是
 ”或“CuS”)。
”或“CuS”)。(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为
(3)“氧化”时,溶液中的
 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式(4)“滤液”的主要成分是
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定
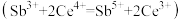 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。①硫酸肼的作用是
②产品的纯度为
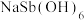 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
您最近一年使用:0次
5 . 钨是国防及高新技术应用中极为重要的功能材料之一,由黑钨矿[主要成分是钨酸亚铁( )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸( )酸性很弱,难溶于水。
)酸性很弱,难溶于水。
②水浸液中含有 、
、 、
、 、
、 等阴离子。
等阴离子。
回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是_______ 。
(2)“焙烧”过程中,生成 的化学方程式为
的化学方程式为_______ 。
(3)“净化”过程中, 的作用是
的作用是_______ 。
(4)“酸化”过程中,发生反应的离子方程式为_______ 。
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为_______ 。
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为_______ 。
(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=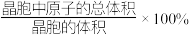 )。
)。
 )、钨酸锰(
)、钨酸锰( ),以及少量的Si、As元素]冶炼钨的流程如下:
),以及少量的Si、As元素]冶炼钨的流程如下:
①钨酸(
 )酸性很弱,难溶于水。
)酸性很弱,难溶于水。②水浸液中含有
 、
、 、
、 、
、 等阴离子。
等阴离子。回答下列问题:
(1)“焙烧”前,需将黑钨矿粉碎,目的是
(2)“焙烧”过程中,生成
 的化学方程式为
的化学方程式为(3)“净化”过程中,
 的作用是
的作用是(4)“酸化”过程中,发生反应的离子方程式为
(5)“高温还原”过程中,被还原的物质与被氧化的物质的物质的量之比为
(6)硬质合金刀具中含碳化钨(WC,碳元素为-4价),利用电解法可以从碳化钨废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸沉淀并放出
 气体,则阳极的电极反应式为
气体,则阳极的电极反应式为(7)钨晶胞为体心立方晶胞,晶胞结构如图所示(注:晶胞体对角线的W原子相切),则钨晶胞的原子空间利用率为_______(填标号。晶胞的原子空间利用率=
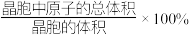 )。
)。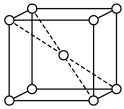
A. | B.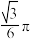 | C. | D. |
您最近一年使用:0次
6 . 硫酸铜是较重要的铜盐之一,在电镀、印染、颜料、农药等方面有广泛应用。 的制备和性质探究实验如下:
的制备和性质探究实验如下:
Ⅰ.制备CuO。洗净的瓷坩埚经充分灼烧干燥并冷却后,在托盘天平上称取3.0g废铜粉(铜粉的含量为98%)放入其内。将坩埚置于泥三角上,用煤气灯氧化焰小火微热,待铜粉干燥后,加大火焰高温灼烧,并不断搅拌,搅拌时必须用坩埚钳夹住坩埚。灼烧至铜粉完全转化为黑色,停止加热并冷却至室温。
Ⅱ.制备粗 溶液。将冷却的CuO倒入100mL小烧杯中,加入18mL
溶液。将冷却的CuO倒入100mL小烧杯中,加入18mL 硫酸,微热使之溶解。
硫酸,微热使之溶解。
Ⅲ.精制 溶液。在粗
溶液。在粗 溶液中,滴加2mL3%的双氧水,将溶液加热,随后检验溶液中是否存在
溶液中,滴加2mL3%的双氧水,将溶液加热,随后检验溶液中是否存在 。当
。当 完全反应后,慢慢加入
完全反应后,慢慢加入 粉末,同时不断搅拌直到溶液
粉末,同时不断搅拌直到溶液 ,在此过程中,要不断地用pH试纸测溶液的pH,控制溶液
,在此过程中,要不断地用pH试纸测溶液的pH,控制溶液 ,再加热至沸,趁热减压过滤(如图所示),将滤液转移至洁净的烧杯中。
,再加热至沸,趁热减压过滤(如图所示),将滤液转移至洁净的烧杯中。 。在精制的
。在精制的 溶液中,滴加
溶液中,滴加 硫酸酸化,调节溶液至pH=1后,将溶液转移至洁净的蒸发皿中,水浴加热,蒸发至液面出现晶膜时停止加热。在室温下冷却至晶体析出,然后减压过滤,晶体用滤纸吸干后,称重得到产品7.0g。
硫酸酸化,调节溶液至pH=1后,将溶液转移至洁净的蒸发皿中,水浴加热,蒸发至液面出现晶膜时停止加热。在室温下冷却至晶体析出,然后减压过滤,晶体用滤纸吸干后,称重得到产品7.0g。
回答下列问题:
(1)步骤Ⅰ中,“搅拌时必须用坩埚钳夹住坩埚”的原因是______ 。
(2)步骤Ⅲ中,双氧水的作用是______ 。
(3)步骤Ⅲ中,“控制溶液 ,再加热至沸”的目的是
,再加热至沸”的目的是______ 。相比于过滤,趁热减压过滤的优点是______ 。
(4)步骤Ⅳ中,蒸发、结晶制备 时,蒸发至刚出现晶膜即停止加热,其原因是
时,蒸发至刚出现晶膜即停止加热,其原因是______ 。用滤纸吸干晶体,而不用酒精灯烘干,原因是______ 。
(5)本实验产率为______ %。(保留2位有效数字)
(6)探究 的性质。取少量产品溶于水,加入足量淀粉-KI溶液,充分搅拌,发现溶液变蓝色,并产生白色沉淀,过滤、洗涤、干燥,测得白色沉淀由Cu、I元素组成且二者质量比为64∶127。该过程中发生反应的离子方程式为
的性质。取少量产品溶于水,加入足量淀粉-KI溶液,充分搅拌,发现溶液变蓝色,并产生白色沉淀,过滤、洗涤、干燥,测得白色沉淀由Cu、I元素组成且二者质量比为64∶127。该过程中发生反应的离子方程式为______ 。
 的制备和性质探究实验如下:
的制备和性质探究实验如下:Ⅰ.制备CuO。洗净的瓷坩埚经充分灼烧干燥并冷却后,在托盘天平上称取3.0g废铜粉(铜粉的含量为98%)放入其内。将坩埚置于泥三角上,用煤气灯氧化焰小火微热,待铜粉干燥后,加大火焰高温灼烧,并不断搅拌,搅拌时必须用坩埚钳夹住坩埚。灼烧至铜粉完全转化为黑色,停止加热并冷却至室温。
Ⅱ.制备粗
 溶液。将冷却的CuO倒入100mL小烧杯中,加入18mL
溶液。将冷却的CuO倒入100mL小烧杯中,加入18mL 硫酸,微热使之溶解。
硫酸,微热使之溶解。Ⅲ.精制
 溶液。在粗
溶液。在粗 溶液中,滴加2mL3%的双氧水,将溶液加热,随后检验溶液中是否存在
溶液中,滴加2mL3%的双氧水,将溶液加热,随后检验溶液中是否存在 。当
。当 完全反应后,慢慢加入
完全反应后,慢慢加入 粉末,同时不断搅拌直到溶液
粉末,同时不断搅拌直到溶液 ,在此过程中,要不断地用pH试纸测溶液的pH,控制溶液
,在此过程中,要不断地用pH试纸测溶液的pH,控制溶液 ,再加热至沸,趁热减压过滤(如图所示),将滤液转移至洁净的烧杯中。
,再加热至沸,趁热减压过滤(如图所示),将滤液转移至洁净的烧杯中。
 。在精制的
。在精制的 溶液中,滴加
溶液中,滴加 硫酸酸化,调节溶液至pH=1后,将溶液转移至洁净的蒸发皿中,水浴加热,蒸发至液面出现晶膜时停止加热。在室温下冷却至晶体析出,然后减压过滤,晶体用滤纸吸干后,称重得到产品7.0g。
硫酸酸化,调节溶液至pH=1后,将溶液转移至洁净的蒸发皿中,水浴加热,蒸发至液面出现晶膜时停止加热。在室温下冷却至晶体析出,然后减压过滤,晶体用滤纸吸干后,称重得到产品7.0g。回答下列问题:
(1)步骤Ⅰ中,“搅拌时必须用坩埚钳夹住坩埚”的原因是
(2)步骤Ⅲ中,双氧水的作用是
(3)步骤Ⅲ中,“控制溶液
 ,再加热至沸”的目的是
,再加热至沸”的目的是(4)步骤Ⅳ中,蒸发、结晶制备
 时,蒸发至刚出现晶膜即停止加热,其原因是
时,蒸发至刚出现晶膜即停止加热,其原因是(5)本实验产率为
(6)探究
 的性质。取少量产品溶于水,加入足量淀粉-KI溶液,充分搅拌,发现溶液变蓝色,并产生白色沉淀,过滤、洗涤、干燥,测得白色沉淀由Cu、I元素组成且二者质量比为64∶127。该过程中发生反应的离子方程式为
的性质。取少量产品溶于水,加入足量淀粉-KI溶液,充分搅拌,发现溶液变蓝色,并产生白色沉淀,过滤、洗涤、干燥,测得白色沉淀由Cu、I元素组成且二者质量比为64∶127。该过程中发生反应的离子方程式为
您最近一年使用:0次
名校
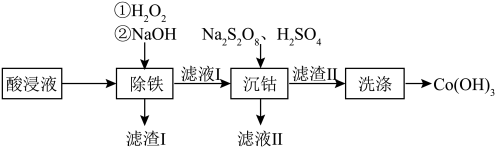
7 . 某工厂采用如下工艺处理含钴废料的硫酸浸取液(含 、
、 和
和 )
) 时:以下说法正确的是
时:以下说法正确的是
 、
、 和
和 )
)
 时:以下说法正确的是
时:以下说法正确的是| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.5 | 7.7 | 0.1 | 6.5 |
| 沉淀完全的pH | 3.2 | 9.0 | 9.2 | 1.1 | 8.0 |
A.滤液Ⅱ中主要存在的离子有 、 、 、 、 、 、 |
B.根据流程可知: 的还原性大于 的还原性大于 |
C.检验 是否洗涤干净可以用稀盐酸和 是否洗涤干净可以用稀盐酸和 溶液 溶液 |
D.沉钻过程中发生的主要反应的离子方程式为 |
您最近一年使用:0次
解题方法
8 . 钛酸钡( )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量CaO、
,含少量CaO、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下:
注:
回答下列问题:
(1)浸渣的主要成分是___________ (填化学式)。
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图所示。___________ 。图2中温度高于65℃,钛浸出率降低的原因可能是___________ 。
(3)“还原”时,主要反应的离子方程式为___________ ,检验“还原”后溶液中是否含 的试剂是
的试剂是___________ (填化学式)。
(4)“沉钛”中,先加入过量 ,溶液,后加入适量
,溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生___________ (填化学式)杂质,影响产率。“调pH”范围为___________ 。
(5)“氧化焙烧”发生反应的化学方程式为___________ 。工业上,还可以直接将 ·4
·4 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是___________ 。
(6)经X射线分析鉴定,钛酸钡的晶胞结构如图所示( 、
、 均与
均与 相接触)。已知晶胞边长为
相接触)。已知晶胞边长为 pm,
pm, 的半径为
的半径为 pm,则
pm,则 的半径为
的半径为___________ pm。
 )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量CaO、
,含少量CaO、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下: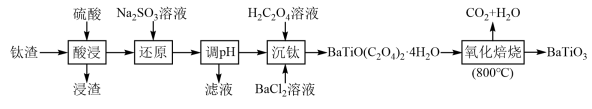
| 金属离子 |  |  |  |
| 开始沉淀/pH | 1.5 | 6.3 | 0.5 |
| 完全沉淀/pH | 2.8 | 8.3 | 2.5 |

回答下列问题:
(1)浸渣的主要成分是
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图所示。

(3)“还原”时,主要反应的离子方程式为
 的试剂是
的试剂是(4)“沉钛”中,先加入过量
 ,溶液,后加入适量
,溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生(5)“氧化焙烧”发生反应的化学方程式为
 ·4
·4 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是(6)经X射线分析鉴定,钛酸钡的晶胞结构如图所示(
 、
、 均与
均与 相接触)。已知晶胞边长为
相接触)。已知晶胞边长为 pm,
pm, 的半径为
的半径为 pm,则
pm,则 的半径为
的半径为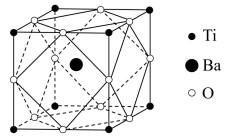
您最近一年使用:0次
名校
9 . 向碘水、淀粉的混合液中加入 溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
 溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
A.①中 氧化了 氧化了 | B.①后溶液pH可能明显变小 |
C.③的目的是除去过量的 溶液 溶液 | D.④可发生 |
您最近一年使用:0次
名校
10 . 香豆素是一种天然香料,存在于黑香豆、兰花等植物中,可利用Perkin反应制备:
Ⅰ.连接如图所示装置,检查装置气密性,加入反应物并通入一段时间 。
。
Ⅱ.升温至135~145℃,回流,排酸。
Ⅲ.继续升温至160~180℃,回流。
Ⅳ.待反应结束后,向仪器A中加热水,分液,结晶,过滤得香豆素粗产品。
回答下列问题:
(1)仪器A的名称为___________ 。
(2)应采取的加热方式为___________ (填标号)。
a.直接加热 b.水浴加热 c.油浴加热
(3)步骤Ⅰ中,通入一段时间 的目的为
的目的为___________ ,加入乙酸酐不宜过多,原因是___________ 。
(4)步骤Ⅱ的目的是___________ 。
(5) 作催化剂的关键是促进生成
作催化剂的关键是促进生成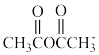 ,下列物质能作为该反应的催化剂的是
,下列物质能作为该反应的催化剂的是___________ (填标号)。
a. b.
b. c.NaCl
c.NaCl
(6)本实验装置存在一处明显缺陷是___________ 。
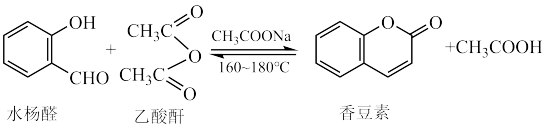
Ⅰ.连接如图所示装置,检查装置气密性,加入反应物并通入一段时间
 。
。Ⅱ.升温至135~145℃,回流,排酸。
Ⅲ.继续升温至160~180℃,回流。
Ⅳ.待反应结束后,向仪器A中加热水,分液,结晶,过滤得香豆素粗产品。
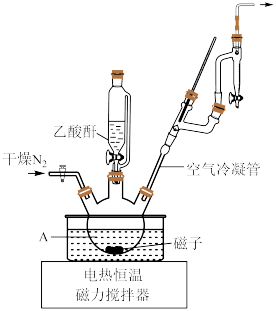
| 物质 | 水杨醛 | 乙酸酐 | 乙酸 | 香豆素 |
| 沸点/℃ | 197 | 138.6 | 117.9 | 298 |
(1)仪器A的名称为
(2)应采取的加热方式为
a.直接加热 b.水浴加热 c.油浴加热
(3)步骤Ⅰ中,通入一段时间
 的目的为
的目的为(4)步骤Ⅱ的目的是
(5)
 作催化剂的关键是促进生成
作催化剂的关键是促进生成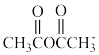 ,下列物质能作为该反应的催化剂的是
,下列物质能作为该反应的催化剂的是a.
 b.
b. c.NaCl
c.NaCl(6)本实验装置存在一处明显缺陷是
您最近一年使用:0次



