名校
解题方法
1 . 明代宋应星《天工开物·杀青篇》中详细记载了古法制纸工艺。步骤可分为五步,“斩竹漂塘”、“煮楻足火”、“荡料入帘”、“覆帘压纸”、“透火焙干”。其中不涉及实验室基本操作的是
| A.加热 | B.过滤 | C.蒸馏 | D.干燥 |
您最近一年使用:0次
解题方法
2 . 海水晒盐后的粗盐样品中,除氯化钠外还含有MgCl2、Na2SO4和CaCl2等可溶性杂质,欲通过下列流程得到较纯净的NaCl固体。下列说法正确的是
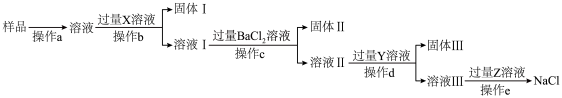
| A.X为NaOH | B.固体Ⅲ为纯净物 |
| C.操作a~d均用到玻璃棒,且作用相同 | D.操作e是蒸发浓缩、冷却结晶、过滤 |
您最近一年使用:0次
7日内更新
|
77次组卷
|
2卷引用:河北省唐山市2024-2025学年高三上学期摸底演练化学试题
解题方法
3 . 实验室模拟工业硫酸镍(除 外,还含有少量
外,还含有少量 等)制备高纯硫酸镍的实验过程可表示为
等)制备高纯硫酸镍的实验过程可表示为 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)如下表。
计算)如下表。
(1)“氧化”的目的是___________ 。
(2)下列可以替代 调节
调节 的是
的是___________ (填字母)。滤渣Ⅰ的化学式为___________ 。
A. B.
B. C.
C. D.
D.
(3)滤渣Ⅱ的化学式为___________ 。该步骤用到的玻璃仪器有烧杯、___________ 、___________ 。
(4)高纯硫酸镍可用于制备镍镉电池正极材料 。
。
① 中
中 的化合价为
的化合价为___________ 。
②写出在强碱溶液中用 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:___________ 。
 外,还含有少量
外,还含有少量 等)制备高纯硫酸镍的实验过程可表示为
等)制备高纯硫酸镍的实验过程可表示为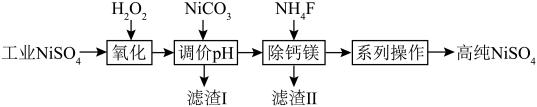
 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)如下表。
计算)如下表。| 金属离子 | 开始沉淀的 | 沉淀完全的 |
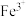 | 1.9 | 3.2 |
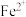 | 7.0 | 9.0 |
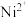 | 7.2 | 9.2 |
(1)“氧化”的目的是
(2)下列可以替代
 调节
调节 的是
的是A.
 B.
B. C.
C. D.
D.
(3)滤渣Ⅱ的化学式为
(4)高纯硫酸镍可用于制备镍镉电池正极材料
 。
。①
 中
中 的化合价为
的化合价为②写出在强碱溶液中用
 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:
您最近一年使用:0次
名校
4 . 海带提碘流程如下:
①酒精灯②烧杯③坩埚④分液漏斗⑤250 mL容量瓶⑥玻璃棒⑦漏斗⑧蒸发皿
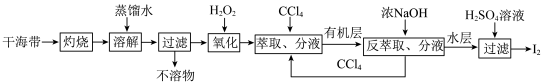
①酒精灯②烧杯③坩埚④分液漏斗⑤250 mL容量瓶⑥玻璃棒⑦漏斗⑧蒸发皿
| A.①②④⑥⑦ | B.①②③④⑤⑦ | C.①②④⑥⑦⑧ | D.①②③④⑥⑦ |
您最近一年使用:0次
2024-09-16更新
|
130次组卷
|
3卷引用:山东省日照市2023-2024学年高三上学期期中考试化学试题
解题方法
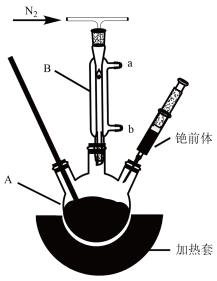
5 . 实验室制备一种钙钛矿型复合物[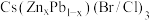 ]的方法如下:
]的方法如下:
实验用品:氯化锌(ZnCl2)、溴化铅(PbBr2)、碳酸铯(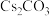 )、十八烯(
)、十八烯(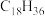 )、油酸(
)、油酸( )、油胺(
)、油胺(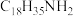 )。
)。
①将适量ZnCl2、0.2gPbBr2、20mL十八烯加入仪器A中,抽气后通入N2,重复3次;
②将混合物升温至120℃进行干燥,注入一定量油酸、油胺,待溶液澄清透明后升温到165℃,迅速注入铯前体,5s后停止反应;
③将步骤②中所得混合物与乙酸甲酯按一定比例混合后离心,分离出沉淀;
④将步骤③中所得沉淀溶解在正己烷中,加入乙酸甲酯离心,再次分离出沉淀,所得沉淀溶解在正庚烷中,离心除去剩余固体,上层清液即为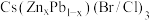 纳米晶体的分散系。
纳米晶体的分散系。
回答下列问题:
(1)仪器B的名称是_______ 。
(2)抽气后通入N2的目的是_______ ,重复3次的原因是_______ 。
(3)铯前体是由碳酸铯与过量的油酸加热时反应得到的产物,生成铯前体的化学方程式为____ 。
(4)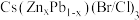 在下列物质中的溶解性最差的是
在下列物质中的溶解性最差的是_______ 。
A.正己烷 B.正庚烷 C.乙酸甲酯
(5)步骤③中乙酸甲酯的作用是_______ 。
(6)可用电感耦合等离子体质谱(ICP—MS)来确定产品[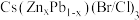 ]中各元素的含量。取0.6g产品溶于稀硝酸,测得锌的含量为
]中各元素的含量。取0.6g产品溶于稀硝酸,测得锌的含量为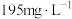 、铅为
、铅为 ,则x的值是
,则x的值是_______ 。
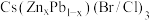 ]的方法如下:
]的方法如下:实验用品:氯化锌(ZnCl2)、溴化铅(PbBr2)、碳酸铯(
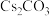 )、十八烯(
)、十八烯(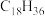 )、油酸(
)、油酸( )、油胺(
)、油胺(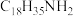 )。
)。
①将适量ZnCl2、0.2gPbBr2、20mL十八烯加入仪器A中,抽气后通入N2,重复3次;
②将混合物升温至120℃进行干燥,注入一定量油酸、油胺,待溶液澄清透明后升温到165℃,迅速注入铯前体,5s后停止反应;
③将步骤②中所得混合物与乙酸甲酯按一定比例混合后离心,分离出沉淀;
④将步骤③中所得沉淀溶解在正己烷中,加入乙酸甲酯离心,再次分离出沉淀,所得沉淀溶解在正庚烷中,离心除去剩余固体,上层清液即为
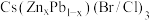 纳米晶体的分散系。
纳米晶体的分散系。回答下列问题:
(1)仪器B的名称是
(2)抽气后通入N2的目的是
(3)铯前体是由碳酸铯与过量的油酸加热时反应得到的产物,生成铯前体的化学方程式为
(4)
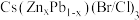 在下列物质中的溶解性最差的是
在下列物质中的溶解性最差的是A.正己烷 B.正庚烷 C.乙酸甲酯
(5)步骤③中乙酸甲酯的作用是
(6)可用电感耦合等离子体质谱(ICP—MS)来确定产品[
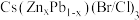 ]中各元素的含量。取0.6g产品溶于稀硝酸,测得锌的含量为
]中各元素的含量。取0.6g产品溶于稀硝酸,测得锌的含量为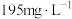 、铅为
、铅为 ,则x的值是
,则x的值是
您最近一年使用:0次
6 . 为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):_______ ,第⑤步中,操作B用到的玻璃仪器是_______ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)_______ 。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是_______ 。
(4)判断BaCl2已过量的方法是_______ 。
(5)下列是某学生设计操作A后混合液中Cl-、 的检验步骤请根据内容填空:
的检验步骤请根据内容填空:
①首先检验_______ 离子,应先加入过量的_______ 。
②将所得混合物_______ (填操作名称),然后在滤液中加入试剂_______ 检验另一离子。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):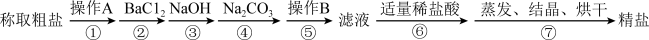
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
(4)判断BaCl2已过量的方法是
(5)下列是某学生设计操作A后混合液中Cl-、
 的检验步骤请根据内容填空:
的检验步骤请根据内容填空:①首先检验
②将所得混合物
您最近一年使用:0次
7 . 下列分离提纯的方法错误的是
| A.重结晶法提纯含有少量食盐和泥沙的苯甲酸 |
| B.萃取法分离Br2和苯 |
| C.升华法除去NaCl(s)中的I2(s) |
| D.蒸馏法分离CH2Cl2和CCl4 |
您最近一年使用:0次
解题方法
8 . 某课题组设计合成了负极材料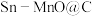 ,某简易流程如图所示(部分反应物、产物和条件省略):
,某简易流程如图所示(部分反应物、产物和条件省略):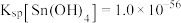 。
。
请回答下列问题:
(1)操作1前,反应物混合溶液要不断搅拌,其目的是___________ 。
(2)在实验室中完成操作1需要的玻璃仪器有___________ (填名称)。
(3) 和
和 表面吸附有
表面吸附有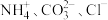 等,检验固体是否洗净的操作是
等,检验固体是否洗净的操作是___________ 。
(4)操作3包括蒸发浓缩、___________ 、过滤、洗涤、干燥。利用如图所示装置除去 固体中少量杂质,提纯氯化铵。
固体中少量杂质,提纯氯化铵。___________ ;扎有小孔的滤纸的用途是___________ 。
(5)已知:离子浓度小于或等于 时认为离子已沉淀完全。常温下,
时认为离子已沉淀完全。常温下, 完全沉淀时溶液
完全沉淀时溶液 最小为
最小为___________ 。
(6)写出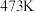 时发生反应的化学方程式:
时发生反应的化学方程式:___________ 。
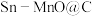 ,某简易流程如图所示(部分反应物、产物和条件省略):
,某简易流程如图所示(部分反应物、产物和条件省略):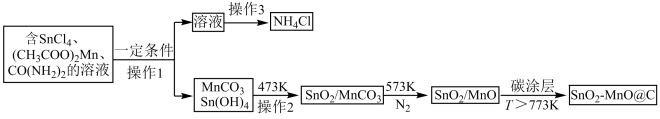
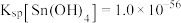 。
。请回答下列问题:
(1)操作1前,反应物混合溶液要不断搅拌,其目的是
(2)在实验室中完成操作1需要的玻璃仪器有
(3)
 和
和 表面吸附有
表面吸附有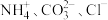 等,检验固体是否洗净的操作是
等,检验固体是否洗净的操作是(4)操作3包括蒸发浓缩、
 固体中少量杂质,提纯氯化铵。
固体中少量杂质,提纯氯化铵。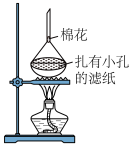
(5)已知:离子浓度小于或等于
 时认为离子已沉淀完全。常温下,
时认为离子已沉淀完全。常温下, 完全沉淀时溶液
完全沉淀时溶液 最小为
最小为(6)写出
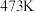 时发生反应的化学方程式:
时发生反应的化学方程式:
您最近一年使用:0次
解题方法
9 . 化学与社会、生产、生活、环境等密切相关。下列说法不正确 的是。
A.泡沫灭火器可用于钠着火的灭火。其成分是 和 和 |
| B.2023年亚运会用可降解聚乳酸塑料代替聚乙烯塑料作为吉祥物手办材料之一,可减少白色污染 |
| C.描述焰色试验的诗句有“纷纷灿烂如星陨,㸌㸌喧豗似火攻”,该现象与原子光谱有关 |
| D.东晋葛洪《肘后备急方》中称“青蒿一握,以水二升渍,绞取汁”,操作中“渍”和“绞”分别表示浸取和过滤 |
您最近一年使用:0次
解题方法
10 . 高铁酸钾(K2FeO4)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下。下列说法错误的是

| A.“反应Ⅰ”中,氧化剂和还原剂的物质的量之比为2:3 |
| B.过滤操作需要用到的玻璃仪器有漏斗、玻璃棒和烧杯 |
| C.将K2FeO4与盐酸混合使用,会降低其杀菌消毒的效果 |
| D.“转化”时,反应能进行的原因是该条件下K2FeO4的溶解度小于Na2FeO4 |
您最近一年使用:0次



