1 . 氯化铁和高铁酸钾都是常见的水处理剂。某兴趣小组以铁屑为原料模拟工业上制备氯化铁及进一步氧化制备高铁酸钾的流程如下:
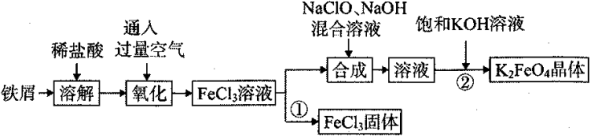
请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是____________ 。
(2)“合成”阶段生成Na2FeO4的离子方程式为___________________________ 。
(3)为了检验“氧化”过程中所得FeCl3 溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是_______ (填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性KMnO4溶液进行检验,请分析方案是否合理,并说明理由:____________ 。
(4)过程①制取FeCl3固体的具体操作步骤是__________________________ 。若使6.4mol/LFeCl3饱和溶液不析出Fe(OH)3,需控制溶液的pH小于____ 。{已知该实验条件下,Ksp[(Fe(OH)3]=8.5×10-36,Kw=1.1×10-13,1.13≈1.33}
(5)在不同温度和不同pH 下,FeO42-的稳定性如下图所示:
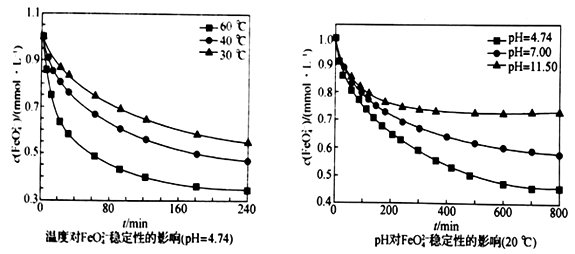
从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为______________________ 。

请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是
(2)“合成”阶段生成Na2FeO4的离子方程式为
(3)为了检验“氧化”过程中所得FeCl3 溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性KMnO4溶液进行检验,请分析方案是否合理,并说明理由:
(4)过程①制取FeCl3固体的具体操作步骤是
(5)在不同温度和不同pH 下,FeO42-的稳定性如下图所示:

从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为
您最近一年使用:0次
2018-03-15更新
|
767次组卷
|
3卷引用:河北省衡水中学2018年高三下学期期初考试(3月)理综化学试题
2 . 下列有关离子检验的操作、现象及结论均正确的是
| A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则该溶液中一定不含K+ |
| B.向无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀出现,则该溶液中一定含有SO42﹣ |
| C.向无色溶液中加入盐酸产生能使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32﹣ |
| D.向某溶液中加入KSCN溶液无现象,再滴入少量H2O2 , 呈血红色,则该溶液中一定含有Fe2+ |
您最近一年使用:0次
2018-01-10更新
|
221次组卷
|
3卷引用:河南省林州一中分校(林虑中学)2017-2018学年高一下学期开学考试化学试题
3 . 检验某溶液X中是否含有 Na+、K+、Fe3+、Mg2+、Iˉ、Cl-、CO32ˉ、SO42ˉ,限用的试剂有:盐酸、硫酸、硝酸银溶液、硝酸钡溶液。设计如下实验步骤,并记录相关现象。下列叙述不正确 的是
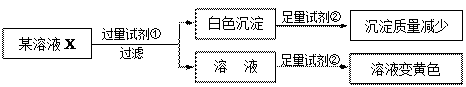

| A.溶液X中一定含有Iˉ、CO32ˉ、SO42ˉ |
| B.通过在黄色溶液中加入硝酸银溶液可以检验溶液X中是否存在Cl- |
| C.试剂①为硝酸钡溶液 |
| D.通过焰色反应,可确认溶液X中阳离子的种类 |
您最近一年使用:0次
2017-08-09更新
|
310次组卷
|
2卷引用:浙江省瑞安市上海新纪元高级中学2019-2020学年高一(1-6)班下学期期初考试化学试题
4 . 对于某些离子的检验及结论一定正确的是
| A.加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO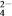 |
C.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则溶液中有CO |
| D.如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素 |
您最近一年使用:0次
5 . 下列有关实验的设计、现象、结论均正确的是
| A.加热固体,用湿润的红色石蕊试纸靠近,看颜色变化,用此法鉴别固体是否为铵盐 |
| B.用短胶头滴管向FeSO4溶液滴加NaOH溶液,产生的白色沉淀可长时间存在 |
| C.将金属钠投入CuSO4溶液,可观察到有红色固体析出 |
| D.向25mL沸腾的蒸馏水中逐滴加入5-6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色, 停止加热,便得到Fe(OH)3胶体 |
您最近一年使用:0次
名校
6 . 下列根据实验操作或现象得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | KBrO3溶液中加入少量苯,然后通入少量Cl2,有机相呈橙色 | 氧化性:Cl2>Br2 |
B | 室温下,向浓度均为0.1mol•L-1的KCl和KI混合溶液中滴加几滴AgNO3溶液,只出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
C | 向1mL1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡后再加入0.5mL有机物Y,加热,未出现砖红色沉淀。 | Y中不含有醛基 |
D | 已知NaClO2溶液的pH>7,将其蒸干并灼烧得到固体残留物。 | 该固体为NaClO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 某溶液可能含有NH4+、K+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,现取l00mL溶液加入少量溴水,溶液呈无色。继续滴加足量HNO3和Ba(NO3)2混合溶液,产生沉淀,沉淀经洗涤、高温干燥后质量为4.66g。滤液加足量NaOH溶液、加热,生成气体在标准状况下体积为1120mL。根据上述实验,以下推测正确的是
| A.原溶液肯定只存在NH4+、SO32- |
| B.原溶液一定不含Ba2+、Fe3+、I- |
| C.原溶液可能存在K+、SO42- |
| D.另取试液滴加足量盐酸、BaCl2溶液,即可确定溶液离子组成 |
您最近一年使用:0次
名校
8 . 下列根据实验操作和现象得出结论不正确的是
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 硝酸银溶液中加足量的NaCl溶液,再加KI溶液 | 先得到白色沉淀后变为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | 相同时间内,HA收集到的氢气多 | HA是弱酸 |
| D | 用洁净的铂丝蘸待测液进行焰色反应 | 火焰呈黄色 | 溶液中含Na+,不含K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D为四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的一种,阴离子分别是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 中的一种(离子在物质中不能重复出现)。现做如下实验:
中的一种(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色;
②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题。
(1)写出A、C的化学式:A_______ ,C_______ 。
(2)写出盐酸与D反应的离子方程式:_______ 。
(3)写出C与Ba(OH)2溶液反应的离子方程式:_______ 。
 、SO
、SO 、Cl-、CO
、Cl-、CO 中的一种(离子在物质中不能重复出现)。现做如下实验:
中的一种(离子在物质中不能重复出现)。现做如下实验:①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色;
②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题。
(1)写出A、C的化学式:A
(2)写出盐酸与D反应的离子方程式:
(3)写出C与Ba(OH)2溶液反应的离子方程式:
您最近一年使用:0次
2017-02-17更新
|
545次组卷
|
10卷引用:云南省镇沅县第一中学2021-2022学年高二下学期开学考试化学试题
云南省镇沅县第一中学2021-2022学年高二下学期开学考试化学试题2016-2017学年广西钦州港区高一上11月月考化学卷吉林省长春市榆树市第一高级中学2019-2020学年高一上学期尖子生考试化学试题黑龙江省哈尔滨市第一中学2021-2022学年高一上学期期中考试化学试题 山东省“学情空间”区域教研共同体2022-2023学年高一上学期10月联考(人教版)化学试题湖南省长沙市南雅中学2022-2023学年高一上学期第一次月考化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高一上学期11月期中检测化学试题湖南省长沙市南雅中学2023-2024学年高一上学期第一次月考化学试题云南省曲靖市罗平县第一中学2023-2024学年高一上学期9月月考化学试题河南省郑州市第四高级中学2023-2024学年高一上学期西藏班第二次调研考试 化学试题
10 . 某白色固体可能由①NH4Cl、②AlCl3、③NaCl、④AgNO3、⑤KOH中的一种或几种组成,此固体投入水中得澄清溶液,该溶液可使酚酞呈红色,若向溶液中加稀硝酸到过量,最终有白色沉淀生成。对原固体的判断不正确的是
| A.肯定存在① | B.至少存在②和⑤ |
| C.无法确定是否有③ | D.至少存在①④⑤ |
您最近一年使用:0次
2016-12-09更新
|
90次组卷
|
3卷引用:2016-2017学年广东省汕头市金山中学高二上学期入学考试化学试卷



