1 . 下列“实验结论”与“实验操作及现象”相符的一组是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中一定含有 |
| B | 向某溶液中加入KSCN溶液,溶液变为红色 | 该溶液中一定含有 |
| C | 向某溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中一定含有 |
| D | 向某溶液中加入稀盐酸,有无色气体产生 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-14更新
|
487次组卷
|
13卷引用:北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题
北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题天津市南开区2023年普通高中学业水平合格性考试模拟练习化学试题(已下线)专题六 物质的电离与离子反应(已下线)合格考真题汇编22化学实验基础二(已下线)专题二 物质的检验、除杂和鉴别云南省红河州弥勒市中小学2018-2019学年高一下学期期末考试化学试题内蒙古集宁一中(西校区)2020—2021学年高一下学期第一次月考化学试题北京第七中学2020-2021学年高一下学期期中考试化学试题北京市朝阳区2021-2022学年高一年级下学期合格考模拟检测化学试题北京景山学校2021-2022学年高一下学期期中考试化学试题北京市第十一中学2021-2022学年高一下学期6月月考化学试题北京市顺义区杨镇第一中学2021-2022学年高一下学期期中考试化学试题北京市第十五中学2023-2024学年高一下学期期中考试化学试题
2 . 下列鉴别或检验不能达到实验目的的是
| A.用石灰水鉴别Na2CO3与NaHCO3 |
| B.用KSCN溶液检验FeSO4是否变质 |
| C.用盐酸酸化的BaCl2溶液检验Na2SO3是否被氧化 |
| D.加热条件下用银氨溶液检验乙醇中是否混有乙醛 |
您最近一年使用:0次
2023-06-13更新
|
10122次组卷
|
20卷引用:2023年高考辽宁卷化学真题
2023年高考辽宁卷化学真题(已下线)T4-化学实验基础(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)甘肃省武威市凉州区2024届高三上学期第一次诊断考试化学试题四川省成都市第七中学2023-2024学年高三上学期入学考试理综化学试题(已下线)考点45 物质的分离、提纯和检验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期9月月考化学试题(已下线)考点2 物质的分离、提纯、检验与鉴别 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)天津市红桥区2023-2024学年高三上学期期中考试化学试题(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型03 离子方程式正误判断 离子共存、检验和推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)热点09 物质的分离、提纯、检验与鉴别(已下线)FHgkyldyjhx13(已下线)测试辽宁化学 请勿下载(已下线)第03讲 离子共存、离子的检验与推断(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
3 . 胆矾(CuSO4·5H2O)又名蓝矾,是化学工业、医药领域中的常见物质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加_______ 至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;
③另取少量①所得溶液,加入足量的_______ 溶液,出现白色沉淀;
④取③中所得上层清液,加入_______ 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=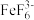 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6
请回答:步骤①中,加入足量NaF溶液的可能原因是_______ ,若不加NaF溶液,可导致最终的测量值_______ (填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为_______ ; 若Na2S2O3标准溶液的平均用量为10.00 mL,则产品中胆矾的质量分数为_______ 。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加
③另取少量①所得溶液,加入足量的
④取③中所得上层清液,加入
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=
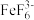 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6请回答:步骤①中,加入足量NaF溶液的可能原因是
您最近一年使用:0次
名校
4 . 一种由铜镉渣生产金属镉的流程如下:(铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。)
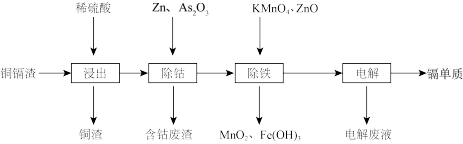
下表列出了相关金属离子生成氢氧化物沉淀的pH
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出。写出通空气将Cu氧化浸出的离子方程式___________ 。
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3,该微电池的正极反应式为_______ 。
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=___________ 。
②除铁时加入ZnO控制反应液pH的范围为___________ 。
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:___________ 。
(5)净化后的溶液可电解获得镉单质。镉的金属性___________ 金属铜(填“强于”或“弱于”)。

下表列出了相关金属离子生成氢氧化物沉淀的pH
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3,该微电池的正极反应式为
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=
②除铁时加入ZnO控制反应液pH的范围为
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:
(5)净化后的溶液可电解获得镉单质。镉的金属性
您最近一年使用:0次
2023-06-02更新
|
99次组卷
|
2卷引用:江苏省海头高级中学2022-2023学年高一下学期模拟考试化学试题
名校
5 . 下列离子的检验方案、现象及结论不正确的是
| 选项 | 检验方案 | 现象 | 结论 |
| A | 向某溶液中加入足量盐酸,再加 溶液 溶液 | 产生白色沉淀 | 原溶液中含 |
| B | 向某溶液中加足量NaOH后,加热 | 产生能使湿润蓝色石蕊试纸变红的气体 | 原溶液中含 |
| C | 向某溶液中加入 溶液 溶液 | 产生白色沉淀 | 原溶液中不一定含 |
| D | 向某溶液中滴加KSCN溶液后,再滴加氯水 | 溶液变为红色 | 原溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 检验下列物质所选用的试剂正确的是
| A.H2S气体:NaOH溶液 |
B.溶液中的CO :盐酸,澄清石灰水 :盐酸,澄清石灰水 |
C.溶液中的SO : Ba(NO3)2溶液 : Ba(NO3)2溶液 |
| D.溶液中的Cu2+:氨水 |
您最近一年使用:0次
7 . 某化学学习小组在帮助老师整理实验室的化学试剂时,发现一瓶无色溶液,标签破损如下图,据老师回忆,该药品应该是中学化学常用试剂。该小组同学根据已掌握的知识,对溶液进行鉴定。下列说法正确的是
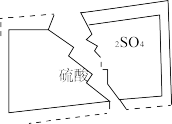

A.该小组同学推测它的阳离子可能是 、 、 、 、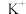 、 、 中的某一个 中的某一个 |
B.若要证明阳离子是否为 ,其方法是:取少量溶液于试管中加稀NaOH溶液,加热,若产生能使湿润的蓝色石蕊试纸变红的气体,则阳离子为 ,其方法是:取少量溶液于试管中加稀NaOH溶液,加热,若产生能使湿润的蓝色石蕊试纸变红的气体,则阳离子为 |
C.某同学操作时不慎将一滴溶液滴落在纸上,纸变黑,说明该溶液为 |
| D.验证阳离子是否为K+的实验方法是焰色反应直接观察火焰是否呈紫色 |
您最近一年使用:0次
解题方法
8 . 某白色粉末中可能含 、
、 、
、 、
、 和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
步骤一:取少量白色粉末溶于水,没有气体逸出,得到无色透明溶液①;
步骤二:向溶液①中滴加稀硫酸,产生浅黄色固体和气体X;
步骤三:将气体X通入 溶液、产生黑色沉淀。
溶液、产生黑色沉淀。
根据上述现象,下列关于该白色粉末的说法中正确的是
 、
、 、
、 、
、 和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:步骤一:取少量白色粉末溶于水,没有气体逸出,得到无色透明溶液①;
步骤二:向溶液①中滴加稀硫酸,产生浅黄色固体和气体X;
步骤三:将气体X通入
 溶液、产生黑色沉淀。
溶液、产生黑色沉淀。根据上述现象,下列关于该白色粉末的说法中正确的是
A.白色粉末一定不含有 和NaCl 和NaCl |
B.白色粉末中 和 和 的物质的量之比大于2 的物质的量之比大于2 |
| C.黑色沉淀不溶于硝酸 |
| D.向溶液①中加入硝酸银可以检验氯离子是否存在 |
您最近一年使用:0次
名校
解题方法
9 . 混合物的水溶液中只可能含有以下离子中的若干种: 、
、 、Mg2+、Ba2+、K+、
、Mg2+、Ba2+、K+、 、
、 ,现取三份体积均为100mL的该溶液进行如下实验:第一份加入AgNO3;溶液有沉淀产生;第二份加入足量NaOH溶液并加热,收集到气体0.04mol;第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到沉淀6.27g,再用足量盐酸洗涤、干燥,沉淀质量减少为2.33g。根据上述实验,下列有关该溶液组成的推断正确的是
,现取三份体积均为100mL的该溶液进行如下实验:第一份加入AgNO3;溶液有沉淀产生;第二份加入足量NaOH溶液并加热,收集到气体0.04mol;第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到沉淀6.27g,再用足量盐酸洗涤、干燥,沉淀质量减少为2.33g。根据上述实验,下列有关该溶液组成的推断正确的是
 、
、 、Mg2+、Ba2+、K+、
、Mg2+、Ba2+、K+、 、
、 ,现取三份体积均为100mL的该溶液进行如下实验:第一份加入AgNO3;溶液有沉淀产生;第二份加入足量NaOH溶液并加热,收集到气体0.04mol;第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到沉淀6.27g,再用足量盐酸洗涤、干燥,沉淀质量减少为2.33g。根据上述实验,下列有关该溶液组成的推断正确的是
,现取三份体积均为100mL的该溶液进行如下实验:第一份加入AgNO3;溶液有沉淀产生;第二份加入足量NaOH溶液并加热,收集到气体0.04mol;第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到沉淀6.27g,再用足量盐酸洗涤、干燥,沉淀质量减少为2.33g。根据上述实验,下列有关该溶液组成的推断正确的是| A.一定不存在K+ | B.可能存在Cl- |
C.含有 ,其浓度为0.1mol/L ,其浓度为0.1mol/L | D.可能存在Mg2+、Ba2+ |
您最近一年使用:0次
2023-05-14更新
|
1071次组卷
|
5卷引用:陕西省西安市第七十五中学2022-2023学年高一上学期期末结业化学试题
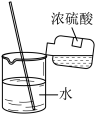
10 . 下列有关实验的装置、操作和结论或原因均正确的是
| 选项 | 装置 | 实验操作 | 结论或原因 |
| A |
| 将浓硫酸沿烧杯壁缓慢倒入装有蒸馏水的烧杯中,并用玻璃棒不断搅拌,用手接触烧杯外壁,感觉到烧杯发热 | 说明浓硫酸稀释是放热过程 |
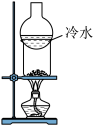
| B |
| 用如图装置分离I2和NH4Cl的固体混合物 | 碘单质受热易升华,遇冷又发生凝华 |
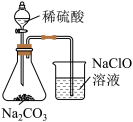
| C |
| 将分液漏斗活塞打开一段时间后,锥形瓶中有气体产生,烧杯中有气泡逸出 | 说明非金属性S>C>Cl |
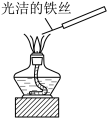
| D |
| 用干燥洁净的铁丝蘸取待测溶液,在酒精灯火焰处燃烧,观察火焰颜色,判断是否存在钾元素 | 钾元素的焰色反应为紫色。 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-27更新
|
206次组卷
|
2卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题