1 . 化合物X由三种元素组成,某实验小组按如下流程进行相关实验。

请回答:
(1)组成X的三种元素为___________ ;X的化学式为___________ 。
(2)溶液B的溶质组成为___________ (用化学式表示)。
(3)①写出由X转化为A的化学方程式:___________ 。
②写出由B转化为C的离子方程式:___________ 。
(4)设计简单实验,写出检验尾气中气体成分的方法:___________ 。

请回答:
(1)组成X的三种元素为
(2)溶液B的溶质组成为
(3)①写出由X转化为A的化学方程式:
②写出由B转化为C的离子方程式:
(4)设计简单实验,写出检验尾气中气体成分的方法:
您最近一年使用:0次
名校
解题方法
2 . 王老师上课做了“木炭在氧气中燃烧”的实验:将点燃的木炭缓缓地伸入集满氧气的集气瓶中,将木炭取出后向集气瓶中倒入少量澄清石灰水后振荡,让大家观察。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
(2)木炭伸入集气瓶中后所观察到的现象是:___________ ,大家根据___________ 现象,可判断木炭燃烧时生成了二氧化碳。
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有___________ 气体。下课后,小华将自己的想法说给老师听,在老师的帮助下,小华对集气瓶中的气体作如下探究:

实验中,当观察到___________ 现象,说明小华的猜想是正确的,请写出直玻璃管中发生反应的化学方程式:___________ 。
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是___________ 。通过检验,集气瓶中还有氧气剩余,请设计实验进行验证___________ 。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
| A.让同学们观察得更清楚 | B.让木炭与氧气充分反应 |
| C.保证实验时的安全 | D.老师的动作都很慢 |
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有

实验中,当观察到
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是
您最近一年使用:0次
名校
解题方法
3 . 硫酸亚铁在工农业生产中具有广泛的应用。该物质不稳定,受热易分解产生氧化物,具有较强的还原性。某学习小组利用如下装置来探究FeSO4受热分解的产物。
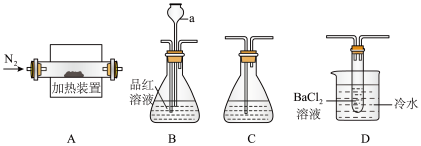
(1)甲组同学利用“A接B接C”的装置来验证产物中含有SO2气体。
①连接好装置后,接下来的操作是_______ 。
②仪器a的名称是_______ ;其作用是_______ 。
(2)乙组同学查阅资料得:硫酸亚铁分解的气体产物中除SO2外还有SO3;SO3的熔点为16.8℃,沸点是46.8℃,溶于水放出大量的热,易形成酸雾。为此设计了“A接D接C”的装置验证产物中含有SO3。
①装置D中的现象是_______ ,BaCl2溶液不能用Ba(NO3)2溶液代替的原因是_______ 。
②装置A中固体变为红棕色,结合两组同学的实验,写出硫酸亚铁分解的化学方程式_______ ;

(1)甲组同学利用“A接B接C”的装置来验证产物中含有SO2气体。
①连接好装置后,接下来的操作是
②仪器a的名称是
(2)乙组同学查阅资料得:硫酸亚铁分解的气体产物中除SO2外还有SO3;SO3的熔点为16.8℃,沸点是46.8℃,溶于水放出大量的热,易形成酸雾。为此设计了“A接D接C”的装置验证产物中含有SO3。
①装置D中的现象是
②装置A中固体变为红棕色,结合两组同学的实验,写出硫酸亚铁分解的化学方程式
您最近一年使用:0次
名校
解题方法
4 . 摩尔盐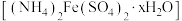 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是___________ 。
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有___________ 。取样品 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为___________ (用含a、b的代数式表示)。
(3)利用摩尔盐分解产生的 ,可制取氯化亚砜
,可制取氯化亚砜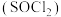 :
: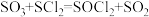 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
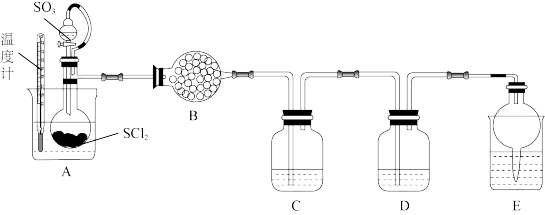
①装置B为无水 ,其作用是
,其作用是___________ 。
②装置C和装置D中的试剂分别是___________ 、___________ (填小写字母)。
a. 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液
(4)利用摩尔盐分解产生的 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
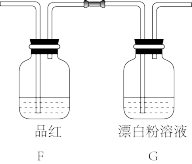
①将少量 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是___________ (用化学反应方程式表示)。
②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是___________ ,其作用是___________ ,通过___________ (填现象)即可证明亚硫酸的酸性强于次氯酸。
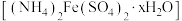 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有
 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为(3)利用摩尔盐分解产生的
 ,可制取氯化亚砜
,可制取氯化亚砜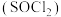 :
: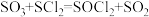 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
①装置B为无水
 ,其作用是
,其作用是②装置C和装置D中的试剂分别是
a.
 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液(4)利用摩尔盐分解产生的
 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
①将少量
 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是
您最近一年使用:0次
2022-07-15更新
|
303次组卷
|
2卷引用:河南省开封市五县2021-2022学年高二下学期期末考试化学试题
解题方法
5 . 某化学小组制备 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):

(1)仪器a的名称是___________ 。
(2)装置A制取 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的___________ 性,___________ (填“能”或“不能”)用浓硝酸代替。
(3)在滴加浓硫酸之前,需先通入一段时间的 ,此操作的目的是
,此操作的目的是___________ 。
(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为___________ 。
(5)装置D验证了 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:___________ 。
(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: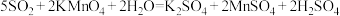 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为___________ 。
 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):
(1)仪器a的名称是
(2)装置A制取
 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的(3)在滴加浓硫酸之前,需先通入一段时间的
 ,此操作的目的是
,此操作的目的是(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为
(5)装置D验证了
 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性
 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: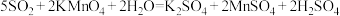 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
2022-07-04更新
|
280次组卷
|
2卷引用:河南省平顶山市2021-2022学年高一下学期期末调研化学试题
解题方法
6 . 将不同质量的 与
与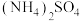 (物质的量之比均为2:1)混合样品分别加入
(物质的量之比均为2:1)混合样品分别加入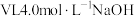 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
下列说法错误的是
 与
与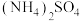 (物质的量之比均为2:1)混合样品分别加入
(物质的量之比均为2:1)混合样品分别加入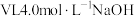 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:| 序号 | ① | ② |
| 铵盐的质量/g | 9.05 | 18.10 |
| 浓硫酸增加的质量/g | m | m |
| A.加热逸出的气体能使湿润的红色石蕊试纸变蓝 |
B.①中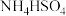 与NaOH溶液反应的离子方程式为 与NaOH溶液反应的离子方程式为 |
C.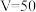 |
| D.当铵盐的质量为36.2g时,恰好与碱反应无气体产生 |
您最近一年使用:0次
7 . 莫尔盐也叫硫酸亚铁铵,是一种重要的化工原料,可作净水剂。在不同温度下其分解产物不同,如图为500℃时隔绝空气加热,探究其分解生成的气体产物的装置。下列说法不正确的是
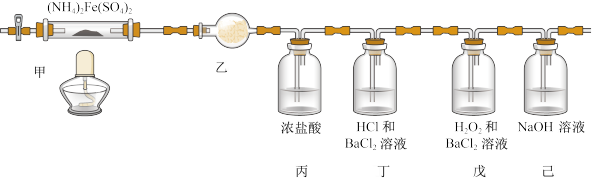

| A.乙装置的干燥管盛装无水硫酸铜检验分解产物中可能含有的水 |
| B.丙中浓盐酸检验可能的分解产物NH3,浓盐酸可用浓硝酸代替 |
| C.若分解产物有SO2,无SO3,则丁装置中无现象,戊装置中有白色沉淀生成 |
| D.己装置吸收实验尾气,防止酸性气体对环境造成污染 |
您最近一年使用:0次
2021-05-11更新
|
1806次组卷
|
4卷引用:云南省昭通市永善、绥江县2021-2022学年高一3月月考化学试题
名校
解题方法
8 . 某校化学研究性学习小组探究足量的镁与浓硫酸反应。回答下列问题:
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有 、
、 。
。
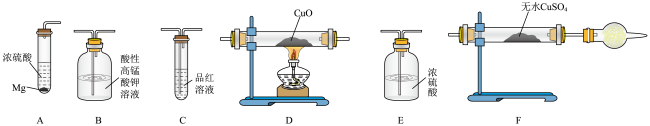
 若按气体从左到右的流向,各装置的连接顺序是
若按气体从左到右的流向,各装置的连接顺序是________  填字母编号
填字母编号 。
。
 已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为
已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为________ mol/L。
 装置C的作用是
装置C的作用是________ 。
 证明混合气体中含有H2的实验现象为
证明混合气体中含有H2的实验现象为________ 。
Ⅱ.乙同学设计如图实验测定混合气体中SO2的含量。
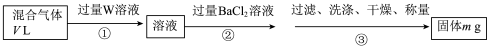
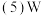 溶液可以是
溶液可以是________  填字母
填字母 。
。
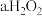 溶液
溶液
 酸性
酸性 溶液
溶液 硫酸酸化
硫酸酸化
 溴水
溴水
 步骤
步骤 中洗涤沉淀的操作为
中洗涤沉淀的操作为________ 。
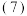 通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量
通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量 体积分数
体积分数 为
为________  用含V、m的代数式表示
用含V、m的代数式表示 。
。
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有
 、
、 。
。
 若按气体从左到右的流向,各装置的连接顺序是
若按气体从左到右的流向,各装置的连接顺序是 填字母编号
填字母编号 。
。 已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为
已知装置A中浓硫酸的质量分数为90%,密度ρ=1.47g/mL,该浓硫酸的物质的量浓度为 装置C的作用是
装置C的作用是 证明混合气体中含有H2的实验现象为
证明混合气体中含有H2的实验现象为Ⅱ.乙同学设计如图实验测定混合气体中SO2的含量。
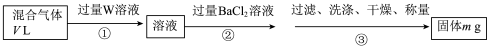
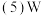 溶液可以是
溶液可以是 填字母
填字母 。
。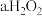 溶液
溶液 酸性
酸性 溶液
溶液 硫酸酸化
硫酸酸化
 溴水
溴水 步骤
步骤 中洗涤沉淀的操作为
中洗涤沉淀的操作为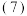 通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量
通过的混合气体体积为VL(已换算成标准状况)时,该混合气体中二氧化硫的含量 体积分数
体积分数 为
为 用含V、m的代数式表示
用含V、m的代数式表示 。
。
您最近一年使用:0次
2020-02-04更新
|
171次组卷
|
2卷引用:甘肃省金昌市永昌县第一高级中学2022-2023学年高三上学期第一次模拟考试化学试题
名校
解题方法
9 . 某校学生课外活动小组的同学设计如图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:【提示:C+CO2 2CO C+H2O(g)
2CO C+H2O(g) CO+H2】
CO+H2】

(1)写出装置A中所发生反应的离子方程式:____________ 。
(2)装置B中最适宜的试剂是________________ 。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是________ 。
(4)按照如图装置进行实验时,首先进行的操作是__________ 。
(5)根据实验中的___________ 现象,可证明CO具有还原性,有关反应的化学方程式是:__________ 。
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在图中装置_____ 与________ 之间连接图中的________ 装置(填序号)。
① NaHCO3溶液 ②
NaHCO3溶液 ② 碱石灰 ③
碱石灰 ③ NaOH溶液 ④
NaOH溶液 ④ 浓H2SO4
浓H2SO4
 2CO C+H2O(g)
2CO C+H2O(g) CO+H2】
CO+H2】
(1)写出装置A中所发生反应的离子方程式:
(2)装置B中最适宜的试剂是
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是
(4)按照如图装置进行实验时,首先进行的操作是
(5)根据实验中的
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在图中装置
①
 NaHCO3溶液 ②
NaHCO3溶液 ② 碱石灰 ③
碱石灰 ③ NaOH溶液 ④
NaOH溶液 ④ 浓H2SO4
浓H2SO4
您最近一年使用:0次
2020-02-01更新
|
97次组卷
|
3卷引用:新疆五家渠市兵团二中金科实验中学2021-2022学年高一下学期开学考试化学试题
名校
解题方法
10 . 某小组为探究K3[Fe(C2O4)3·3H2O(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验。下列有关叙述错误的是
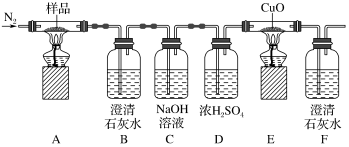

| A.通入氮气的目的有;隔绝空气、使反应产生的气体全部进入后续装置 |
| B.实验中观察到装置F中澄清石灰水变浑浊,装置E中固体变为红色,由此可判断热分解产物中一定含有CO2和CO |
| C.为防止倒吸,停止实验时应进行的操作是:先熄灭装置A、E的酒精灯,冷却后停止通入氮气 |
D.样品完全分解后,取少许装置A中残留物于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,可证明残留物中含有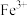 |
您最近一年使用:0次
2020-01-12更新
|
1480次组卷
|
8卷引用:福建省厦门双十中学2022-2023学年高一上学期第二次月考化学试题
福建省厦门双十中学2022-2023学年高一上学期第二次月考化学试题山东省日照一中2020届高三新高考3月份自测化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(二)山东省潍坊昌乐县第二中学2020届高三下学期3月阶段测试化学试题北京市第一七一中学 2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw78【省级联考】湖北省2020年第五届高考测评活动高三元月调考(一模)理综化学试题福建省三明第一中学2023-2024学年高一上学期12月月考化学试题



