1 . 某兴趣小组的同学设计实验制备并探究SO2的性质。回答下列问题:
(1)实验室用废铜屑制备SO2的化学方程式为______ 。
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有______ 性。
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为______ 。
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为______ 。(Cr2O72-被还原为Cr3+)
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=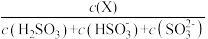 ]随pH的变化如图所示:
]随pH的变化如图所示:
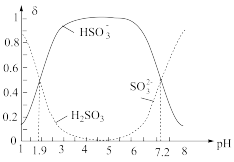
H2SO3的lgKa1=______ ;反应HSO3-+OH- SO32-+H2O的lgK=
SO32-+H2O的lgK=______ ;用0.100mol•L-1NaOH溶液滴入0.100mol•L-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______ 。
(1)实验室用废铜屑制备SO2的化学方程式为
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=
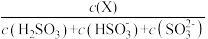 ]随pH的变化如图所示:
]随pH的变化如图所示:
H2SO3的lgKa1=
 SO32-+H2O的lgK=
SO32-+H2O的lgK=
您最近一年使用:0次



