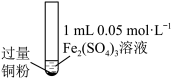
1 . 现有下列实验探究摩尔盐 的化学性质。
的化学性质。
下列解释相应实验现象的离子方程式错误的是
 的化学性质。
的化学性质。装置 | 实验 | 试剂a | 现象 |
| ① | 紫色石蕊溶液 | 溶液变红色 |
② | 过量NaOH溶液 | 产生白色沉淀 | |
③ | 酸性KMnO4溶液 | KMnO4溶液褪色 | |
④ |
| 产生蓝色沉淀 |
A.①中溶液变红: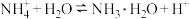 ; ;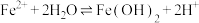 |
B.②中产生白色沉淀: |
C.③中溶液褪色: |
D.④中产生蓝色沉淀: |
您最近一年使用:0次
2 . 根据下列实验的操作和现象,可以说明相应结论的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将乙醇和浓硫酸的混合液加热,将生成的气体通入溴水中 | 溴水褪色 | 乙醇发生了消去反应 |
| B | 取一定质量久置的亚硫酸钠固体于试管中,加蒸馏水完全溶解后,滴加BaCl2溶液 | 产生白色沉淀 | 亚硫酸钠变质 |
| C | 常温下,将两块相同的未经打磨的铝片分别投入5.0mL饱和的CuSO4溶液和CuCl2溶液中 | 前者无明显现象,后者迅速反应,现象明显 | Cl-能加速破坏铝片表面的氧化膜 |
| D | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中缓慢滴加硫酸,黄色变为橙红色 | 增大氢离子浓度,转化平衡向生成 的方向移动 的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某化学兴趣小组欲探究氢氧化镁固体在氯化铵中溶解的原因,进行了如下实验:
已知:①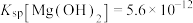 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
关于以上实验,下列说法错误的是
| 操作 | 实验序号 | 试剂X | 实验现象 |
| 实验一 | 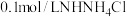 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 |
| 实验二 | 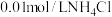 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验三 | 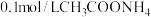 溶液,5.0mL 溶液,5.0mL | 白色浊液逐渐变澄清 | |
| 实验四 | 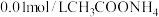 溶液,5.0mL 溶液,5.0mL | 白色浊液变化不明显 | |
| 实验五 | 0.01mol/L蒸馏水,5.0mL | 白色浊液变化不明显 |
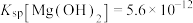 ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。关于以上实验,下列说法错误的是
| A.只通过实验一和二,氢氧化镁溶解可能是铵根或者氢离子作用的结果 |
B.若加入试剂X为0.1mol/LHCl溶液5mL,实验现象为白色浊液逐渐变澄清,与实验一形成对照,可以说明 被 被 溶解 溶解 |
C.实验三和四中加入 可以排除 可以排除 的干扰,因为 的干扰,因为 溶液显中性 溶液显中性 |
D.通过以上四个实验证明, 溶解的原因是和 溶解的原因是和 形成了更难电离的 形成了更难电离的 |
您最近一年使用:0次
名校
解题方法
4 . 下列实验操作和现象所得结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 浓硫酸滴在滤纸上 | 滤纸变黑 | 浓硫酸具有脱水性 |
| B |  通入酸性 通入酸性 溶液中 溶液中 | 酸性 溶液褪色 溶液褪色 |  具有还原性 具有还原性 |
| C |
| 溴水褪色,生成白色沉淀 | 发生了加成反应 |
| D |  通入 通入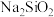 溶液 溶液 | 溶液变浑浊 |  的酸性比 的酸性比 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 本实验将氨的制备与性质探究及尾气处理综合在一起进行一体化创新设计,实验使用氢氧化钠固体与浓氨水在常温下反应快速制备少量氨,省时高效。
(1)图中装置用到的玻璃实验仪器有______________ (填字母)。
a.具支试管 b.干燥管 c.试管架 d.烧瓶 e.烧杯 f.铁架台 g.橡胶塞
(2)①本实验改进了氨极易溶于水的喷泉实验,运用自制紫甘蓝溶液替代常规的水加无色酚酞溶液,使喷泉的颜色由_______________ 色变得绚丽多彩。
表1紫甘蓝指示剂变色范围
②本实验将氨的尾气吸收试剂(常规的吸收试剂为水或稀硫酸)改为水与无水乙醇以体积比1:1混合而成的乙醇溶液,其作用为___________________ 。
(3)实验步骤及现象分析
①检查装置气密性。如图所示连接好装置,打开开关__________________ (填“1”或“2”,下同),关闭开关__________________ ,使整个装置密闭。记录小注射器活塞的初始位置,缓慢向下拉大注射器活塞一段距离,松开大注射器活塞,观察,若大、小注射器活塞均回到原来的位置,则说明装置气密性良好。
②装入试剂,准备实验。本实验增设了氨与氯气的反应实验,增设实验中另选装置用高锰酸钾固体与浓盐酸在常温下反应快速制备氯气,写出该反应的离子方程式:__________________ 。
Ⅱ.探究氨气的还原性
已知:Cu2O为红色固体,在酸性溶液中不稳定: 。
。
(4)用装置A制备氨气,仪器接口的连接顺序为_________________ ,装置B的作用为_________________ ,实验开始前应先通一段时间的N2,其目的是_________________ 。_________________ 。

(1)图中装置用到的玻璃实验仪器有
a.具支试管 b.干燥管 c.试管架 d.烧瓶 e.烧杯 f.铁架台 g.橡胶塞
(2)①本实验改进了氨极易溶于水的喷泉实验,运用自制紫甘蓝溶液替代常规的水加无色酚酞溶液,使喷泉的颜色由
表1紫甘蓝指示剂变色范围
| pH | 1 | 2~3 | 4~6 | 7~9 | 10 | 11 | 12~14 |
| 紫甘蓝溶液颜色变化 | 深红 | 紫红 | 浅紫 | 蓝 | 青 | 绿 | 黄 |
(3)实验步骤及现象分析
①检查装置气密性。如图所示连接好装置,打开开关
②装入试剂,准备实验。本实验增设了氨与氯气的反应实验,增设实验中另选装置用高锰酸钾固体与浓盐酸在常温下反应快速制备氯气,写出该反应的离子方程式:
Ⅱ.探究氨气的还原性
已知:Cu2O为红色固体,在酸性溶液中不稳定:
 。
。(4)用装置A制备氨气,仪器接口的连接顺序为
A. 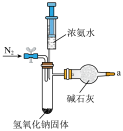 B.
B. 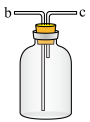 C.
C. 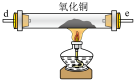 D.
D. 
您最近一年使用:0次
名校
解题方法
6 . 实验小组探究溶液酸碱性对含锰化合物和 氧化还原反应的影响。
氧化还原反应的影响。
资料: .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。
 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。
 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。
 .
.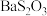 为微溶物。
为微溶物。
已知:实验 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是
 氧化还原反应的影响。
氧化还原反应的影响。资料:
 .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。 .
.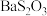 为微溶物。
为微溶物。| 实验 | 序号 | 试剂 | 现象 |
| i.先加试剂a ii.再加试剂b
|  | a:10滴3mol/LH2SO4溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊 |
 | a:10滴蒸馏水 b:20滴0.002mol/LNa2S2O3溶液 | 产生棕黑色沉淀 | |
 | a:x滴6mol/LNaOH溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液变为绿色,无沉淀生成;静置5min,绿色变浅,有棕黑色沉淀生成 |
 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是A.实验 中出现乳白色浑浊发生反应:S2O 中出现乳白色浑浊发生反应:S2O +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
B.实验 所得溶液中 所得溶液中 的检验:取少量溶液加入足量 的检验:取少量溶液加入足量 ,若有白色沉淀生成,则说明有 ,若有白色沉淀生成,则说明有 |
| C.x=10 |
D.实验 产生棕黑色沉淀可能原因是 产生棕黑色沉淀可能原因是 碱性减弱后不稳定生成 碱性减弱后不稳定生成 棕黑色沉淀 棕黑色沉淀 |
您最近一年使用:0次
名校
解题方法
7 . 某小组同学通过实验研究 溶液与铜粉发生的氧化还原反应。实验记录如下:
溶液与铜粉发生的氧化还原反应。实验记录如下:
下列说法不正确的是
 溶液与铜粉发生的氧化还原反应。实验记录如下:
溶液与铜粉发生的氧化还原反应。实验记录如下:序号 | Ⅰ | Ⅱ | Ⅲ |
实验步骤 |
|
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
A.实验Ⅰ、Ⅱ、Ⅲ中均涉及 被还原 被还原 |
| B.对比实验Ⅰ、Ⅱ说明白色沉淀的产生与铜粉的量有关 |
C.实验Ⅱ、Ⅲ中加入蒸馏水后 相同 相同 |
| D.向实验Ⅲ反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀 |
您最近一年使用:0次
名校
8 . 某校化学兴趣小组探究 与
与 溶液的反应。
溶液的反应。
资料:①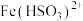 为红棕色,它可以将
为红棕色,它可以将 还原为
还原为 。
。
②生成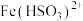 的反应为:
的反应为: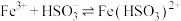 。
。
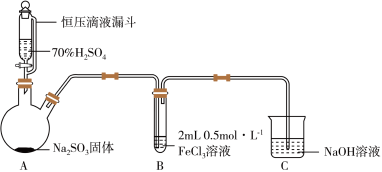
(1)实验室常用 硫酸与亚硫酸钠固体反应制备
硫酸与亚硫酸钠固体反应制备 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。在制备 的过程中,同学们发现,使用
的过程中,同学们发现,使用 的硫酸比用
的硫酸比用 的浓硫酸反应速率快,分析其中的原因是
的浓硫酸反应速率快,分析其中的原因是___________ 。
(2)该小组同学预测 与
与 溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式:
溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式:___________ 。
(3)向试管 中溶液通入
中溶液通入 至饱和,溶液变成红棕色,静置
至饱和,溶液变成红棕色,静置 后,溶液的颜色从红棕色慢慢变回黄色。静置
后,溶液的颜色从红棕色慢慢变回黄色。静置 后,溶液慢慢由黄色变为浅绿色。
后,溶液慢慢由黄色变为浅绿色。
①甲同学认为溶液变红的原因是通入 后,
后, 水解程度增大,形成
水解程度增大,形成 胶体。乙同学根据
胶体。乙同学根据 的性质否定了这一推论,原因是
的性质否定了这一推论,原因是___________ 。
②静置9小时后,溶液变浅绿色的离子反应方程式为___________ 。向反应后的溶液中滴加___________ (填试剂名称),产生蓝色沉淀,证明反应后的溶液中含有 。
。
③为了探究如何缩短溶液由红棕色变为浅绿色的时间,该小组同学进行了如下实验。
综合上述实验探究过程,得出的结论为:___________ 。
 与
与 溶液的反应。
溶液的反应。资料:①
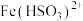 为红棕色,它可以将
为红棕色,它可以将 还原为
还原为 。
。②生成
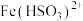 的反应为:
的反应为: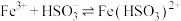 。
。
(1)实验室常用
 硫酸与亚硫酸钠固体反应制备
硫酸与亚硫酸钠固体反应制备 ,写出反应的化学方程式:
,写出反应的化学方程式: 的过程中,同学们发现,使用
的过程中,同学们发现,使用 的硫酸比用
的硫酸比用 的浓硫酸反应速率快,分析其中的原因是
的浓硫酸反应速率快,分析其中的原因是(2)该小组同学预测
 与
与 溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式:
溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式:(3)向试管
 中溶液通入
中溶液通入 至饱和,溶液变成红棕色,静置
至饱和,溶液变成红棕色,静置 后,溶液的颜色从红棕色慢慢变回黄色。静置
后,溶液的颜色从红棕色慢慢变回黄色。静置 后,溶液慢慢由黄色变为浅绿色。
后,溶液慢慢由黄色变为浅绿色。①甲同学认为溶液变红的原因是通入
 后,
后, 水解程度增大,形成
水解程度增大,形成 胶体。乙同学根据
胶体。乙同学根据 的性质否定了这一推论,原因是
的性质否定了这一推论,原因是②静置9小时后,溶液变浅绿色的离子反应方程式为
 。
。③为了探究如何缩短溶液由红棕色变为浅绿色的时间,该小组同学进行了如下实验。
| 实验I | 往 重新配制的 重新配制的 溶液中通入 溶液中通入 气体,溶液立即变为红棕色。微热 气体,溶液立即变为红棕色。微热 ,溶液颜色变为浅绿色。 ,溶液颜色变为浅绿色。 |
| 实验Ⅱ | 往5mL重新配制的 。溶液(用浓盐酸酸化)中通入 。溶液(用浓盐酸酸化)中通入 气体,溶液立即变为红棕色。几分钟后,溶液颜色变成浅绿色。 气体,溶液立即变为红棕色。几分钟后,溶液颜色变成浅绿色。 |
您最近一年使用:0次
名校
解题方法
9 . 某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置和下列步骤进行实验(加热装置和夹持装置均已略去,F是用于鼓入空气的双连打气球)。
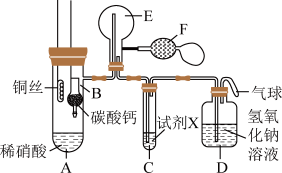
下列说法错误的是

| 实验操作(未排序) |
| ①将A装置中铜丝插入稀硝酸中,给A装置中的试管微微加热 |
| ②将仪器B下移,使碳酸钙与稀硝酸接触产生气体 |
| ③用F装置向E装置中鼓入空气 |
| ④当C装置中产生白色沉淀时,立刻将仪器B上提 |
| ⑤反应结束后,再将仪器B下移,使碳酸钙与稀硝酸接触产生气体 |
| A.试剂X可以是澄清的石灰水 |
| B.正确的实验操作顺序是:①②④③⑤ |
C.进行操作③后,C装置中白色沉淀溶解生成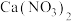 |
D.当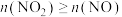 时,NO、 时,NO、 尾气可完全被氢氧化钠溶液吸收 尾气可完全被氢氧化钠溶液吸收 |
您最近一年使用:0次
10 . 下列实验操作、现象及得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向淀粉溶液中加适量20% 溶液,加热,冷却后加NaOH溶液至碱性,再滴加少量碘水 溶液,加热,冷却后加NaOH溶液至碱性,再滴加少量碘水 | 溶液未变蓝色 | 淀粉已完全水解 |
| B | 从装有过氧化钠的试剂瓶中取一定量固体于试管中然后加入 溶液 溶液 | 产生白色沉淀 | 过氧化钠变质产生 碳酸钠 |
| C | 镁在燃烧匙中点燃,迅速伸入盛满 的集气瓶中 的集气瓶中 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 |  具有氧化性 具有氧化性 |
| D | 将 溶液滴入酸性 溶液滴入酸性 溶液中 溶液中 | 紫红色褪去 |  有还原性 有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 溶液
溶液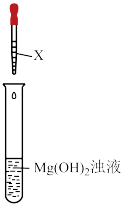
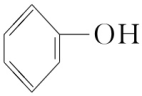 加入溴水中
加入溴水中