名校
解题方法
1 . 硫氰化钾(KSCN)在有机合成中具有重要应用,但会污染环境。预测浓硝酸能与KSCN反应以消除污染,现通过如下实验进行探究。
已知: 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
【实验一】
取2 mL浓硝酸于试管中,向其中滴加5滴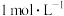 的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
(1)向浓硝酸中滴加KSCN溶液,溶液立即变红是因为生成了______ (填化学式)。KSCN中S元素的化合价为-2,预测剧烈反应后含硫产物可能是______ 。
【实验二】
将实验一放出的气体通入 和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
(2)该实验证实了红棕色气体中不含SO2,证据是______ ,白色沉淀为______ 。
【实验三】
(3)另取少量实验一最终所得溶液,______ (填操作和现象),证明溶液中含有 。
。
(4)经检验实验一放出的红棕色气体中含NO2,但NO2不一定是 的氧化产物,理由是
的氧化产物,理由是______ 。
【实验四】
(5)某同学向待测溶液中加入KSCN溶液,再加入浓硝酸,最终未得红色溶液,由此得出结论:待测液中不含 。
。
你认为该同学的结论是否正确:______ (填“是”或“否”),理由是______ 。
已知:
 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。【实验一】
取2 mL浓硝酸于试管中,向其中滴加5滴
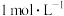 的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。(1)向浓硝酸中滴加KSCN溶液,溶液立即变红是因为生成了
【实验二】
将实验一放出的气体通入
 和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。(2)该实验证实了红棕色气体中不含SO2,证据是
【实验三】
(3)另取少量实验一最终所得溶液,
 。
。(4)经检验实验一放出的红棕色气体中含NO2,但NO2不一定是
 的氧化产物,理由是
的氧化产物,理由是【实验四】
(5)某同学向待测溶液中加入KSCN溶液,再加入浓硝酸,最终未得红色溶液,由此得出结论:待测液中不含
 。
。你认为该同学的结论是否正确:
您最近一年使用:0次
2024-02-04更新
|
162次组卷
|
2卷引用:福建省泉州市泉港区第一中学2023-2024学年高一下学期3月月考化学试题
名校
2 . 某小组分别进行如下3组实验研究 与
与 的反应,实验记录如下:
的反应,实验记录如下:
已知:水溶液中, 为白色沉淀,
为白色沉淀,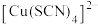 呈黄色。
呈黄色。 被称为“拟卤素”。
被称为“拟卤素”。
下列说法不正确的是
 与
与 的反应,实验记录如下:
的反应,实验记录如下:| 序号 | 实验 | 试剂 | 现象 |
| ① | 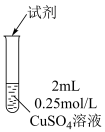 | 1滴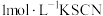 溶液 溶液 | 溶液迅速变绿,未见白色沉淀生成; 静置2小时后底部有少量白色沉淀 |
| ② | 先加入5滴 溶液,再加入1滴 溶液,再加入1滴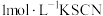 溶液 溶液 | 溶液变红,未见白色沉淀生成 | |
| ③ | 先加入5滴 溶液,再加入1滴 溶液,再加入1滴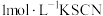 溶液 溶液 | 溶液变红,同时迅速生成白色沉淀,振荡后红色消失 |
 为白色沉淀,
为白色沉淀,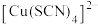 呈黄色。
呈黄色。 被称为“拟卤素”。
被称为“拟卤素”。下列说法不正确的是
A.①中生成白色沉淀的原因是: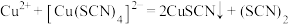 |
| B.由①可推知:①中生成配合物反应的反应速率大于氧化还原反应的 |
C.由②③可推知,结合 的能力: 的能力: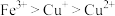 |
D.由①③可推知: 促进了 促进了 转化为 转化为 |
您最近一年使用:0次
2024-01-19更新
|
341次组卷
|
4卷引用:福建省泉州市永春一中、培元中学、石光中学、季延中学2023-2024学年高三下学期第二次联合考试化学试题
解题方法
3 . Ⅰ.探究NH3的某些性质,按如图装置进行实验(夹持仪器已略去):
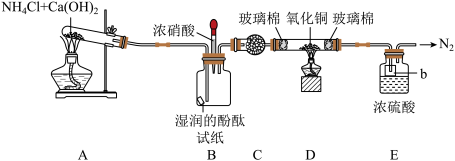
(1)装置连接后,先检查装置气密性,然后再开始实验。装置B中观察到的现象是湿润的酚酞试纸___________ ,挤压装置B中胶头滴管里的浓硝酸,有白烟产生,写出产生白烟的化学方程式 ___________ 。
(2)装置D中固体变红,若将D的CuO换成BaCu3O4,则与原来相比,产物多了Ba(OH)2,写出该反应的化学方程式为___________ 。
Ⅱ.探究一氧化氮能否被Na2O2完全吸收,设计了如图实验,装置如图二(加热装置省略):
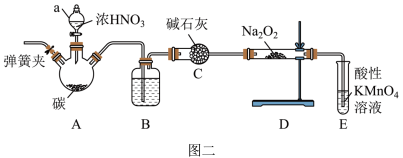
查阅资料所知:①2NO+Na2O2=NaNO2
②酸性条件下,NO或NO2都能与KMnO4溶液反应生成NO
(3)三颈烧瓶A中反应的化学方程式为___________ 。
(4)B瓶内装一种纯净物,该物质是___________ (写化学式)。
(5)C装置的作用是___________ 。
(6)若反应过程NO2被KMnO4吸收,还原产物为 Mn2+,则反应的离子方程式为___________ 。

(1)装置连接后,先检查装置气密性,然后再开始实验。装置B中观察到的现象是湿润的酚酞试纸
(2)装置D中固体变红,若将D的CuO换成BaCu3O4,则与原来相比,产物多了Ba(OH)2,写出该反应的化学方程式为
Ⅱ.探究一氧化氮能否被Na2O2完全吸收,设计了如图实验,装置如图二(加热装置省略):

查阅资料所知:①2NO+Na2O2=NaNO2
②酸性条件下,NO或NO2都能与KMnO4溶液反应生成NO

(3)三颈烧瓶A中反应的化学方程式为
(4)B瓶内装一种纯净物,该物质是
(5)C装置的作用是
(6)若反应过程NO2被KMnO4吸收,还原产物为 Mn2+,则反应的离子方程式为
您最近一年使用:0次
4 . 利用下图实验装置,探究 与
与 能否发生氧化还原反应。下列说法错误的是
能否发生氧化还原反应。下列说法错误的是
 与
与 能否发生氧化还原反应。下列说法错误的是
能否发生氧化还原反应。下列说法错误的是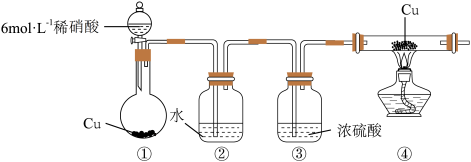
A.②中的水可除去 和硝酸蒸气 和硝酸蒸气 | B.当④中红棕色气体消失时,再点燃酒精灯 |
C.因反应生成 ,故无需尾气处理 ,故无需尾气处理 | D.④中红色固体变黑说明 能氧化 能氧化 |
您最近一年使用:0次
2023-07-06更新
|
714次组卷
|
3卷引用:福建省泉州市2022-2023 学年度高一下学期普通高中教学质量监测化学试题
福建省泉州市2022-2023 学年度高一下学期普通高中教学质量监测化学试题(已下线)专题02 氮及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题
真题
名校
5 . 某小组进行实验,向 蒸馏水中加入
蒸馏水中加入 ,充分振荡,溶液呈浅棕色,再加入
,充分振荡,溶液呈浅棕色,再加入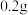 锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知
锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知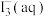 为棕色,下列关于颜色变化的解释错误的是
为棕色,下列关于颜色变化的解释错误的是
 蒸馏水中加入
蒸馏水中加入 ,充分振荡,溶液呈浅棕色,再加入
,充分振荡,溶液呈浅棕色,再加入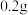 锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知
锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知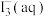 为棕色,下列关于颜色变化的解释错误的是
为棕色,下列关于颜色变化的解释错误的是| 选项 | 颜色变化 | 解释 |
| A | 溶液呈浅棕色 |  在水中溶解度较小 在水中溶解度较小 |
| B | 溶液颜色加深 | 发生了反应: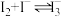 |
| C | 紫黑色晶体消失 |  ( ( )的消耗使溶解平衡 )的消耗使溶解平衡 右移 右移 |
| D | 溶液褪色 |  与有色物质发生了置换反应 与有色物质发生了置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-13更新
|
8516次组卷
|
19卷引用:福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题
福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题2023年高考辽宁卷化学真题(已下线)T13-实验方案的设计与评价(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 氯气和卤族元素(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷(已下线)第3讲 物质制备实验的设计与评价10-2023新东方高二上期中考化学中国人民大学附属中学2023-2024学年高三下学期化学练习6湖北省鄂东新领先协作体2023-2024学年高二下学期3月联考化学试题(已下线)FHgkyldyjhx10(已下线)测试辽宁化学 请勿下载2024年中国人民大学附属中学高三下学期高考化学模拟练习试卷(六)
名校
6 . 利用软锰矿 和浓盐酸制取纯净干燥氯气的装置如下:
和浓盐酸制取纯净干燥氯气的装置如下:

(1)装置A为___________ (填标号),发生反应的化学方程式为___________ 。
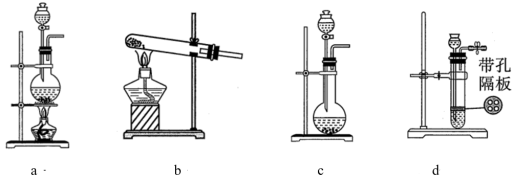
(2)装置E中盛放的试剂是___________ 溶液(填化学式)。
(3)某学习小组进行以下实验探究。
【实验任务】探究常温下饱和NaCl溶液抑制 溶解的原因。
溶解的原因。
【理论分析】存在反应: 反应1
反应1
【提出猜想】猜想a: 可抑制
可抑制 溶解。
溶解。
猜想b: 可抑制
可抑制 溶解。
溶解。
【实验验证】
实验1 测定 在不同浓度
在不同浓度 、HCl溶液中的溶解度
、HCl溶液中的溶解度
实验ⅰ的结果符合猜想a,实验ⅱ的结果说明还有其他因素会影响 在水中的溶解度。
在水中的溶解度。
【交流讨论】查阅资料: 反应2
反应2
①饱和氯水中 ,
, ,
,
___________ ,此时 的溶解主要受反应1影响。
的溶解主要受反应1影响。
②在HCl溶液中, 时,
时, 对
对 溶解起
溶解起___________ (填“促进”或“抑制”)作用; 时,随着
时,随着 浓度增大,
浓度增大, 溶解度增大的原因是
溶解度增大的原因是___________ 。
实验2 测定 在不同浓度NaCl溶液中的溶解度
在不同浓度NaCl溶液中的溶解度
③综合以上数据,对 溶解的抑制效果:
溶解的抑制效果:
___________  (填“>”或“<”),证据是
(填“>”或“<”),证据是___________ 。
【实验结论】
④常温下饱和NaCl溶液抑制 溶解的原因是
溶解的原因是___________ 。
 和浓盐酸制取纯净干燥氯气的装置如下:
和浓盐酸制取纯净干燥氯气的装置如下:
(1)装置A为

(2)装置E中盛放的试剂是
(3)某学习小组进行以下实验探究。
【实验任务】探究常温下饱和NaCl溶液抑制
 溶解的原因。
溶解的原因。【理论分析】存在反应:
 反应1
反应1【提出猜想】猜想a:
 可抑制
可抑制 溶解。
溶解。猜想b:
 可抑制
可抑制 溶解。
溶解。【实验验证】
实验1 测定
 在不同浓度
在不同浓度 、HCl溶液中的溶解度
、HCl溶液中的溶解度| 实验 | 浓度/mol/L 溶解度/mol/L 物质 | 0.1 | 0.2 | 0.5 | 1.0 | 3.0 | 5.0 |
| ⅰ |  | - | - | 0.0627 | 0.0568 | 0.0435 | 0.0407 |
| ⅱ | HCl | 0.0634 | 0.0619 | 0.0630 | 0.0665 | 0.0824 | 0.1004 |
 在水中的溶解度。
在水中的溶解度。【交流讨论】查阅资料:
 反应2
反应2①饱和氯水中
 ,
, ,
,
 的溶解主要受反应1影响。
的溶解主要受反应1影响。②在HCl溶液中,
 时,
时, 对
对 溶解起
溶解起 时,随着
时,随着 浓度增大,
浓度增大, 溶解度增大的原因是
溶解度增大的原因是实验2 测定
 在不同浓度NaCl溶液中的溶解度
在不同浓度NaCl溶液中的溶解度NaCl浓度 | 0.5 | 1.0 | 3.0 | 5.0 |
 溶解度 溶解度 | 0.0658 | 0.0580 | 0.0416 | 0.0360 |
 溶解的抑制效果:
溶解的抑制效果:
 (填“>”或“<”),证据是
(填“>”或“<”),证据是【实验结论】
④常温下饱和NaCl溶液抑制
 溶解的原因是
溶解的原因是
您最近一年使用:0次
2023-05-13更新
|
373次组卷
|
2卷引用:福建省厦门市2023届高三下学期第四次质量检测化学试题
名校
解题方法
7 . 探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通
时的硝酸浓度。如图所示,先通 一段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至
一段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至 ,取
,取 ,用
,用 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是
(忽略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是
 时的硝酸浓度。如图所示,先通
时的硝酸浓度。如图所示,先通 一段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至
一段时间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至 ,取
,取 ,用
,用 的
的 溶液滴定至终点时消耗
溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是
(忽略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是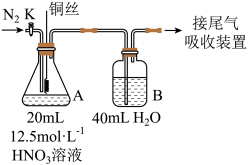
A.可用盛有 溶液的洗气瓶进行尾气吸收 溶液的洗气瓶进行尾气吸收 |
B.铜与硝酸反应主要生成 时的硝酸浓度不大于 时的硝酸浓度不大于 |
C.若不通 ,可能导致所得实验结果偏高 ,可能导致所得实验结果偏高 |
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果偏低 的干扰)进行求算,所得实验结果偏低 |
您最近一年使用:0次
2023-04-29更新
|
1071次组卷
|
4卷引用:福建省厦门第一中学2024届高三上学期10 月月考化学试题
福建省厦门第一中学2024届高三上学期10 月月考化学试题山东省淄博市部分学校2023届高三下学期二模化学试题(已下线)第7讲 金属材料和金属矿物利用(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
8 . Mg与水反应时,Mg表面会覆盖致密的 导致反应较缓慢。某兴趣小组为了验证部分离子对Mg与水反应的影响,进行了如下实验。
导致反应较缓慢。某兴趣小组为了验证部分离子对Mg与水反应的影响,进行了如下实验。
I.验证 和
和 对Mg与水反应的促进作用
对Mg与水反应的促进作用
(1)某同学认为根据上表能够说明 对Mg与水的反应起促进作用,他的理由是
对Mg与水的反应起促进作用,他的理由是__________ 。
(2)实验b、d镁条表面附着固体中还检验出碱式碳酸镁 ,写出Mg与
,写出Mg与 溶液反应生成该固体的离子方程式:
溶液反应生成该固体的离子方程式:________________ 。
(3)综合实验a~d可以得出结论: 和
和 都能与
都能与 作用而加快Mg与水的反应,
作用而加快Mg与水的反应,________________________________ (补充两点)。
II.室温下,探究 对Mg与水反应的影响
对Mg与水反应的影响
该小组用Mg与NaCl溶液反应,实验发现当 浓度过低或过高时,反应速率没有变化,当
浓度过低或过高时,反应速率没有变化,当 浓度为2 mol·L
浓度为2 mol·L 时,Mg与水反应较快,产生大量的气泡,同时生成白色固体,最终溶液pH约为10.98。
时,Mg与水反应较快,产生大量的气泡,同时生成白色固体,最终溶液pH约为10.98。
(4)经检验该白色固体含有碱式氯化镁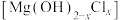 。碱式氯化镁受热(>100℃)易分解生成氧化镁和两种气体,写出其分解的化学方程式:
。碱式氯化镁受热(>100℃)易分解生成氧化镁和两种气体,写出其分解的化学方程式:__________________________ 。实验室检验镁条表面生成的白色固体含有碱式氯化镁的操作是__________________ 。
(5)常温下,饱和 溶液的
溶液的
______ ,试从化学平衡角度分析实验得到最终溶液的pH大于该值的原因:___________ (已知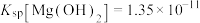 ,
,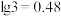 )。
)。
 导致反应较缓慢。某兴趣小组为了验证部分离子对Mg与水反应的影响,进行了如下实验。
导致反应较缓慢。某兴趣小组为了验证部分离子对Mg与水反应的影响,进行了如下实验。I.验证
 和
和 对Mg与水反应的促进作用
对Mg与水反应的促进作用| 实验序号 | a | b | c | d |
0.1 mol·L 盐溶液 盐溶液 |  |  | NaCl |  |
| 30 min内产生气体的体积/mL | 1.5 | 0.7 | <0.1 | 1.4 |
| 气体的主要成分 |  | |||
| 30 min时镁条表面情况 | 大量固体附着(固体可溶于盐酸) | |||
 对Mg与水的反应起促进作用,他的理由是
对Mg与水的反应起促进作用,他的理由是(2)实验b、d镁条表面附着固体中还检验出碱式碳酸镁
 ,写出Mg与
,写出Mg与 溶液反应生成该固体的离子方程式:
溶液反应生成该固体的离子方程式:(3)综合实验a~d可以得出结论:
 和
和 都能与
都能与 作用而加快Mg与水的反应,
作用而加快Mg与水的反应,II.室温下,探究
 对Mg与水反应的影响
对Mg与水反应的影响该小组用Mg与NaCl溶液反应,实验发现当
 浓度过低或过高时,反应速率没有变化,当
浓度过低或过高时,反应速率没有变化,当 浓度为2 mol·L
浓度为2 mol·L 时,Mg与水反应较快,产生大量的气泡,同时生成白色固体,最终溶液pH约为10.98。
时,Mg与水反应较快,产生大量的气泡,同时生成白色固体,最终溶液pH约为10.98。(4)经检验该白色固体含有碱式氯化镁
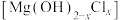 。碱式氯化镁受热(>100℃)易分解生成氧化镁和两种气体,写出其分解的化学方程式:
。碱式氯化镁受热(>100℃)易分解生成氧化镁和两种气体,写出其分解的化学方程式:(5)常温下,饱和
 溶液的
溶液的
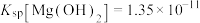 ,
,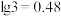 )。
)。
您最近一年使用:0次
2023-02-16更新
|
617次组卷
|
5卷引用:T12-实验综合题



