名校
1 .  为白色微溶物,常温下某小组对
为白色微溶物,常温下某小组对 和
和 的反应进行如下探究实验,测得
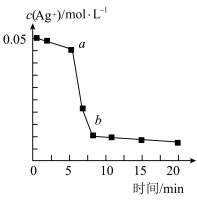
的反应进行如下探究实验,测得 随时间变化如图,实验过程中测得温度几乎无变化,下列说法正确的是
随时间变化如图,实验过程中测得温度几乎无变化,下列说法正确的是
 为白色微溶物,常温下某小组对
为白色微溶物,常温下某小组对 和
和 的反应进行如下探究实验,测得
的反应进行如下探究实验,测得 随时间变化如图,实验过程中测得温度几乎无变化,下列说法正确的是
随时间变化如图,实验过程中测得温度几乎无变化,下列说法正确的是| 实验 | 操作 | 现象 |
| Ⅰ | 向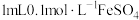 溶液中,加入 溶液中,加入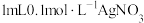 溶液 溶液 | 几分钟后,出现大量灰黑色浑浊 |
| Ⅱ | 先向试管中加入几滴 溶液,然后重复实验Ⅰ的操作 溶液,然后重复实验Ⅰ的操作 | 现象与实验Ⅰ相同 |
A.实验Ⅰ只发生反应: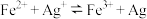 ,灰黑色浑浊是单质Ag ,灰黑色浑浊是单质Ag |
B.图中 由a→b急速变化的可能原因是生成的Ag起催化作用 由a→b急速变化的可能原因是生成的Ag起催化作用 |
C.图中 由a→b急速变化的可能原因是反应放热 由a→b急速变化的可能原因是反应放热 |
D.图中 由a→b急速变化的可能原因是生成的 由a→b急速变化的可能原因是生成的 起催化作用 起催化作用 |
您最近一年使用:0次
2023-04-29更新
|
345次组卷
|
6卷引用:福建省厦门第一中学2022-2023学年高一下学期期中考试化学试题
福建省厦门第一中学2022-2023学年高一下学期期中考试化学试题福建省福州市六校联考2022-2023学年高一下学期期末考试化学试题(已下线)专题03 化学反应的速率与限度-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)福建省三明市第一中学2023-2024学年高一下学期期中考试化学试题(选考)福建省泉州市第七中学2023-2024学年高一下学期5月期中考试化学试题
名校
解题方法
2 . 利用如图微型实验装置制取H2S和SO2,并探究硫元素之间的转化。实验时挤压胶头滴管使硫酸滴到药匙中,然后倾斜试管使硫酸滴到药匙外与FeS反应。下列说法错误的是
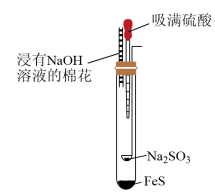

| A.实验开始一段时间后,试管内壁上有黄色颗粒出现 |
| B.玻璃导气管中塞有蘸NaOH棉花的目的是吸收尾气 |
| C.实验过程中发生的反应均可用离子方程式表示 |
D.生成SO2的离子反应为SO +2H+=SO2↑+H2O +2H+=SO2↑+H2O |
您最近一年使用:0次
2023-04-28更新
|
209次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高一下学期4月期中考试化学试题
名校
3 . 实验的方法常用于研究有机化合物的结构及性质。
(1)依据下列有机物回答问题:
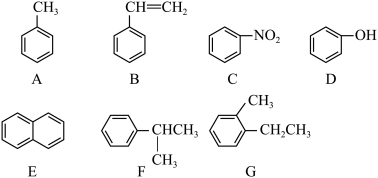
①属于芳香烃的是_________ 。
②从官能团分类的角度判断D属于_________ 类物质。
③互为同系物的是_________ 。
④F的一氯代物有_________ 种。
⑤互为同分异构体的是_________ 。
(2)如图是制备和研究乙炔性质的实验装置图。
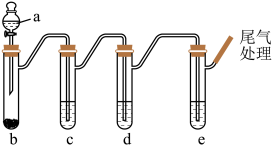
①仪器a的名称为_________ 。
②b中发生反应的化学方程式是_________ 。
③c中盛放的 溶液的作用是
溶液的作用是_________ 。
④d中溴的四氯化碳溶液褪色,生成物的结构简式是_________ 。
⑤e中溶液检验乙炔的还原性,则盛放试剂为_________ 。
⑥若在空气中点燃乙炔,可观察到的实验现象是_________ 。
(1)依据下列有机物回答问题:

①属于芳香烃的是
②从官能团分类的角度判断D属于
③互为同系物的是
④F的一氯代物有
⑤互为同分异构体的是
(2)如图是制备和研究乙炔性质的实验装置图。

①仪器a的名称为
②b中发生反应的化学方程式是
③c中盛放的
 溶液的作用是
溶液的作用是④d中溴的四氯化碳溶液褪色,生成物的结构简式是
⑤e中溶液检验乙炔的还原性,则盛放试剂为
⑥若在空气中点燃乙炔,可观察到的实验现象是
您最近一年使用:0次
名校
解题方法
4 . 某实验小组利用微型实验装置进行氯气的制备和性质探究,装置如图所示,下列有关说法错误的是
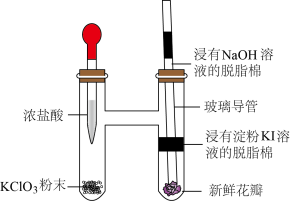
A. 与浓盐酸反应,HCl只体现还原性 与浓盐酸反应,HCl只体现还原性 |
B.浸有淀粉KI溶液的脱脂棉变蓝,说明氧化性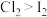 |
| C.新鲜花瓣褪色是因为氯气与水反应生成的HClO有漂白性 |
| D.浸有NaOH溶液的脱脂棉可吸收过量氯气 |
您最近一年使用:0次
2023-04-27更新
|
707次组卷
|
3卷引用:广东省大湾区2023届普通高中毕业班下学期联合模拟考试(二)化学试题
名校
解题方法
5 . 一定温度下,探究铜与稀硝酸的反应,反应过程如图,下列说法不正确的是
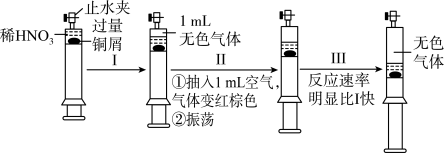

A.过程Ⅰ中生成气体的离子方程式为3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
| B.当活塞不再移动时,再抽入空气,金属铜屑继续溶解 |
| C.①中产生的现象可以用来检验该无色气体 |
| D.过程Ⅲ反应速率比过程Ⅰ快的原因是反应物浓度增大 |
您最近一年使用:0次
解题方法
6 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图所示的实验。下列说法正确的是


| A.装置A中粉末不变色 |
| B.装置B中溶液褪色 |
| C.装置C用于检验CO2 |
| D.装置D用于吸收尾气 |
您最近一年使用:0次
7 . 氯气、氯水、漂白粉都是常见的含氯消毒剂。回答下列有关问题。
Ⅰ.实验室中制备
方法一: 与浓盐酸反应
与浓盐酸反应
方法二:漂白粉与浓盐酸反应,原理为
(1)方法一的化学反应方程式为____________ ,发生装置为______ (填编号)。

(2)当制得相同质量 时,方法一与方法二转移的电子数之比为
时,方法一与方法二转移的电子数之比为______ 。
Ⅱ.某实验小组利用如图装置制备氯水,并探究其部分性质。
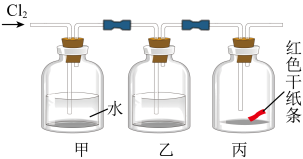
(3)若实验过程中观察到红色干纸条未褪色,则乙中的试剂可能是______ (填编号)。
A.浓 B.饱和NaCl溶液 C.NaOH溶液
B.饱和NaCl溶液 C.NaOH溶液
(4)将装置甲中所得氯水滴入含有酚酞的NaOH稀溶液中,观察到溶液红色褪去。有同学提出如下两种原因:
【原因1】氯水中含有的 中和掉NaOH而使溶液褪色
中和掉NaOH而使溶液褪色
【原因2】氯水中含有的______ 具有漂白性而使溶液褪色
请设计实验验证:褪色的原因确实存在“原因2”。向褪色后的溶液中滴加______ (填试剂与现象)。
Ⅰ.实验室中制备

方法一:
 与浓盐酸反应
与浓盐酸反应方法二:漂白粉与浓盐酸反应,原理为

(1)方法一的化学反应方程式为

(2)当制得相同质量
 时,方法一与方法二转移的电子数之比为
时,方法一与方法二转移的电子数之比为Ⅱ.某实验小组利用如图装置制备氯水,并探究其部分性质。

(3)若实验过程中观察到红色干纸条未褪色,则乙中的试剂可能是
A.浓
 B.饱和NaCl溶液 C.NaOH溶液
B.饱和NaCl溶液 C.NaOH溶液(4)将装置甲中所得氯水滴入含有酚酞的NaOH稀溶液中,观察到溶液红色褪去。有同学提出如下两种原因:
【原因1】氯水中含有的
 中和掉NaOH而使溶液褪色
中和掉NaOH而使溶液褪色【原因2】氯水中含有的
请设计实验验证:褪色的原因确实存在“原因2”。向褪色后的溶液中滴加
您最近一年使用:0次
8 . 某小组探究 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。
已知:ⅰ. 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;
ⅲ. 可与
可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是________________________ 。
(2) 与KI反应的离子方程式为
与KI反应的离子方程式为________________________ 。
为了研究 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
(3)实验2-1不能用于测定 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有____________ 。
(4)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与
先与 反应,使
反应,使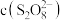 降低;
降低;
猜想2: 先与KI反应,
先与KI反应, ,
,
①甲同学提出猜想1的依据:由信息ⅲ推测, 的还原性
的还原性______ (填“强于”或“弱于”)KI的。
②乙同学根据现有数据证明猜想1不成立,理由是__________________ 。
③补全猜想2:________________________________________________ 。
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率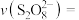
____________  (写出计算式)。
(写出计算式)。
(6)实验2-2中,30s内未检测到 与
与 反应,可能原因是
反应,可能原因是______ 。(写出2条)。
 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。已知:ⅰ.
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;ⅲ.
 可与
可与 发生反应:
发生反应: 。
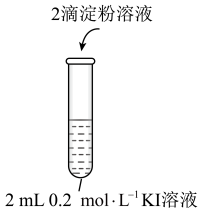
。编号 | 1-1 | 1-2 |
实验操作 |
|
|
现象 | 无明显现象 | 溶液立即变蓝 |
(2)
 与KI反应的离子方程式为
与KI反应的离子方程式为为了研究
 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
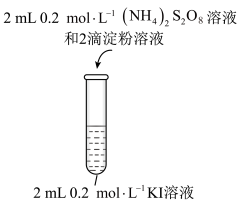
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。编号 |
|
| 蒸馏水/mL | 0.4%的淀粉溶液/滴 |
| 变色时间/s |
2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有(4)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。猜想1:
 先与
先与 反应,使
反应,使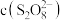 降低;
降低;猜想2:
 先与KI反应,
先与KI反应, ,
,①甲同学提出猜想1的依据:由信息ⅲ推测,
 的还原性
的还原性②乙同学根据现有数据证明猜想1不成立,理由是
③补全猜想2:
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率
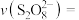
 (写出计算式)。
(写出计算式)。(6)实验2-2中,30s内未检测到
 与
与 反应,可能原因是
反应,可能原因是
您最近一年使用:0次
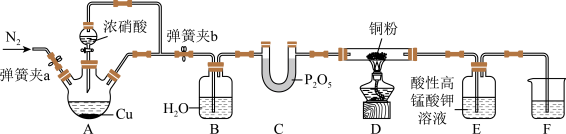
9 . 过多的NOx排放,往往会产生污染。某研究性小组探究 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
已知: 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。
(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:将F中的长导管插入液面以下→_______→_______→_______→_______→_______ (操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)装置B的作用_______ 。
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式_______ 。
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为_______ ;
(5)实验前和实验结束时,都需通一段时间的 ,目的分别是
,目的分别是_______ 、_______ 。
(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行 的是_______。
 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
已知:
 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:将F中的长导管插入液面以下→_______→_______→_______→_______→____
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)装置B的作用
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为
(5)实验前和实验结束时,都需通一段时间的
 ,目的分别是
,目的分别是(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中
| A.加热该绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
您最近一年使用:0次
名校
解题方法
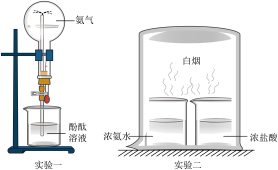
10 . 如图所示是 的两个性质探究实验,下列有关说法中正确的是
的两个性质探究实验,下列有关说法中正确的是
 的两个性质探究实验,下列有关说法中正确的是
的两个性质探究实验,下列有关说法中正确的是
| A.两个实验均只表现氨气的化学性质 | B.两个实验均表现了 易挥发的性质 易挥发的性质 |
C.两个实验均可说明 是碱性气体 是碱性气体 | D.两个实验均可说明 是还原性气体 是还原性气体 |
您最近一年使用:0次
2023-04-20更新
|
184次组卷
|
3卷引用:江西省抚州市七校2022-2023学年高一下学期期中考试化学试题
江西省抚州市七校2022-2023学年高一下学期期中考试化学试题(已下线)第17讲 氨的转化与生成-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)江西省南丰县第一中学 黎川一中 宜黄一中 南城二中 金溪一中 广昌一中 乐安县实验学校2022-2023学年高一下学期期中联考化学试卷

 KI溶液/mL
KI溶液/mL


