1 . Ⅰ.由三种元素组成的固体化合物A,按如下流程进行实验。已知气体C为纯净物,气体E能使湿润的红色石蕊试纸变蓝。
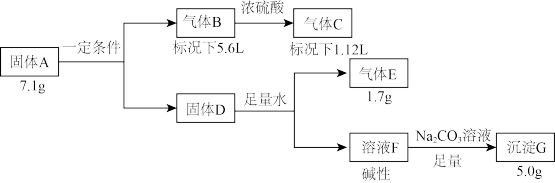
请回答:
(1)组成A的三种元素是N和____ (填元素符号),A的化学式是____ 。
(2)固体D与足量水反应的离子方程式是____ 。
(3)将气体E通入SCl2的热溶液中可制得S4N4,同时生成一种常见的盐和一种淡黄色单质,该反应的化学方程式是____ 。
II. 某实验小组用下图装置进行铜和浓硫酸反应的实验。
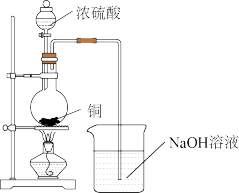
请回答:
(1)上述装置有一处不合理,请从安全角度提出改进方案____ 。
(2)实验中观察到有白色固体生成,请设计实验方案检验该白色固体成分____ 。

请回答:
(1)组成A的三种元素是N和
(2)固体D与足量水反应的离子方程式是
(3)将气体E通入SCl2的热溶液中可制得S4N4,同时生成一种常见的盐和一种淡黄色单质,该反应的化学方程式是
II. 某实验小组用下图装置进行铜和浓硫酸反应的实验。

请回答:
(1)上述装置有一处不合理,请从安全角度提出改进方案
(2)实验中观察到有白色固体生成,请设计实验方案检验该白色固体成分
您最近一年使用:0次
2020-12-09更新
|
1454次组卷
|
4卷引用:浙江省嘉兴市2021届高三12月教学测试化学试题
浙江省嘉兴市2021届高三12月教学测试化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题(已下线)2021年6月浙江高考化学试题变式题26-31(已下线)2022年浙江省6月高考真题变式题26-31
2 . Ⅰ.电镀废水中常含有阴离子A,排放前可加CuSO4溶液处理,使之转化为沉淀B,按如图流程进行实验。
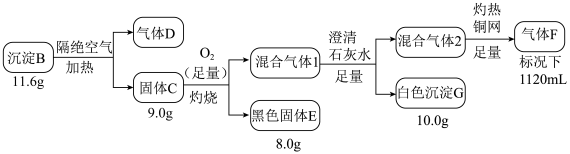
已知:B含三种元素;气体D标况下密度2.32g/L;混合气体l无色无味;气体F标况下密度为1.25g/L。请回答:
(1)组成B的三种元素是_______ ,气体D的分子式是______ 。
(2)写出固体C在足量氧气中灼烧的方程式_______ 。
(3)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为199),则反应的化学方程式是________ 。
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,打开弹簧夹,向盛有NaBr溶液的试管B和分液漏斗C中同时通入少量Cl2,将少量分液漏斗C中溶液滴入试管D中,取试管D振荡,静止后观察现象。实验装置如图:
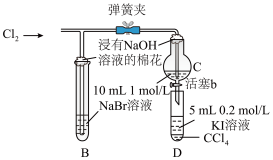
(4)说明氧化性 Br2>I2的实验现象是________ 。
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗C中通入Cl2 未过量。试设计简单实验方案检验_________ 。

已知:B含三种元素;气体D标况下密度2.32g/L;混合气体l无色无味;气体F标况下密度为1.25g/L。请回答:
(1)组成B的三种元素是
(2)写出固体C在足量氧气中灼烧的方程式
(3)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为199),则反应的化学方程式是
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,打开弹簧夹,向盛有NaBr溶液的试管B和分液漏斗C中同时通入少量Cl2,将少量分液漏斗C中溶液滴入试管D中,取试管D振荡,静止后观察现象。实验装置如图:

(4)说明氧化性 Br2>I2的实验现象是
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗C中通入Cl2 未过量。试设计简单实验方案检验
您最近一年使用:0次
3 . 草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:
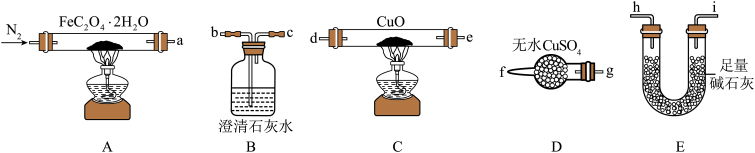
①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→___ →尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2,其目的为__ 。
③实验证明了气体产物中含有CO,依据的实验现象为__ 。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是__ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为__ 。
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为__ 。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为__ ;步骤3中加入锌粉的目的为___ 。
(5)若步骤 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将__ (填“偏高”、“偏低”或“不变”)
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:

①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→
②检查装置气密性后,先通入一段时间N2,其目的为
③实验证明了气体产物中含有CO,依据的实验现象为
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为
(5)若步骤
 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
2020-06-12更新
|
1222次组卷
|
3卷引用:吉林省延边州2020届高三4月教学质量检测理科综合化学试题
4 . 草酸是草本植物常具有的成分。查阅相关资料得到草酸晶体(H2C2O4·3H2O)及其盐的性质如表。
(1)草酸晶体(H2C2O4·3H2O)175℃以上会发生分解生成三种氧化物,某实验小组欲通过实验证明这三种氧化物。
①该小组选用装置丙作为分解装置,不选用甲装置的原因是_______ 。丙装置相对于乙装置的优点是________ 。实验前检验该装置气密性的操作方法是________ 。
甲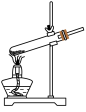 乙
乙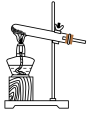 丙
丙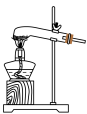
②从图中选用合适的装置,验证分解产生的气体,装置的连接顺序是______________ 。(用装置编号表示,某些装置可以重复使用,也可以装不同的试剂)
B C
C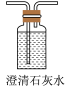 D
D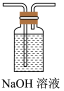 E
E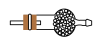 F
F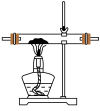
③B装置的作用是__________ 。
(2)某实验小组称取4.0g粗草酸晶体配成100mL溶液,采用0.1mol·L-1酸性高锰酸钾溶液滴定该草酸溶液,测定该草酸晶体的纯度。
①配制草酸溶液需要用到的主要玻璃仪器有_______________ 。
②本实验达到滴定终点的标志是___________ 。
③将所配草酸分为四等份,实验测得每份平均消耗酸性高锰酸钾溶液20mL。计算该粗草酸中含草酸晶体的质量为_______ g(保留两位有效数字)。
| 熔沸点 | 颜色与溶解性 | 部分化学性质 | 盐 |
| 熔点:101-102℃ 沸点:150-160℃升华 | 草酸晶体无色,易溶于水 | 100.1℃受热脱水,175℃以上分解成气体;具有还原性 | 草酸钙盐难溶于水 |
①该小组选用装置丙作为分解装置,不选用甲装置的原因是
甲
 乙
乙 丙
丙
②从图中选用合适的装置,验证分解产生的气体,装置的连接顺序是
B
 C
C D
D E
E F
F
③B装置的作用是
(2)某实验小组称取4.0g粗草酸晶体配成100mL溶液,采用0.1mol·L-1酸性高锰酸钾溶液滴定该草酸溶液,测定该草酸晶体的纯度。
①配制草酸溶液需要用到的主要玻璃仪器有
②本实验达到滴定终点的标志是
③将所配草酸分为四等份,实验测得每份平均消耗酸性高锰酸钾溶液20mL。计算该粗草酸中含草酸晶体的质量为
您最近一年使用:0次
名校
解题方法
5 . 草酸是一种常用的还原剂,某校高三化学小组探究草酸被氧化的速率问题。
(1)H2C2O4是二元弱酸,写出H2C2O4溶于水的电离方程式:___________ 。
(2)实验Ⅰ试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为__________ 。
(3)瑛瑛和超超查阅资料,实验Ⅰ试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
实验Ⅳ的目的是:_______________ 。
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72-浓度变化如图:
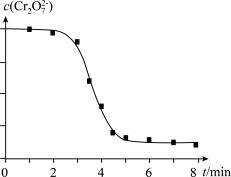
臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i:MnO2与H2C2O4反应生成了Mn2+。
过程ii:___________ 。
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001mol MnO2加入到6mL______ 中,固体完全溶解;从中取出少量溶液,加入过量PbO2固体,充分反应后静置,观察到________________ 。
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案如下:将2mL、0.3mol/LH2C2O4溶液与4mL0.01mol/LK2Cr2O7溶液混合,调至pH=2,加入0.0001molMnSO4固体,6分钟后现象为:______________
(5)综合以上实验可知,草酸发生氧化反应的速率与____________ 有关。
| 实验Ⅰ | 试剂 | 混合后 溶液pH | 现象 (1 h后溶液) | ||
| 试管 | 滴管 | ||||
 | a | 4mL0.01mol•L-1KMnO4溶液,几滴浓H2SO4 | 2 mL0.3mol•L-1 H2C2O4溶液 | 2 | 褪为无色 |
| b | 4mL0.01mol•L-1KMnO4溶液,几滴浓NaOH | 7 | 无明显变化 | ||
| c | 4mL0.01mol•L-1K2Cr2O7溶液,几滴浓H2SO4 | 2 | 无明显变化 | ||
| d | 4mL0.01mol•L-1K2Cr2O7溶液,几滴浓NaOH | 7 | 无明显变化 | ||
(2)实验Ⅰ试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为
(3)瑛瑛和超超查阅资料,实验Ⅰ试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
| 实验Ⅱ | 实验Ⅲ | 实验Ⅳ | |
| 实验 操作 | 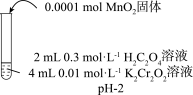 |  |  |
| 实验 现象 | 6 min后固体完全溶解,溶液橙色变浅,温度不变 | 6 min后固体未溶解,溶液颜色无明显变化 | 6 min后固体未溶解,溶液颜色无明显变化 |
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72-浓度变化如图:

臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i:MnO2与H2C2O4反应生成了Mn2+。
过程ii:
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001mol MnO2加入到6mL
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案如下:将2mL、0.3mol/LH2C2O4溶液与4mL0.01mol/LK2Cr2O7溶液混合,调至pH=2,加入0.0001molMnSO4固体,6分钟后现象为:
(5)综合以上实验可知,草酸发生氧化反应的速率与
您最近一年使用:0次
6 . 碳酸亚铁可用于制备补血剂。某研究小组制备了FeCO3,并对FeCO3的性质和应用进行了探究。
已知:①FeCO3是白色固体,难溶于水
②Fe2++6SCN- Fe(SCN)64-(无色)
Fe(SCN)64-(无色)
Ⅰ.FeCO3的制取(夹持装置略)
实验i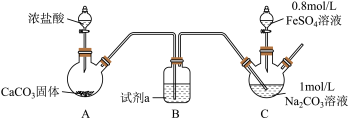
装置C中,向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a是__ 。
(2)向Na2CO3溶液通入CO2的目的是__ 。
(3)C装置中制取FeCO3的离子方程式为__ 。
(4)有同学认为C中出现白色沉淀之后应继续通CO2,你认为是否合理并说明理由__ 。
Ⅱ.FeCO3的性质探究
实验ii
实验iii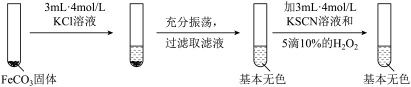
(5)对比实验ⅱ和ⅲ,得出的实验结论是__ 。
(6)依据实验ⅱ的现象,写出加入10%H2O2溶液的离子方程式__ 。
Ⅲ.FeCO3的应用
(7)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,此反应的离子方程式为__ 。该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是__ (不考虑操作不当引起的误差)。
已知:①FeCO3是白色固体,难溶于水
②Fe2++6SCN-
 Fe(SCN)64-(无色)
Fe(SCN)64-(无色)Ⅰ.FeCO3的制取(夹持装置略)
实验i

装置C中,向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a是
(2)向Na2CO3溶液通入CO2的目的是
(3)C装置中制取FeCO3的离子方程式为
(4)有同学认为C中出现白色沉淀之后应继续通CO2,你认为是否合理并说明理由
Ⅱ.FeCO3的性质探究
实验ii

实验iii

(5)对比实验ⅱ和ⅲ,得出的实验结论是
(6)依据实验ⅱ的现象,写出加入10%H2O2溶液的离子方程式
Ⅲ.FeCO3的应用
(7)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,此反应的离子方程式为
您最近一年使用:0次
7 . 某化学小组用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
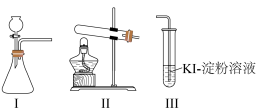
供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
(2)丙实验中O2与KI溶液反应的离子方程式为___________________________________ 。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是__________ 。为进一步探究该条件对反应速率的影响,可采取的实验措施是____________________________ 。
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入_________ (填字母)溶液中,依据实验现象来证明白雾中含有H2O2。
A.酸性KMnO4B.FeCl2C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应___________________________________ (写离子方程式)造成的,请设计实验证明他们的猜想是否正确:___________________________________ 。

供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
| 操作 | 现象 | |
| 甲 | 向装置I的锥形瓶中加入MnO2固体,向装置I的 | 装置I中产生无色气体并伴随大量白雾;装置Ⅲ中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向装置Ⅱ中加入KMnO4固体,连接装置Ⅱ、Ⅲ,点燃酒精灯 | 装置Ⅲ中有气泡冒出,溶液不变蓝 |
| 丙 | 向装置Ⅱ中加入 | 装置Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式为
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入
A.酸性KMnO4B.FeCl2C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应
您最近一年使用:0次
2019-12-25更新
|
548次组卷
|
2卷引用:安徽省示范高中2019-2020学年高二上学期第二次考试化学试题
名校
解题方法
8 . 某化学实验小组将装有铜与浓硫酸烧瓶加热一段时间后,取出烧瓶中固体,探究其成分。查资料可知,浓硫酸与铜反应可能生成CuS或Cu2S,它们都难溶于水,能溶于稀硝酸。实验如下:
(i)用蒸馏水洗涤固体,得到蓝色溶液,固体呈黑色。
(ii)取少量黑色固体于试管中,加入适量稀硝酸,黑色固体逐渐溶解,溶液变为蓝色,产生无色气泡。取少量上层清液于试管,滴加氯化钡溶液,产生白色沉淀。
①根据实验(i)得到蓝色溶液可知,固体中含____________ (填化学式)
②根据实验(ii)的现象_______ (填“能”或“不能”)确定黑色固体是CuS还是Cu2S,理由是__________________________________________________________________________ 。
写出Cu2S与稀硝酸反应的化学方程式____________________________________________
③为了进一步探究黑色固体的成分,将实验(i)中黑色固体洗涤、烘干,再称取48.0g黑色固体进行如下实验,通入足量O2,使硬质玻璃管中黑色固体充分反应,观察到F瓶中品红溶液褪色。
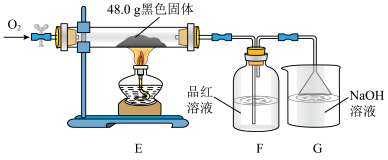
根据上表实验数据推测:实验I中黑色固体的化学式为_____________________________ ;实验Ⅱ中黑色固体的成分及质量为_______________________________________________ 。
(i)用蒸馏水洗涤固体,得到蓝色溶液,固体呈黑色。
(ii)取少量黑色固体于试管中,加入适量稀硝酸,黑色固体逐渐溶解,溶液变为蓝色,产生无色气泡。取少量上层清液于试管,滴加氯化钡溶液,产生白色沉淀。
①根据实验(i)得到蓝色溶液可知,固体中含
②根据实验(ii)的现象
写出Cu2S与稀硝酸反应的化学方程式
③为了进一步探究黑色固体的成分,将实验(i)中黑色固体洗涤、烘干,再称取48.0g黑色固体进行如下实验,通入足量O2,使硬质玻璃管中黑色固体充分反应,观察到F瓶中品红溶液褪色。

| 实验序号 | 反应前黑色固体质量/g | 充分反应后黑色固体质量/g |
| I | 48.0 | 48.0 |
| Ⅱ | 48.0 | 44.0 |
| Ⅲ | 48.0 | 40.0 |
您最近一年使用:0次
2019-07-05更新
|
657次组卷
|
3卷引用:湖南省湘东六校2018-2019学年高二下学期期末联考化学试题
名校
解题方法
9 . 某研究小组设计如下所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
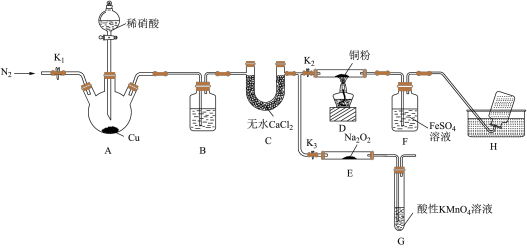
已知:①NO与Na2O2可发生反应2NO+Na2O2===2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为NO3-
③在溶液中存在平衡FeSO4+NO Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是______________________ 。
(2)装置B中盛放的试剂为水,其作用是______________________ 。
(3)装置F中的实验现象为___________ 。装置H中收集的气体为___________ (填化学式)。
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是______________________ 。
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有___________ (填化学式)。
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO2-可将MnO4-还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①滴定过程中发生反应的离子方程式为______________________ 。
②滴定过程中酸性KMnO4溶液的作用是___________ 。
③样品中NaNO2的质量分数为___________ 用含有a、b的代数式表示)

已知:①NO与Na2O2可发生反应2NO+Na2O2===2NaNO2。
②NO能被酸性高锰酸钾溶液氧化为NO3-
③在溶液中存在平衡FeSO4+NO
 Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO2-可将MnO4-还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①滴定过程中发生反应的离子方程式为
②滴定过程中酸性KMnO4溶液的作用是
③样品中NaNO2的质量分数为
您最近一年使用:0次
10 . 某小组探究Na2SO3溶液和KIO3溶液的反应。
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有_________ 性。
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能______ (填“大”或“小”),反应速率慢导致的。
ii.t秒前生成了I2,但由于存在Na2SO3,_____ (用离子方程式表示),I2被消耗。
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入_______ ,蓝色迅速消失,后再次变蓝。
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
① K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,现象是______ 。
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是_______ 。
③ 结合反应解释t2~t3时指针回到“0”处的原因:________ 。
(5)综合实验I、II、III,下列说法正确的是_______ 。
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能
ii.t秒前生成了I2,但由于存在Na2SO3,
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
| 表盘 |  | 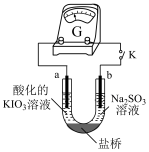 | ||
| 时间/min | 0~t1 | t2~t3 | t4 | |
| 偏转 位置 | 右偏至Y | 指针回到“0”处,又返至“X”处;如此周期性往复多次…… | 指针 归零 | |
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是
③ 结合反应解释t2~t3时指针回到“0”处的原因:
(5)综合实验I、II、III,下列说法正确的是
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
您最近一年使用:0次
2019-04-04更新
|
2440次组卷
|
8卷引用:【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题
【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(A)专题3.2 非金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)《2020年新高考政策解读与配套资源》模拟试题07-2020年北京新高考化学模拟试题北京市海淀区北京大学附中2020 届高三化学阶段性测试化学试题(已下线)第10讲 氯及其化合物-2021年高考化学一轮复习名师精讲练2021年北京高考化学试题变式题11-19 北京市回民学校2023-2024学年高三上学期统练二化学试题



