真题
解题方法
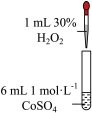
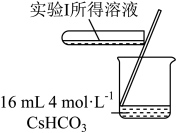
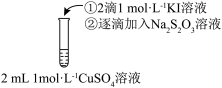
1 . 学习小组为探究 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。
已知: 为粉红色、
为粉红色、 为蓝色、
为蓝色、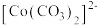 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:
(1)配制 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的_______ (填标号)。
_______ (填“能”或“不能”)催化 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是_______ 。实验Ⅲ初步表明 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式_______ 、_______ 。
(3)实验I表明,反应 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因_______ 。_______ 、_______ 。
 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。| 实验I | 实验Ⅱ | 实验Ⅲ |
|
|
|
| 无明显变化 | 溶液变为红色,伴有气泡产生 | 溶液变为墨绿色,并持续产生能使带火星木条复燃的气体 |
 为粉红色、
为粉红色、 为蓝色、
为蓝色、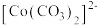 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:(1)配制
 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的a.  b.
b. 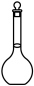 c.
c.  d.
d.

 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式(3)实验I表明,反应
 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因实验Ⅳ:
您最近一年使用:0次
2 . 实验室可用如图装置探究可燃物的燃烧条件,根据所学知识回答下列问题:____ 。
(2)气球的作用是____ 。
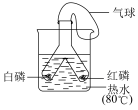
(2)气球的作用是
您最近一年使用:0次
3 .  是最常见的硫的氧化物,某小组利用如图所示的装置制备并检验其性质。下列说法正确的是
是最常见的硫的氧化物,某小组利用如图所示的装置制备并检验其性质。下列说法正确的是
 是最常见的硫的氧化物,某小组利用如图所示的装置制备并检验其性质。下列说法正确的是
是最常见的硫的氧化物,某小组利用如图所示的装置制备并检验其性质。下列说法正确的是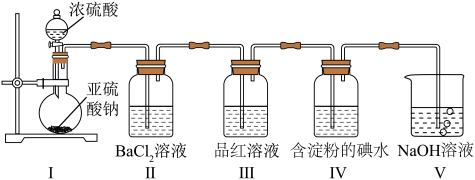
| A.装置Ⅰ中浓硫酸体现强氧化性 |
| B.装置Ⅱ无明显变化,实验结束后向其中通入空气,也无明显变化 |
C.装置Ⅲ中现象证明 具有漂白性,装置Ⅳ中现象证明 具有漂白性,装置Ⅳ中现象证明 具有氧化性 具有氧化性 |
| D.装置V中使用酸性高锰酸钾溶液也可达到实验目的 |
您最近一年使用:0次
名校
4 . 化学小组探究 与
与 是否存在反应,实验过程如下图所示。
是否存在反应,实验过程如下图所示。
 与
与 是否存在反应,实验过程如下图所示。
是否存在反应,实验过程如下图所示。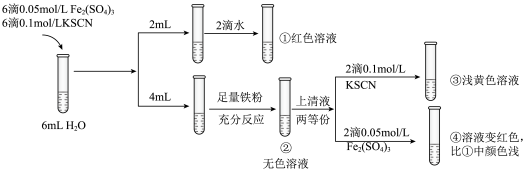
A.②中溶液无色是因为 ,导致平衡 ,导致平衡 逆向移动 逆向移动 |
B.③中溶液略显黄色,可能是因为②→③过程中 被空气氧化 被空气氧化 |
C.④中溶液颜色比①浅,说明 与 与 反应导致 反应导致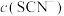 减小 减小 |
D.将向①中加入的2滴水改为2滴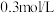  溶液,两次实验后的溶液颜色相同 溶液,两次实验后的溶液颜色相同 |
您最近一年使用:0次
2024-06-06更新
|
149次组卷
|
2卷引用:北京市第二中学2023-2024学年高三下学期三模化学试题
名校
5 . 某小组为探究 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。
已知: ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;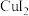 在溶液中不存在;
在溶液中不存在; 呈无色,
呈无色,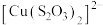 呈黄色。
呈黄色。
下列结论或推断不合理 的是
 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。| 实验 |
|
|
| 现象 | ①产生土黄色沉淀,溶液为棕黄色 ②变为白色悬浊液,最后得到无色澄清溶液 | ①产生土黄色沉淀,溶液为蓝绿色 ②开始变为浅蓝色悬浊液,逐渐变为黄绿色悬浊液,然后变为黄色溶液,最后得到无色溶液 |
 ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;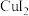 在溶液中不存在;
在溶液中不存在; 呈无色,
呈无色,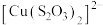 呈黄色。
呈黄色。下列结论或推断
A. 与 与 能发生反应: 能发生反应: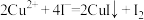 |
B. 与 与 反应的速率快于 反应的速率快于 与 与 反应的速率 反应的速率 |
C.黄绿色悬浊液变为黄色溶液时,有 、 、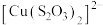 生成 生成 |
D. 与 与 生成配合物反应的限度小于二者发生氧化还原反应的限度 生成配合物反应的限度小于二者发生氧化还原反应的限度 |
您最近一年使用:0次
2024-06-04更新
|
328次组卷
|
2卷引用:北京市海淀区2023-2024学年高三下学期期末练习(二模)化学试题
名校
解题方法
6 . 某小组同学为探究FeSO4的性质设计了如下实验。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)
_______ g,其部分实验操作示意图如下,正确的步骤顺序为_______ (填序号)。
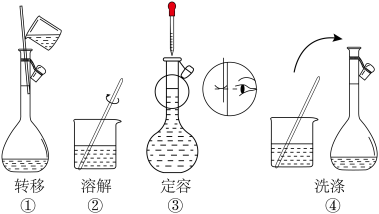
Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:
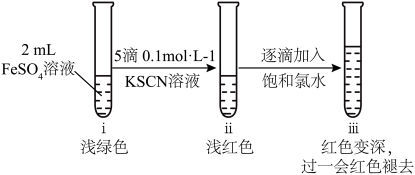
(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在_______ (填离子符号)。
(3)ⅲ中溶液红色变深的主要原因是_______ (用离子方程式表示)。
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
(4)乙同学的猜想是_______ 。为验证甲、乙两位同学的猜想,设计如下实验:将褪色后的溶液分为两等份,一份滴加KSCN溶液,呈血红色;另一份加入氯化铁溶液,无明显现象,则_______ 同学猜想是正确的。
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =_______ g,FeSO4固体在空气氛围中加热时反应的化学方程式为_______ 。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)

Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:

(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在
(3)ⅲ中溶液红色变深的主要原因是
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
| 猜想 | |
| 甲 | +3价铁又被还原成+2价铁 |
| 乙 |
(4)乙同学的猜想是
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =
您最近一年使用:0次
2024-06-01更新
|
180次组卷
|
2卷引用:2024届四川省成都市蓉城名校联盟高三下学期第三次模拟考试理科综合试题-高中化学
名校
7 . 某兴趣小组设计实验验证铜与浓硝酸、稀硝酸的反应,装置如图所示(夹持装置未画出):
按图示连接好装置,_______后,装入药品,关闭 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。
实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是_______ ;装置B中装浓硝酸的仪器名称是_______ 。
(2)实验一中“关闭 、
、 ,打开
,打开 ”的目的是
”的目的是_______
(3)装置B中发生反应的离子方程式为_______
(4)实验二的后续操作顺序为_______ (填标号),打开止水夹后装置C的具支试管中的现象为_______ 。
a.打开止水夹 b.打开 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。
(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2: 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。
继续实验,打开 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明_______ 可能成立,请设计实验验证另一猜想的可能性:_______ 。
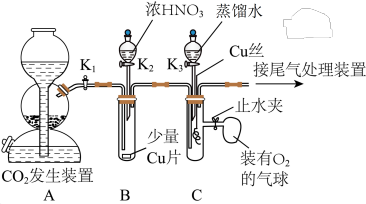
按图示连接好装置,_______后,装入药品,关闭
 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是
(2)实验一中“关闭
 、
、 ,打开
,打开 ”的目的是
”的目的是(3)装置B中发生反应的离子方程式为
(4)实验二的后续操作顺序为
a.打开止水夹 b.打开
 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2:
 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。继续实验,打开
 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明
您最近一年使用:0次
2024-06-01更新
|
391次组卷
|
4卷引用:2024届河南省周口市高三5月全真模拟理科综合试题-高中化学
名校
8 . 在医学上,氯化铵片用于治疗黏痰不易咳出症状,某化学探究活动小组为制备 并探究
并探究 的某些性质,进行了以下实验。回答下列问题:
的某些性质,进行了以下实验。回答下列问题:
步骤一:按上图所示连接装置,进行操作Ⅰ,然后向三颈烧瓶中加入8.0g粉状NaCl,再滴加浓氨水,搅拌至NaCl恰好完全溶解,停止滴加浓氨水,得到饱和氨化食盐水。
步骤二:控制一定范围温度,将 缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的
缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的 ,抽滤。
,抽滤。
步骤三:控制一定范围温度,向滤液中加入适量研细的NaCl,并通入 ,待析出大量晶体时,经过一系列操作,即得
,待析出大量晶体时,经过一系列操作,即得 晶体。
晶体。
已知:①几种物质的溶解度随温度变化如图所示(高于35℃时 开始分解);
开始分解);
(1)步骤一中操作Ⅰ为________________ 。
(2)装置B的作用包括除杂和________________ 。
(3)步骤二和步骤三中适宜的温度分别为________ 和________ (填字母)。步骤二中析出的晶体为________ (填化学式),继续通入 的作用是
的作用是________ 。
A.0~10℃ B.30~35℃ C.55~60℃ D.90~100℃
实验Ⅱ: 溶液的性质探究
溶液的性质探究
向0.5g镁粉中加入足量的 的
的 溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
a.气体成分探究:用排水法(水中滴加几滴紫色石蕊溶液)收集一小试管气体。
(4)____________ (填实验操作或现象,下同),说明气体中含 ;
;________________ ,说明气体中含 。
。
b.沉淀成分探究:将灰白色固体洗净后,再加入稀 溶解,然后滴加几滴
溶解,然后滴加几滴 溶液,有白色沉淀出现。
溶液,有白色沉淀出现。
(5)结合已知信息和实验现象推测,灰白色固体应属于________ (填“混盐”、“复盐”或“碱式盐”),其化学式可能为________ 。
 并探究
并探究 的某些性质,进行了以下实验。回答下列问题:
的某些性质,进行了以下实验。回答下列问题: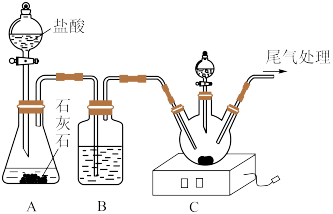

步骤一:按上图所示连接装置,进行操作Ⅰ,然后向三颈烧瓶中加入8.0g粉状NaCl,再滴加浓氨水,搅拌至NaCl恰好完全溶解,停止滴加浓氨水,得到饱和氨化食盐水。
步骤二:控制一定范围温度,将
 缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的
缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的 ,抽滤。
,抽滤。步骤三:控制一定范围温度,向滤液中加入适量研细的NaCl,并通入
 ,待析出大量晶体时,经过一系列操作,即得
,待析出大量晶体时,经过一系列操作,即得 晶体。
晶体。已知:①几种物质的溶解度随温度变化如图所示(高于35℃时
 开始分解);
开始分解);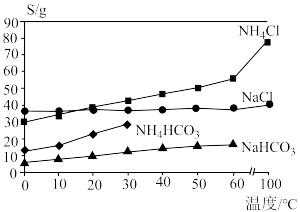
(1)步骤一中操作Ⅰ为
(2)装置B的作用包括除杂和
(3)步骤二和步骤三中适宜的温度分别为
 的作用是
的作用是A.0~10℃ B.30~35℃ C.55~60℃ D.90~100℃
实验Ⅱ:
 溶液的性质探究
溶液的性质探究向0.5g镁粉中加入足量的
 的
的 溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:a.气体成分探究:用排水法(水中滴加几滴紫色石蕊溶液)收集一小试管气体。
(4)
 ;
; 。
。b.沉淀成分探究:将灰白色固体洗净后,再加入稀
 溶解,然后滴加几滴
溶解,然后滴加几滴 溶液,有白色沉淀出现。
溶液,有白色沉淀出现。(5)结合已知信息和实验现象推测,灰白色固体应属于
您最近一年使用:0次
2024-05-31更新
|
55次组卷
|
2卷引用:河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)
名校
解题方法
9 . 探究配制不同金属离子—氨配体溶液的差异性,实验操作及现象如下:
资料:①饱和氨水的浓度约为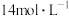
② 为浅青色沉淀
为浅青色沉淀
③ 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液
(1)实验i-a中生成蓝色沉淀的离子方程式为___________ 。
(2)有研究认为蓝色沉淀中还有 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,___________ 。(填后续操作和现象)
(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。___________ ,c=___________ 。
②实验现象是___________ 。
(5)从平衡移动角度,结合化学用语,解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(6)针对实验ii未能成功配制 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:
①在实验ii-a的基础上继续加入___________ ,即可成功配制。
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:___________ 。
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、___________ 。
| 实验序号 | 操作 | 现象 | |
实验i: 的配制 的配制 | 实验i-a | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的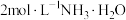 | 产生蓝色沉淀,加入 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 |
| 实验i-b | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的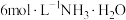 | 产生蓝色沉淀,加入 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 | |
| 实验i-c | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的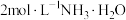 | 产生蓝色沉淀,加入 后沉淀完全溶解,得到澄清的深蓝色溶液。 后沉淀完全溶解,得到澄清的深蓝色溶液。 | |
实验ii: 的配制 的配制 | 实验ii-a | 在试管内混合 溶液和过量 溶液和过量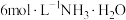 | 得到浅青色沉淀,沉淀未见明显溶解。 |
| 实验ii-b | 在试管内混合 溶液和过量 溶液和过量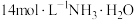 | 得到浅青色沉淀,沉淀未见明显溶解。 | |
实验iii: 的配制 的配制 | 实验iii | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的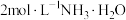 | 产生白色沉淀,加入 后沉淀完全溶解,得到无色溶液。 后沉淀完全溶解,得到无色溶液。 |
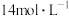
②
 为浅青色沉淀
为浅青色沉淀③
 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液(1)实验i-a中生成蓝色沉淀的离子方程式为
(2)有研究认为蓝色沉淀中还有
 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测
 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。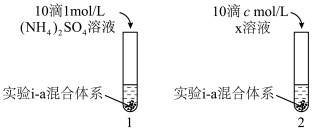
②实验现象是
(5)从平衡移动角度,结合化学用语,解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(6)针对实验ii未能成功配制
 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:①在实验ii-a的基础上继续加入
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、
您最近一年使用:0次
2024-05-31更新
|
278次组卷
|
3卷引用:北京市昌平区2023-2024学年高三下学期二模化学试题
名校
解题方法
10 . 下列各组实验中,实验操作、现象及结论或解释均正确的是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| B | 在干冰中央挖一个小穴,撒一些镁粉,用红热的铁棒把镁引燃,盖上另一块干冰 | 镁粉在干冰中继续燃烧,发出耀眼的白光 | CO2不能扑灭金属镁引起的火灾 |
| C | 向K2S溶液中通入足量的CO2,然后将产生的气体导入CuSO4溶液中 | CuSO4溶液中产生黑色沉淀 | Ka1(H2S)>Ka1(H2CO3) |
| D | 向蔗糖中加入适量浓硫酸,搅拌 | 产生黑色“面包” | 浓硫酸具有酸性和吸水性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-30更新
|
173次组卷
|
2卷引用:广东省深圳市光明区高级中学2023-2024学年高三下学期5月模拟考试化学试题