名校
1 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。_______ ,仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成段液柱,若_______ 则整个装置气密性良好。
(2)A中如果用浓硫酸和铜反应,也可制得 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为_______ 。
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”); 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为_______ 。
(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为_______ 溶液。

(2)A中如果用浓硫酸和铜反应,也可制得
 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是方案
 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为
您最近一年使用:0次
名校
解题方法
2 . 某小组同学欲研究 及
及 的性质。
的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是____________ 。
(2)实验室通常用______试剂检验 。
。
(3)利用如图所示的装置研究 的性质:(熔点:
的性质:(熔点: -
-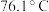 ,
,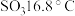 ;沸点:
;沸点: -
- ,
,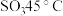 )
)
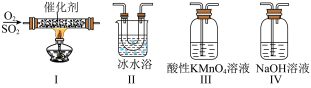
①装置I模拟工业生产中 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是____________ 。
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是____________ ;装置III中溶液逐渐褪色,则该反应的离子方程式是____________ 。
③乙同学按I、II、IV的顺序连接装置,若装置Ⅳ中有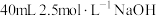 溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式
溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式____________ 。
(4)已知 溶液与
溶液与 反应时,
反应时,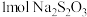 转移
转移 电子。该反应的离子方程式是
电子。该反应的离子方程式是_____ 。
(5)该实验小组的学生丁用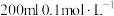 酸性
酸性 溶液测定空气中
溶液测定空气中 含量,若气体流速为
含量,若气体流速为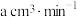 ,当时间为
,当时间为 时酸性
时酸性 溶液恰好褪色,则空气中
溶液恰好褪色,则空气中 的含量为
的含量为___ ( )。
)。
 及
及 的性质。
的性质。(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是
第1组 | 第2组 | 第3组 |
S(单质) |
|
|
 。
。| A.紫色石蕊 | B.品红 | C.酚酞 | D.高锰酸钾 |
 的性质:(熔点:
的性质:(熔点: -
-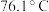 ,
,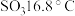 ;沸点:
;沸点: -
- ,
,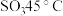 )
)
①装置I模拟工业生产中
 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是
③乙同学按I、II、IV的顺序连接装置,若装置Ⅳ中有
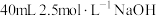 溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式
溶液,反应后增重4.8g,则装置IV中发生总反应的化学方程式(4)已知
 溶液与
溶液与 反应时,
反应时,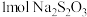 转移
转移 电子。该反应的离子方程式是
电子。该反应的离子方程式是(5)该实验小组的学生丁用
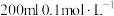 酸性
酸性 溶液测定空气中
溶液测定空气中 含量,若气体流速为
含量,若气体流速为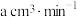 ,当时间为
,当时间为 时酸性
时酸性 溶液恰好褪色,则空气中
溶液恰好褪色,则空气中 的含量为
的含量为 )。
)。
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组在实验室中利用如图装置制备SO2并进行相关性质的探究。回答下列问题:
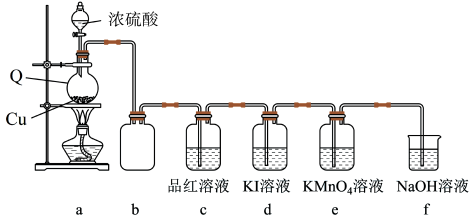
(1)仪器Q的名称为_____ ;装置c中品红溶液褪色,可证明SO2具有_____ 性。
(2)装置b的作用是_____ 。
(3)装置c中KMnO4溶液褪色,可证明SO2具有_____ 性。
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
①取适量装置d中浊液,向其中滴加几滴_____ 溶液(填试剂名称),振荡,无明显变化,浊液中无I2。
②将装置d中浊液进行分离,得淡黄色固体和澄清溶液:取适量分离后的澄清溶液于试管中,_____ ,出现白色沉淀,产物溶液中存在SO 。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为_____ 。

(1)仪器Q的名称为
(2)装置b的作用是
(3)装置c中KMnO4溶液褪色,可证明SO2具有
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。①取适量装置d中浊液,向其中滴加几滴
②将装置d中浊液进行分离,得淡黄色固体和澄清溶液:取适量分离后的澄清溶液于试管中,
 。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
2023-03-27更新
|
363次组卷
|
3卷引用:四川省内江市威远中学校2022-2023学年高一下学期期中考试化学试题
名校
4 . 化学是一门以实验为基础的科学。根据如图回答问题。
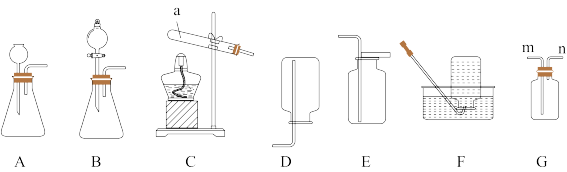
(1)仪器a的名称是_______ 。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学反应方程式为_______ ,若用F装置收集氧气,当观察到_______ 的现象时再开始收集。
(3)甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,应选用的发生装置是_______ (填标号,下同 ),若用G装置收集时,则气体要从
),若用G装置收集时,则气体要从_______ 端通入。
(4)若用如图套管实验装置验证碳酸钠和碳酸氢钠的稳定性,其反应的化学方程式为_______ 、_______ ,试管B中装入的固体最好是_______ (填化学式) 。

(5)碳酸氢钠溶液与过量澄清石灰水反应的离子方程式为_______ 。

(1)仪器a的名称是
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学反应方程式为
(3)甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。实验室常用加热碱石灰氧化钙和氢氧化钠固体的混合物和醋酸钠固体制取甲烷气体,应选用的发生装置是
 ),若用G装置收集时,则气体要从
),若用G装置收集时,则气体要从(4)若用如图套管实验装置验证碳酸钠和碳酸氢钠的稳定性,其反应的化学方程式为

(5)碳酸氢钠溶液与过量澄清石灰水反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 某研究性学习小组对实验室中NH3制取、收集、吸收,以及NH3的还原性探究进行了如下实验设计。
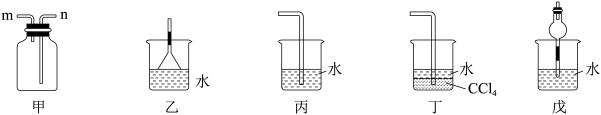
Ⅰ.NH3的收集和吸收
(1)若用图甲装置,排空气法收集NH3,气体应从___________ 口进入(选填“m”或“n”)。
(2)已知NH3难溶于CCl4.图乙、丙、丁、戊四种装置中,不能用来吸收NH3的是___________ 。
Ⅱ.NH3的还原性探究:
利用下列装置,进行NH3还原Fe2O3的反应。
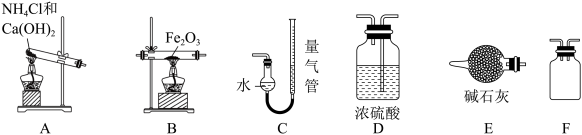
已知:NH3与Fe2O3反应的生成物为Fe、H2O和无毒气体X,且X不被浓硫酸和碱石灰吸收。
(3)采用上图A所示装置作为NH3的发生装置,写出该反应的化学方程式___________ 。
(4)按气流方向正确的装置连接顺序为A→___________ →___________ →___________ →___________ →C(填序号,每个装置只用一次)。装置连接后,首先应进行的操作是___________ 。
(5)实验结束时,应首先___________ (填序号)。
①熄灭A装置的酒精灯 ②熄灭B装置的酒精灯
(6)若称取1.6克Fe2O3完全反应后,测得生成气体X的体积为 (已折算为标准状况),通过计算推测B中NH3与Fe2O3反应的化学方程式为
(已折算为标准状况),通过计算推测B中NH3与Fe2O3反应的化学方程式为___________ 。
Ⅰ.NH3的收集和吸收
(1)若用图甲装置,排空气法收集NH3,气体应从
(2)已知NH3难溶于CCl4.图乙、丙、丁、戊四种装置中,不能用来吸收NH3的是

Ⅱ.NH3的还原性探究:
利用下列装置,进行NH3还原Fe2O3的反应。

已知:NH3与Fe2O3反应的生成物为Fe、H2O和无毒气体X,且X不被浓硫酸和碱石灰吸收。
(3)采用上图A所示装置作为NH3的发生装置,写出该反应的化学方程式
(4)按气流方向正确的装置连接顺序为A→
(5)实验结束时,应首先
①熄灭A装置的酒精灯 ②熄灭B装置的酒精灯
(6)若称取1.6克Fe2O3完全反应后,测得生成气体X的体积为
 (已折算为标准状况),通过计算推测B中NH3与Fe2O3反应的化学方程式为
(已折算为标准状况),通过计算推测B中NH3与Fe2O3反应的化学方程式为
您最近一年使用:0次
2021-04-06更新
|
337次组卷
|
4卷引用:四川省内江市第六中学2020-2021学年高一下期期中考试化学试题
名校
6 . 乙二酸(化学式 H2C2O4)又名草酸是二元弱酸,具有强还原性,不稳定性,在189.5℃或遇浓硫酸会分解生成CO、CO2和H2O;草酸在150—160℃升华。草酸盐溶解性与碳酸盐类似。
Ⅰ某同学设计如下实验,完成对草酸部分分解产物的检验

(1)分解草酸应选图1中_______ (填序号)
(2)证明产物中含有CO的实验现象______________
(3)若没有装置A,B中澄清石灰水变浑浊,______ (填“能”或“不能”,填“能”下空不回答)说明草酸分解产物中含有CO2,原因是______________ (用离子方程式解释)
(4)气囊的作用为_______________
Ⅱ草酸浓度的标定可以用标准KMnO4滴定。
(5)标准KMnO4溶液应盛装在_______ 滴定管。
(6)滴定终点现象为____________________
(7)滴定完仰视读数,使标定的草酸浓度___________ (填“偏大”或“偏小”或“无影响”)
(8)写出滴定时反应的离子反应______________________
Ⅰ某同学设计如下实验,完成对草酸部分分解产物的检验

(1)分解草酸应选图1中
(2)证明产物中含有CO的实验现象
(3)若没有装置A,B中澄清石灰水变浑浊,
(4)气囊的作用为
Ⅱ草酸浓度的标定可以用标准KMnO4滴定。
(5)标准KMnO4溶液应盛装在
(6)滴定终点现象为
(7)滴定完仰视读数,使标定的草酸浓度
(8)写出滴定时反应的离子反应
您最近一年使用:0次
2020-10-19更新
|
202次组卷
|
5卷引用:四川省内江市威远中学校2022-2023学年高二下学期期中考试化学试题
名校
解题方法
7 . 某化学兴趣小组探究石蜡油分解产物,设计了如图实验方案。下列说法错误的是
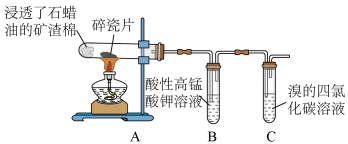

| A.碎瓷片有催化和积蓄热量的作用 |
| B.点燃C 出口处,火焰明亮,伴有黑烟 |
| C.B、C 中溶液均褪色,反应类型相同 |
| D.结束反应时,先撤出导管,再停止加热 |
您最近一年使用:0次

 、
、
 、
、 、
、 、
、


