1 . 化学实验兴趣小组为了探究在实验室制备 的过程中有水蒸气挥发出来,同时验证
的过程中有水蒸气挥发出来,同时验证 的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
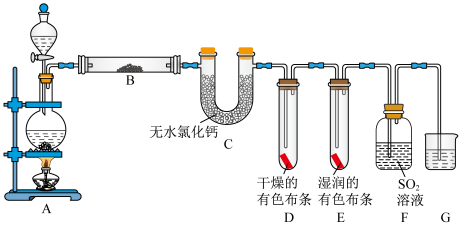
(1)实验室制备 的反应原理中,从氧化还原的角度分析,
的反应原理中,从氧化还原的角度分析, 属于
属于___________ 产物。
(2)在标准状况下,若用含0.2mol HCl的浓盐酸与足量的 反应制取
反应制取 ,制得
,制得 体积
体积____________ (填“>”、“<”、“=”)1.12L。
(3)装置B中盛放无水 ,若出现的现象为
,若出现的现象为____________________________________ ,说明生成 含有水蒸气。
含有水蒸气。
(4)实验时装置D和E中出现了不同的现象,说明装置E中氯气与水发生反应的化学方程式为____________________________________ 。
(5)当装置F中通入 ,发生反应的离子方程式为
,发生反应的离子方程式为________________________________ 。
(6)装置G中应放入____________ ,吸收多余 ,防止污染环境。
,防止污染环境。
(7)某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1。则氯气与
的个数比为3:1。则氯气与 反应时,被还原的氯原子和被氧化的氯原子的个数比为
反应时,被还原的氯原子和被氧化的氯原子的个数比为____________ 。
 的过程中有水蒸气挥发出来,同时验证
的过程中有水蒸气挥发出来,同时验证 的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
(1)实验室制备
 的反应原理中,从氧化还原的角度分析,
的反应原理中,从氧化还原的角度分析, 属于
属于(2)在标准状况下,若用含0.2mol HCl的浓盐酸与足量的
 反应制取
反应制取 ,制得
,制得 体积
体积(3)装置B中盛放无水
 ,若出现的现象为
,若出现的现象为 含有水蒸气。
含有水蒸气。(4)实验时装置D和E中出现了不同的现象,说明装置E中氯气与水发生反应的化学方程式为
(5)当装置F中通入
 ,发生反应的离子方程式为
,发生反应的离子方程式为(6)装置G中应放入
 ,防止污染环境。
,防止污染环境。(7)某温度下,将氯气通入
 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1。则氯气与
的个数比为3:1。则氯气与 反应时,被还原的氯原子和被氧化的氯原子的个数比为
反应时,被还原的氯原子和被氧化的氯原子的个数比为
您最近一年使用:0次
名校
解题方法
2 . 氯及其化合物在工业生产生活中有很重要的作用。图①中为实验室制取氧气及性质验证的装置图。

(1)盛放浓盐酸的仪器名称:___________ ;利用装置A制备Cl2,写出该反应的离子方程式:___________
(2)装置B的作用:___________ ;装置C中的试剂:___________
(3)若图①装置中a为干燥的有色布条,b为湿润的有色布条,可观察到的实验现象:___________ ;通过实验现象说明什么结论:___________ ;
(4)写出装置D中发生反应的离子方程式:___________ ;
(5)实验室也可用KMnO4和浓盐酸制取氯气,反应如下:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。该反应中被氧化的HCl与起酸性的HCl物质的量比为___________ ;用单线桥标出电子转移的方向和数目:___________ ,图②作为最佳发生装置是___________ 。
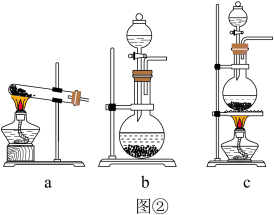

(1)盛放浓盐酸的仪器名称:
(2)装置B的作用:
(3)若图①装置中a为干燥的有色布条,b为湿润的有色布条,可观察到的实验现象:
(4)写出装置D中发生反应的离子方程式:
(5)实验室也可用KMnO4和浓盐酸制取氯气,反应如下:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。该反应中被氧化的HCl与起酸性的HCl物质的量比为

您最近一年使用:0次
2024-01-09更新
|
148次组卷
|
4卷引用:江西省抚州市资溪县第一中学2023-2024学年高一上学期11月期中考试化学试题
3 . 某化学兴趣小组利用如图所示装置进行“铁与水蒸气反应”的实验,并检验产物的性质。请回答下列问题:
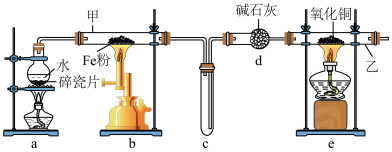
(1)整套装置中,先点燃___________ (填“a”或“b”)处的酒精灯或酒精喷灯,装置a的作用是___________ 。
(2)写出仪器甲中发生反应的化学方程式:___________ 。
(3)装置e的现象是___________ 。

(1)整套装置中,先点燃
(2)写出仪器甲中发生反应的化学方程式:
(3)装置e的现象是
您最近一年使用:0次
名校
4 . 某实验小组欲探究 的相关性质,设计了如下实验,并用
的相关性质,设计了如下实验,并用 传感器测得容器内
传感器测得容器内 的分压变化如图所示。
的分压变化如图所示。
实验①:在锥形瓶内装入新配制的饱和 溶液,测得密闭容器内
溶液,测得密闭容器内 的分压如图1;
的分压如图1;
实验②:在锥形瓶内加入水,再依次加入碳酸氢钠固体、氯化钙固体,测得密闭容器内 的分压如图2。
的分压如图2。
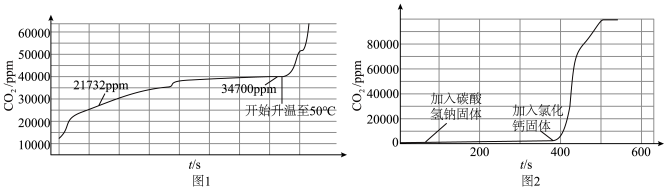
下列有关说法正确的是
 的相关性质,设计了如下实验,并用
的相关性质,设计了如下实验,并用 传感器测得容器内
传感器测得容器内 的分压变化如图所示。
的分压变化如图所示。实验①:在锥形瓶内装入新配制的饱和
 溶液,测得密闭容器内
溶液,测得密闭容器内 的分压如图1;
的分压如图1;实验②:在锥形瓶内加入水,再依次加入碳酸氢钠固体、氯化钙固体,测得密闭容器内
 的分压如图2。
的分压如图2。
下列有关说法正确的是
A.实验①中,饱和 溶液在加热过程中未发生分解 溶液在加热过程中未发生分解 |
B.实验①中,加入酚酞指示剂,加热至 时,溶液红色变浅 时,溶液红色变浅 |
| C.实验②中,溶液中所有离子质量都减少 |
D.实验②中,发生反应: |
您最近一年使用:0次
2023-12-26更新
|
155次组卷
|
2卷引用:江西省鹰潭市2023-2024学年高一上学期11月期中化学试题
名校
解题方法
5 . 某化学兴趣小组用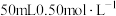 盐酸与
盐酸与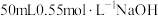 溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:

(1)实验时玻璃搅拌器的使用方法是___________ ;不能用铜质搅拌器代替玻璃搅拌器的理由是___________ 。
(2)NaOH溶液稍过量的原因是___________ 。
(3)某同学记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为 ,中和反应后溶液的比热容
,中和反应后溶液的比热容 )
)
依据该同学的实验数据计算,该实验测得反应放出的热量为___________ J。
(4)下列操作会导致实验结果出现偏差的是___________ (填字母)。
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将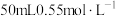 氢氧化钠溶液取成了
氢氧化钠溶液取成了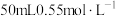 氢氧化钾溶液
氢氧化钾溶液
d.做本实验的当天室温较高
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得的中和反应反应热( )
)___________ (填“偏大”、“偏小”或“不变”)。
(6)如果用 盐酸与
盐酸与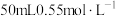 溶液进行实验,与上述实验相比,二者所放出的热量
溶液进行实验,与上述实验相比,二者所放出的热量___________ (填“相等”或“不相等”,下同),所求的中和反应反应热( )
)___________
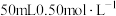 盐酸与
盐酸与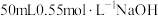 溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
(1)实验时玻璃搅拌器的使用方法是
(2)NaOH溶液稍过量的原因是
(3)某同学记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为
 ,中和反应后溶液的比热容
,中和反应后溶液的比热容 )
)| 实验序号 | 起始温度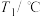 | 终止温度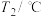 | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.3 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.4 | 20.6 | 23.8 |
(4)下列操作会导致实验结果出现偏差的是
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将
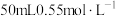 氢氧化钠溶液取成了
氢氧化钠溶液取成了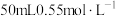 氢氧化钾溶液
氢氧化钾溶液d.做本实验的当天室温较高
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得的中和反应反应热(
 )
)(6)如果用
 盐酸与
盐酸与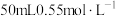 溶液进行实验,与上述实验相比,二者所放出的热量
溶液进行实验,与上述实验相比,二者所放出的热量 )
)
您最近一年使用:0次
2023-12-03更新
|
54次组卷
|
2卷引用:江西省抚州市资溪县第一中学2023-2024学年高二上学期11月期中化学试题
名校
解题方法
6 . 某研究性学习小组同学为探究氯气的性质,设计如图装置进行实验探究。

下列说法不正确的是

下列说法不正确的是
A.利用装置 可探究氯气是否有漂白性 可探究氯气是否有漂白性 |
B.通入氯气后可观察到装置 中溶液变红 中溶液变红 |
C.装置 中产生白色沉淀说明氯气与水反应生成了 中产生白色沉淀说明氯气与水反应生成了 |
D.装置e中反应的离子方程式: |
您最近一年使用:0次
2023-12-02更新
|
260次组卷
|
3卷引用:江西省鹰潭市2023-2024学年高一上学期11月期中化学试题
江西省鹰潭市2023-2024学年高一上学期11月期中化学试题江西省部分学校2023-2024学年高一上学期11月期中考试化学试题(已下线)寒假作业05 氯及其化合物-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)
名校
解题方法
7 . 某同学类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他在实验室中选择以下装置对该反应能否发生进行了实验探究。
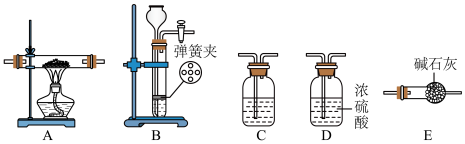
依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置___________ (填装置下方对应字母),反应的化学方程式为___________ 。
(2)装置 C所装的试剂是___________ ,发生的反应为(用离子方程式表示)___________ 。
(3)为达到实验目的,选择上图中的装置,其连接顺序为:按二氧化碳的发生装置→___________ 。(按气流方向,填写装置的大写字母)。
(4)操作中通空气和加热的先后顺序为___________ 。
(5)该同学在制取 的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
(6)若反应过程中 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为 ;②生成的固体物质为
;②生成的固体物质为 和C的混合物③生成的固体物质为
和C的混合物③生成的固体物质为 和
和 的混合物;④生成的固体物质为
的混合物;④生成的固体物质为 和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是___________ ;则钠与 反应的化学方程式为
反应的化学方程式为___________ 。
(7)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知, 溶液可以吸收
溶液可以吸收 ,同时得到黑色的
,同时得到黑色的 和一种酸。于是他在装置后加装一个盛
和一种酸。于是他在装置后加装一个盛 溶液的吸收装置,该装置中发生反应的化学方程式为
溶液的吸收装置,该装置中发生反应的化学方程式为___________ 。

依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置
(2)装置 C所装的试剂是
(3)为达到实验目的,选择上图中的装置,其连接顺序为:按二氧化碳的发生装置→
(4)操作中通空气和加热的先后顺序为
(5)该同学在制取
 的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。
的过程中,向装置B中加入某酸后,发现固体与酸没有接触,为使反应顺利进行,下列可再加入的试剂是___________。| A.稀硝酸 | B. 溶液 溶液 |
| C.煤油 | D. (无色有机溶剂,与水互不相溶,密度比水大) (无色有机溶剂,与水互不相溶,密度比水大) |
(6)若反应过程中
 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为 ;②生成的固体物质为
;②生成的固体物质为 和C的混合物③生成的固体物质为
和C的混合物③生成的固体物质为 和
和 的混合物;④生成的固体物质为
的混合物;④生成的固体物质为 和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是 反应的化学方程式为
反应的化学方程式为(7)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,
 溶液可以吸收
溶液可以吸收 ,同时得到黑色的
,同时得到黑色的 和一种酸。于是他在装置后加装一个盛
和一种酸。于是他在装置后加装一个盛 溶液的吸收装置,该装置中发生反应的化学方程式为
溶液的吸收装置,该装置中发生反应的化学方程式为
您最近一年使用:0次
2023-11-28更新
|
120次组卷
|
2卷引用:江西省抚州市资溪县第一中学2023-2024学年高一上学期11月期中考试化学试题
8 . 某实验小组用收集到的氯气制得氯水并对氯水成分和性质进行研究,实验如下:
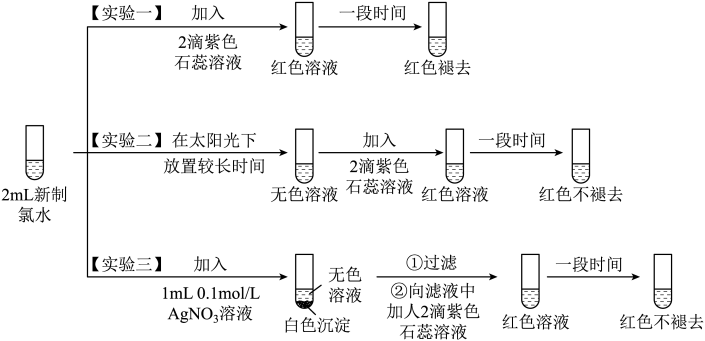
(1)实验一的现象表明,氯水具有酸性和___________ 性。
(2)氯气与水反应的化学方程式为___________ 。
(3)用化学方程式说明实验二中“红色不褪去”的原因___________ 。
【实验四】
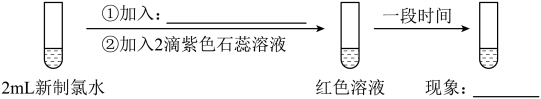
(4)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象___________ 、___________ 。
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(5)由此确定实验三的白色沉淀主要成分为___________ 。

(1)实验一的现象表明,氯水具有酸性和
(2)氯气与水反应的化学方程式为
(3)用化学方程式说明实验二中“红色不褪去”的原因
【实验四】

(4)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(5)由此确定实验三的白色沉淀主要成分为
您最近一年使用:0次
名校
解题方法
9 . 1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
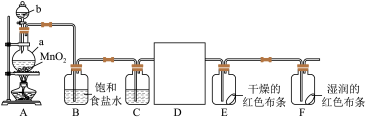
(1)仪器b的名称为___________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为___________ 。
(2)仪器a中发生反应的化学方程式为___________ 。根据氯气的性质D中的收集装置可以选择___________ (填序号)。
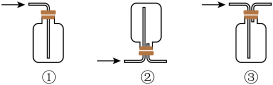
(3)下列有关该实验的说法中不正确 的是___________(填字母)。
(4)实验室还可用等物质的量的 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为___________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中
| A.将b中溶液换为稀盐酸,同样可以产生氯气 |
| B.C中试剂是浓硫酸,目的是干燥氯气 |
| C.F中红色布条褪色,证明氯气具有漂白性 |
| D.可用湿润的淀粉碘化钾试纸检验氯气是否收集满 |
(4)实验室还可用等物质的量的
 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为
您最近一年使用:0次
2023-11-22更新
|
211次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高一上学期11月期中化学试题
名校
10 . 某化学兴趣小组查阅资料后制备过氧化钠,并设计实验验证其相关性质。
(1)某小组查阅资料发现, 用途广泛,写出
用途广泛,写出 的一种用途;
的一种用途;___________ ; 能与盐酸发生剧烈反应,写出该反应的化学方程式:
能与盐酸发生剧烈反应,写出该反应的化学方程式:___________ 。
(2)某小组同学取一定量淡黄色固体粉末溶于冷水中,待固体粉末全部反应后,仍可缓慢释放出气体。为探究该固体粉末溶解后的溶液成分,设计如下实验:

①如何证明乙中产生的气体是什么物质?___________ 。
②乙→丙过程说明固体粉末溶解后溶液中含有___________ (填化学式), 在丙中的作用是
在丙中的作用是___________ 。
(3)为验证 与
与 能否反应,该小组同学设计如下实验:
能否反应,该小组同学设计如下实验:
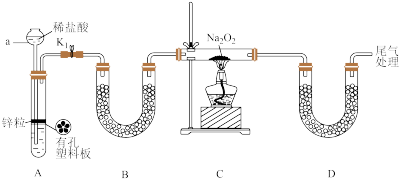
①仪器a的名称是___________ ;装置B的作用是___________ 。
②若 与
与 能反应产生
能反应产生 ,该实验装置C、D之间还缺少检验反应产物
,该实验装置C、D之间还缺少检验反应产物 的装置,缺少的仪器和药品是
的装置,缺少的仪器和药品是___________ 。
(1)某小组查阅资料发现,
 用途广泛,写出
用途广泛,写出 的一种用途;
的一种用途; 能与盐酸发生剧烈反应,写出该反应的化学方程式:
能与盐酸发生剧烈反应,写出该反应的化学方程式:(2)某小组同学取一定量淡黄色固体粉末溶于冷水中,待固体粉末全部反应后,仍可缓慢释放出气体。为探究该固体粉末溶解后的溶液成分,设计如下实验:

①如何证明乙中产生的气体是什么物质?
②乙→丙过程说明固体粉末溶解后溶液中含有
 在丙中的作用是
在丙中的作用是(3)为验证
 与
与 能否反应,该小组同学设计如下实验:
能否反应,该小组同学设计如下实验:
①仪器a的名称是
②若
 与
与 能反应产生
能反应产生 ,该实验装置C、D之间还缺少检验反应产物
,该实验装置C、D之间还缺少检验反应产物 的装置,缺少的仪器和药品是
的装置,缺少的仪器和药品是
您最近一年使用:0次



