1 . 草酸亚铁晶体( ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。

(1)按照气流从左到右的方向,上述装置的接口顺序为A→_______ →尾气处理装置(仪器可重复使用)。
(2)实验证明了气体产物中含有 ,依据的实验现象为
,依据的实验现象为_______ 。
(3)实验证明了气体产物中含有CO,依据的实验现象为_______ 。
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(5)工业制得的草酸亚铁晶体中常含有 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品溶于稀 中,配成250 mL溶液;
中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用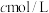
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 ,再用
,再用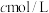
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。
①步骤2中滴定终点的现象为_______ 。
②该样品中草酸亚铁晶体的质量分数的表达式为_______ 。
③若步骤1配制溶液时部分 被氧化变质,则测定结果将
被氧化变质,则测定结果将_______ (填“偏高”“偏低”或“不变”)。
 ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
(1)按照气流从左到右的方向,上述装置的接口顺序为A→
(2)实验证明了气体产物中含有
 ,依据的实验现象为
,依据的实验现象为(3)实验证明了气体产物中含有CO,依据的实验现象为
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(5)工业制得的草酸亚铁晶体中常含有
 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:步骤1:称取m g草酸亚铁晶体样品溶于稀
 中,配成250 mL溶液;
中,配成250 mL溶液;步骤2:取上述溶液25.00 mL,用
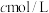
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀
 ,再用
,再用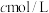
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。①步骤2中滴定终点的现象为
②该样品中草酸亚铁晶体的质量分数的表达式为
③若步骤1配制溶液时部分
 被氧化变质,则测定结果将
被氧化变质,则测定结果将
您最近一年使用:0次
2022-12-16更新
|
190次组卷
|
2卷引用:辽宁省大连市滨城联盟2022-2023学年高三上学期期中(‖)考试化学试题
2 . 某化学兴趣小组用如图Ⅰ所示的装置进行制取乙烯的实验CH3CH2OH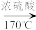 CH2=CH2↑+H2O。当温度迅速上升后,可观察到试管中的溴水褪色,反应混合液变为黑色且产生的气体有刺激性气味。
CH2=CH2↑+H2O。当温度迅速上升后,可观察到试管中的溴水褪色,反应混合液变为黑色且产生的气体有刺激性气味。
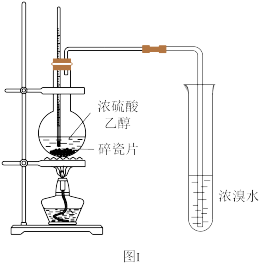
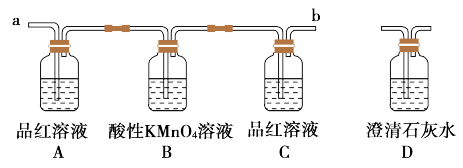
(1)装浓硫酸与乙醇混合液的仪器名称是_______ 。
(2)经分析黑色物质是碳单质,该过程体现了浓硫酸的_______ 性。
(3)写出使溴水褪色可能的化学方程式_______ 、_______ 。
(4)某同学想检验发生装置中是否有CO2产生,准备利用后边的装置进行检验,其中试剂选择明显错误的是_______ (填字母)可以用_______ 代替,可以证明有CO2产生的现象是_______ 。
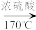 CH2=CH2↑+H2O。当温度迅速上升后,可观察到试管中的溴水褪色,反应混合液变为黑色且产生的气体有刺激性气味。
CH2=CH2↑+H2O。当温度迅速上升后,可观察到试管中的溴水褪色,反应混合液变为黑色且产生的气体有刺激性气味。

(1)装浓硫酸与乙醇混合液的仪器名称是
(2)经分析黑色物质是碳单质,该过程体现了浓硫酸的
(3)写出使溴水褪色可能的化学方程式
(4)某同学想检验发生装置中是否有CO2产生,准备利用后边的装置进行检验,其中试剂选择明显错误的是
您最近一年使用:0次
解题方法
3 . 8.34g FeSO4·7H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。回答下列问题:
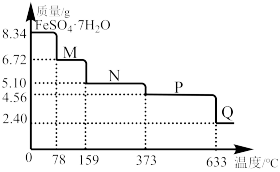
(1)试确定200℃时固体物质N的化学式___________ 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式___________ 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
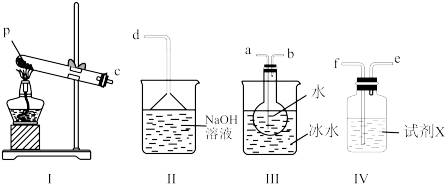
①试剂X的名称是___________ 。
②按气流方向连接仪器,用字母表示接口的连接顺序:c→___________ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为___________ g.(填计算式)

(1)试确定200℃时固体物质N的化学式
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是
②按气流方向连接仪器,用字母表示接口的连接顺序:c→
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为
您最近一年使用:0次
名校
解题方法
4 . SO2在生产、生活中具有重要的作用,据所学知识回答相关问题。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有___________ (填“酸性”、“氧化性”、“还原性”或“漂白性”,下同),SO2通入品红溶液中,品红溶液褪色,说明SO2具有___________ 。
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为___________ ,请写出该反应的离子方程式___________ 。
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为___________ ,若反应中有0.1mol电子转移,则生成ZnS2O4___________ g。
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为___________ 。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 把氢气、氮气、二氧化碳、一氧化碳组成的混合气体,先通过灼热的氧化铜,再依次通过烧碱溶液和浓硫酸,最后剩下的气体是________ ;如果把原混合气体先通过烧碱溶液,然后再依次通过灼热的氧化铜和浓硫酸,最后剩下的气体是________
您最近一年使用:0次
名校
6 . 某化学学习小组为了探究镁和二氧化硫的反应产物,进行如下实验。
Ⅰ.设计如图所示装置完成镁和二氧化硫的反应。
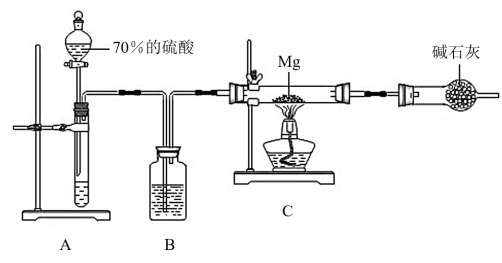
(1)实验室用亚硫酸钠与浓硫酸反应制备SO2,利用的是浓硫酸的___________
a.强氧化性 b.强酸性 c.脱水性 d.腐蚀性
(2)B装置中试剂的名称是_____________ ;E装置的作用是_________________ 。
Ⅱ.探究燃烧的反应产物
(3)反应后取C装置中的固体粉末于烧瓶F中,加入稀硫酸,有气体生成
①产生的气体中含有氢气,则可说明固体中含有______________
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是______________ (用离子方程式表示)
(4)取出F装置烧瓶中的混合物,经过滤、干燥得到少量固体粉末,为了探究固体粉末的成分,选择下列装置进行实验:
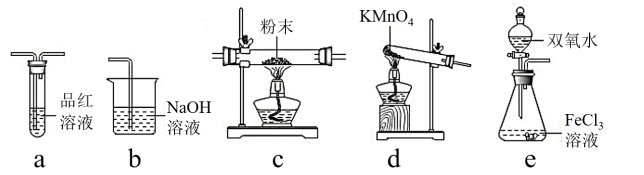
①按气体从左至右,选择所需装置,正确的连接顺序为______________ (字母 )
②能证明固体粉末是硫磺的实验现象是_____________________ 。
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,写出镁与SO2在加热条件下反应的化学方程式:________________ 。
Ⅰ.设计如图所示装置完成镁和二氧化硫的反应。

(1)实验室用亚硫酸钠与浓硫酸反应制备SO2,利用的是浓硫酸的
a.强氧化性 b.强酸性 c.脱水性 d.腐蚀性
(2)B装置中试剂的名称是
Ⅱ.探究燃烧的反应产物
(3)反应后取C装置中的固体粉末于烧瓶F中,加入稀硫酸,有气体生成
①产生的气体中含有氢气,则可说明固体中含有
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是
(4)取出F装置烧瓶中的混合物,经过滤、干燥得到少量固体粉末,为了探究固体粉末的成分,选择下列装置进行实验:

①按气体从左至右,选择所需装置,正确的连接顺序为
②能证明固体粉末是硫磺的实验现象是
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,写出镁与SO2在加热条件下反应的化学方程式:
您最近一年使用:0次



