1 . 数字化实验在化学研究中发挥了重要的作用。
(1)某实验小组探究氢氧化钠溶液与二氧化碳的反应。将电脑、数字化实验中压强传感器通过真空橡胶管与盛有二氧化碳的烧瓶相连,迅速注入80mL的40%氢氧化钠溶液。得到实验压强变化如曲线A。

①仪器甲的名称是___________ ,曲线A的变化趋势可能的原因是:二氧化碳与氢氧化钠溶液反应或可能原因是___________ 。
②为了更科学的判断二氧化碳与氢氧化钠溶液反应发生,还需用80mL___________ (填写试剂名称)做同样的实验得曲线B,这样做的原因是___________ 。
(2)实验(1)能说明氢氧化钠溶液与二氧化碳反应,但不能确定反应产物。由此实验小组进行了以下实验:
实验A中发生反应的离子方程式是___________ ;实验B中生成物的名称是___________ 。
(3)由实验(1)(2)说明氢氧化钠溶液能与二氧化碳反应,且随着通入二氧化碳的量不同反应的产物不同。若同时生成两种产物,检验产物的方法是:先向反应后的产物中滴加足量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中滴加___________ (填写试剂名称),观察到的现象是___________ ,证明同时有两种产物生成。
(1)某实验小组探究氢氧化钠溶液与二氧化碳的反应。将电脑、数字化实验中压强传感器通过真空橡胶管与盛有二氧化碳的烧瓶相连,迅速注入80mL的40%氢氧化钠溶液。得到实验压强变化如曲线A。

①仪器甲的名称是
②为了更科学的判断二氧化碳与氢氧化钠溶液反应发生,还需用80mL
(2)实验(1)能说明氢氧化钠溶液与二氧化碳反应,但不能确定反应产物。由此实验小组进行了以下实验:
| 实验步骤 | 实验现象 |
| 实验A:向氢氧化钠溶液中通入足量二氧化碳后,然后滴加氯化钡溶液 | 没有沉淀产生 |
| 实验B:向氢氧化钠溶液中通入少量二氧化碳后,然后滴加氯化钡溶液。 | 产生白色沉淀 |
(3)由实验(1)(2)说明氢氧化钠溶液能与二氧化碳反应,且随着通入二氧化碳的量不同反应的产物不同。若同时生成两种产物,检验产物的方法是:先向反应后的产物中滴加足量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中滴加
您最近一年使用:0次
2 . 为探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,按以下装置图进行实验,按要求填空。
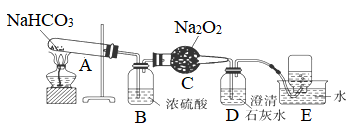
(1)A中反应的化学方程式为________ 。
(2)B中浓硫酸的作用是____ 。
(3)C中发生反应的化学方程式为____ ,每反应1molNa2O2转移______ mol电子。
(4)D中现象是_____ ,反应的离子方程式是_____________________ 。
(5)E中收集的气体主要是________________ 。

(1)A中反应的化学方程式为
(2)B中浓硫酸的作用是
(3)C中发生反应的化学方程式为
(4)D中现象是
(5)E中收集的气体主要是
您最近一年使用:0次
2018-08-25更新
|
1202次组卷
|
4卷引用:广西壮族自治区桂林十八中2014-2015学年高一下学期开学考试化学试卷
广西壮族自治区桂林十八中2014-2015学年高一下学期开学考试化学试卷湖南省衡阳县2017-2018学年高二下学期期末考试化学试题(已下线)2018年11月3日 《每日一题》人教必修1- 周末培优河南省南阳市内乡县菊潭高级中学2022届高三入学考试化学试题
14-15高三上·四川成都·阶段练习
名校
解题方法
3 . 为验证氧化性Cl2>Fe3+> SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
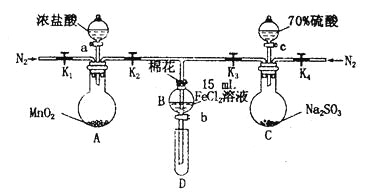
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程I的目的是______________________________________________________________________________ 。
(2)检验B中溶液是否还有Fe2+的方法之一是:取少量B中溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生蓝色沉淀.写出该反应的离子方程式___________________________________________________________________________________________________________________________________________________ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式_____________________________________________________________ 。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定不能够证明氧化性Cl2>Fe3+>SO2的是_____________________________ (填“甲”、“乙”或“丙”)。
(6)将B中的FeCl2溶液换成100 mLFeBr2溶液并向其中通入1.12 LCl2(标准状况下),若溶液中有1/2的Br一被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为________ mol/L。

实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程I的目的是
(2)检验B中溶液是否还有Fe2+的方法之一是:取少量B中溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生蓝色沉淀.写出该反应的离子方程式
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定不能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中 含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
(6)将B中的FeCl2溶液换成100 mLFeBr2溶液并向其中通入1.12 LCl2(标准状况下),若溶液中有1/2的Br一被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
您最近一年使用:0次
2016-12-09更新
|
725次组卷
|
6卷引用:广西钦州市钦州港经济技术开发区中学2017届高三下学期期中考试化学试题
11-12高一上·广西桂林·阶段练习
4 . 根据要求填写:
(1)金属钠在空气中燃烧,火焰呈__ 色,化学方程式:_______________________ ;
(2)将过氧化钠固体放入试管中加入少量水,再加入几滴酚酞试液,溶液变红色但很快褪色,原因是:_____________________________________ ,过氧化钠固体与水反应的化学方程式:______________________________________________ ;
(3)苏打和小苏打分别和同浓度的盐酸反应,反应较快且剧烈的是______ (填化学式),小苏打与盐酸反应的离子方程式为:________________________________________ ;
(4)金属钠和金属钾分别和水反应试验中,其中反应较剧烈的反应的化学方程式:___________________________________________ ;
(1)金属钠在空气中燃烧,火焰呈
(2)将过氧化钠固体放入试管中加入少量水,再加入几滴酚酞试液,溶液变红色但很快褪色,原因是:
(3)苏打和小苏打分别和同浓度的盐酸反应,反应较快且剧烈的是
(4)金属钠和金属钾分别和水反应试验中,其中反应较剧烈的反应的化学方程式:
您最近一年使用:0次



