1 . 亚硝酸钠(NaNO2)为白色粉末,易溶于水,味微咸,有毒;广泛应用于工业建筑领域,允许限量做食品添加剂,用于防腐和肉制品增色。某化学小组对亚硝酸钠的性质和用途进行了如下探究。
(1)NaNO2中N元素的化合价为__ ,据此推断NaNO2__ (填字母)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(2)资料表明:误食NaNO2后,血红蛋白中的亚铁转变成三价铁,失去携氧功能,因此造成人体缺氧中毒。
①预测性质:上述过程中NaNO2作___________ (填“氧化剂”或“还原剂”)。
②实验和结论:取NaNO2固体配成溶液,取少量溶液于试管中,滴入___________ (填“FeSO4溶液、KSCN溶液”或“酸性KMnO4溶液”),观察到的实验现象为___________ ,据此得出预测结论。
(3)该小组查阅资料得知工业制备亚硝酸钠的途径有两种。
途径一:NaNO3加热到380℃分解2NaNO3 2NaNO2+O2↑。
2NaNO2+O2↑。
途径二:NaOH溶液吸收NO、NO2气体。
①写出途径二反应的离子方程式___________ 。
②制备等量的NaNO2途径一与途径二转移电子的物质的量之比为___________ 。
(1)NaNO2中N元素的化合价为
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(2)资料表明:误食NaNO2后,血红蛋白中的亚铁转变成三价铁,失去携氧功能,因此造成人体缺氧中毒。
①预测性质:上述过程中NaNO2作
②实验和结论:取NaNO2固体配成溶液,取少量溶液于试管中,滴入
(3)该小组查阅资料得知工业制备亚硝酸钠的途径有两种。
途径一:NaNO3加热到380℃分解2NaNO3
 2NaNO2+O2↑。
2NaNO2+O2↑。途径二:NaOH溶液吸收NO、NO2气体。
①写出途径二反应的离子方程式
②制备等量的NaNO2途径一与途径二转移电子的物质的量之比为
您最近一年使用:0次
2 . 氯化铁(FeCl3)是一种易潮解、易升华的无机化工产品。某同学在实验室制备氯气(Cl2),并用干燥纯净的氯气与 反应制备
反应制备 ,装置如图所示(部分夹持仪器已省略):
,装置如图所示(部分夹持仪器已省略):
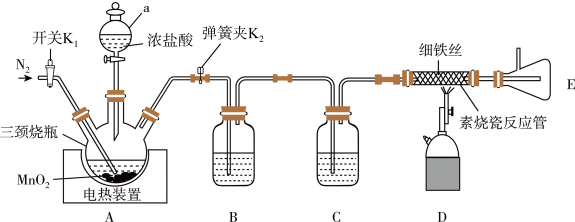
回答下列问题:
(1)仪器a的名称是___________ ,装置B、C装的试剂分别是___________ 、___________ 。
(2)写出三颈烧瓶中反应的离子方程式___________ 。
(3)实验开始前需要通入一段时间N2,其目的是___________ 。
(4)该装置存在的不足之处是___________ ,改进方法中需要用到的试剂为___________ 。
A.浓硫酸 B.无水CaCl2 C.无水硫酸铜 D.碱石灰
 反应制备
反应制备 ,装置如图所示(部分夹持仪器已省略):
,装置如图所示(部分夹持仪器已省略):
回答下列问题:
(1)仪器a的名称是
(2)写出三颈烧瓶中反应的离子方程式
(3)实验开始前需要通入一段时间N2,其目的是
(4)该装置存在的不足之处是
A.浓硫酸 B.无水CaCl2 C.无水硫酸铜 D.碱石灰
您最近一年使用:0次
2023-12-12更新
|
276次组卷
|
2卷引用:河南省周口市鹿邑县2023-2024学年高一上学期1月期末化学试题
名校
3 . 某小组为了探究硫酸的性质,设计如下实验:
回答下列问题:
(1)实验①没有明显现象的原因是___________ ;改变一个条件,为使实验①中的反应持续发生,改变条件是___________ 。
(2)为了引发实验②中的反应,宜采取的措施是___________ ;实验后,观察产物水溶液的颜色,其操作方法是___________ 。
(3)实验④产生的气体是___________ (填化学式),比较实验③和④可知,从氧化还原角度分析,H+的作用是___________ ;写出该反应的离子方程式:___________ 。
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为___________ ;M能与稀硫酸酸化的KI溶液反应生成白色沉淀CuI(碘化亚铜),在滤液中加入淀粉溶液,溶液变蓝色。写出M和稀硫酸酸化的KI溶液反应的离子方程式:___________ 。
| 序号 | 操作 | 现象 |
| ① | 常温下,在铁片中加入过量的浓硫酸 | 没有明显现象 |
| ② | 常温下,在铜片上加入过量的浓硫酸 | 没有明显现象 |
| ③ | 在铜和过量30%H2O2的混合溶液中加入Na2SO4溶液 | 没有明显现象 |
| ④ | 在铜和过量30%H2O2的混合溶液中加入稀硫酸 | 溶液变蓝色,并产生气泡 |
(1)实验①没有明显现象的原因是
(2)为了引发实验②中的反应,宜采取的措施是
(3)实验④产生的气体是
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为
您最近一年使用:0次
2023-10-22更新
|
73次组卷
|
4卷引用:河南省六市重点高中2024届高三上学期10月调研考试化学试题
4 . 为了研究化学反应能量变化情况,某同学设计了如图所示三种装置进行实验,忽略溶解过程的热效应,回答下列问题。

(1)若利用甲装置进行实验,当向装有铁屑的试管中滴加稀硫酸时,一段时间后观察到U形管中左端液面低于右端液面,说明该反应为______________ (填“放热”或“吸热”)反应,反应物的总能量比生成物的总能量______________ (填“高”或“低”),若试管中28g铁屑全部溶解,则产生的 在标准状况下的体积为
在标准状况下的体积为____________ L。
(2)若利用乙装置进行实验,试管内反应的化学方程式为__________________ ,一段时间后U形管中左端液面低于右端液面,________ (填“能”或“不能”)判断该反应的能量变化情况。
(3)若利用丙装置进行实验,滴加稀盐酸前,气囊适度鼓起,滴加稀盐酸后,试管内反应的离子方程式为________________________________________________ ,气囊体积会____________ (填“增大”或“减小”),原因是________________________________________________ 。

(1)若利用甲装置进行实验,当向装有铁屑的试管中滴加稀硫酸时,一段时间后观察到U形管中左端液面低于右端液面,说明该反应为
 在标准状况下的体积为
在标准状况下的体积为(2)若利用乙装置进行实验,试管内反应的化学方程式为
(3)若利用丙装置进行实验,滴加稀盐酸前,气囊适度鼓起,滴加稀盐酸后,试管内反应的离子方程式为
您最近一年使用:0次
名校
5 . “7•20”特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和ClO2等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理____ ,标况下56L氯气完全被吸收,需要____ L1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为_____ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论____ (填“同意”或“不同意”),若不同意,你认为的结论是____ (若同意,此空不用填)
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是_____ (从①②③中选填)。
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为_____ 。ClO2还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式_____ 。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为
您最近一年使用:0次
解题方法
6 . 已知 与硫的氧化物、氮的氧化物反应可以生成
与硫的氧化物、氮的氧化物反应可以生成 、NOCl、
、NOCl、 等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于
等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于 等有机溶剂。
等有机溶剂。
(1)NOCl中N元素的化合价为_______ ,N、O、Cl三种元素原子半径由大到小的顺序为_______ 。
(2)实验室制取的NOCl中常含有 ,除去
,除去 的方法为
的方法为_______ 。
(3)NOCl遇水生成一种氮的氧化物(该氧化物遇空气变红棕色),且只有一种元素的化合价发生改变,写出该反应的化学方程式:_______ 。
(4)NOCl与 同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:
同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:_______ 。反应中消耗1mol NOCl则转移电子的物质的量为_______ 。
(5) 可作为晶体的除水剂(反应生成两种酸性气体),写出
可作为晶体的除水剂(反应生成两种酸性气体),写出 与
与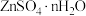 反应的化学方程式:
反应的化学方程式:_______ 。
 与硫的氧化物、氮的氧化物反应可以生成
与硫的氧化物、氮的氧化物反应可以生成 、NOCl、
、NOCl、 等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于
等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于 等有机溶剂。
等有机溶剂。(1)NOCl中N元素的化合价为
(2)实验室制取的NOCl中常含有
 ,除去
,除去 的方法为
的方法为(3)NOCl遇水生成一种氮的氧化物(该氧化物遇空气变红棕色),且只有一种元素的化合价发生改变,写出该反应的化学方程式:
(4)NOCl与
 同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:
同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:(5)
 可作为晶体的除水剂(反应生成两种酸性气体),写出
可作为晶体的除水剂(反应生成两种酸性气体),写出 与
与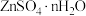 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
7 . 亚硫酸钠( )是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究
)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 的性质,进行了如下实验。
的性质,进行了如下实验。
【性质预测】
(1) 中硫元素的化合价是
中硫元素的化合价是_______ 价,属于S元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下, 被还原为
被还原为 。
。
【分析解释】
(2)实验i中,反应的离子方程式是_______ 。
【继续探究】
(3)甲同学认为实验ii的现象不能直接得出“ 具有氧化性”。
具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设a:酸性溶液中的 具有氧化性,可产生S;
具有氧化性,可产生S;
假设b:空气中存在 ,在酸性条件下,由于
,在酸性条件下,由于_______ (用离子方程式表示),可产生S;
假设c:酸性溶液中的 具有氧化性,可产生S。
具有氧化性,可产生S。
②设计实验iii证实了假设a和b不是产生S的主要原因。
实验iii:向 溶液中加入
溶液中加入_______ (填试剂名称),产生有臭鸡蛋气味的气体,溶液未变浑浊。
(4)结合实验ii和iii,用离子方程式解释实验ii中产生淡黄色浑浊的原因:_______ 。
 )是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究
)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 的性质,进行了如下实验。
的性质,进行了如下实验。【性质预测】
(1)
 中硫元素的化合价是
中硫元素的化合价是【实验验证】
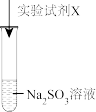 | 实验序号 | 实验试剂X | 实验现象 |
| i |  溶液、稀硫酸 溶液、稀硫酸 | 紫色褪去 | |
| ii |  溶液、稀硫酸 溶液、稀硫酸 | 加入 溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊 溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊 |
资料:酸性条件下,
 被还原为
被还原为 。
。【分析解释】
(2)实验i中,反应的离子方程式是
【继续探究】
(3)甲同学认为实验ii的现象不能直接得出“
 具有氧化性”。
具有氧化性”。①对淡黄色浑浊产生的原因作出如下假设:
假设a:酸性溶液中的
 具有氧化性,可产生S;
具有氧化性,可产生S;假设b:空气中存在
 ,在酸性条件下,由于
,在酸性条件下,由于假设c:酸性溶液中的
 具有氧化性,可产生S。
具有氧化性,可产生S。②设计实验iii证实了假设a和b不是产生S的主要原因。
实验iii:向
 溶液中加入
溶液中加入(4)结合实验ii和iii,用离子方程式解释实验ii中产生淡黄色浑浊的原因:
您最近一年使用:0次
8 . 物质的类别和元素的化合价是研究物质性质的两个重要角度。请根据如图所示信息,回答下列问题:

(1)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是_______ (填标号)。
a. b.
b. c.
c. d.
d.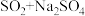
(2)Y可使品红溶液褪色,说明Y具有_______ 。
(3)图为铜丝与W的浓溶液反应并验证其产物性质的实验装置。

Ⅰ.想要立即终止①的反应,最恰当的方法是_______ (填标号)。
a.撤去酒精灯b.拔去橡胶塞倒出溶液c.上移铜丝,使其脱离溶液
将反应后试管①中的溶液慢慢倒入到水中,发生的变化是_______ 。
Ⅱ.装置④溶液中发生的离子反应方程式_______ 。
Ⅲ.反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式_______ 。

(1)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是a.
 b.
b. c.
c. d.
d.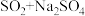
(2)Y可使品红溶液褪色,说明Y具有
(3)图为铜丝与W的浓溶液反应并验证其产物性质的实验装置。

Ⅰ.想要立即终止①的反应,最恰当的方法是
a.撤去酒精灯b.拔去橡胶塞倒出溶液c.上移铜丝,使其脱离溶液
将反应后试管①中的溶液慢慢倒入到水中,发生的变化是
Ⅱ.装置④溶液中发生的离子反应方程式
Ⅲ.反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式
您最近一年使用:0次
9 . 化学工作者经常从不同的角度来预测某些物质的性质,然后进行实验验证,得出结论。某化学研究小组根据H2O2中氧元素的化合价,预测H2O2具有氧化性和还原性,并设计如下实验进行验证。请根据实验室提供的试剂以及相关实验内容选择合适的化学试剂进行实验验证,并对主要的实验现象进行描述,写出相关反应的离子方程式。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性_______ 。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
| 验证H2O2的性质 | 选用的化学试剂 | 主要的实验现象 | 发生反应的离子方程式 |
| 还原性 | ① | ② | 略 |
| 氧化性 | ③ | ④ | ⑤ |
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性
您最近一年使用:0次
名校
10 . 物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”,根据图示回答下列问题:

(1)根据“价类二维图”,下列能与B反应的物质有_____ ,反应中使B表现还原性的物质是__ (填序号)。
①NaOH溶液 ②CaCl2溶液 ③酸性KMnO4溶液 ④H2S溶液
(2)C的钠盐放置在空气中极易变质,请设计实验方案证明其已被氧化___ 。
(3)请写出金属铜与D的浓溶液在一定条件下发生反应的化学方程式______ 。

(1)根据“价类二维图”,下列能与B反应的物质有
①NaOH溶液 ②CaCl2溶液 ③酸性KMnO4溶液 ④H2S溶液
(2)C的钠盐放置在空气中极易变质,请设计实验方案证明其已被氧化
(3)请写出金属铜与D的浓溶液在一定条件下发生反应的化学方程式
您最近一年使用:0次
2020-03-13更新
|
324次组卷
|
2卷引用:河南省郑州市2019-2020学年高一上学期期末考试化学试题



