1 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
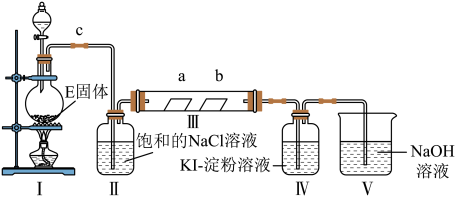
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)实验过程中,装置IV中的实验现象为___________ ;发生反应的化学方程式为___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___________ 装置(填序号),
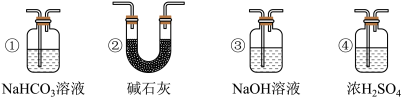
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___________ 。

(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是
(2)装置Ⅱ的作用是
(3)实验过程中,装置IV中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的

(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式
您最近一年使用:0次
解题方法
2 . 硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有 的硬质玻璃管;
的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。
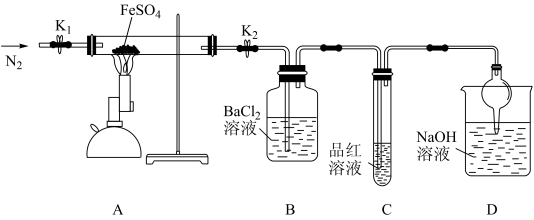
(1)根据B、C装置中的实验现象可推测分解产物中含有_______ 和_______ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的_______ (填“能”或“不能”),原因是_______ 。
(3)D装置中发生的主要反应的离子方程式是_______ 。
(4)通过计算确定剩余10.88g固体的成分,写出计算过程。______
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有
 的硬质玻璃管;
的硬质玻璃管;③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的离子方程式是
(4)通过计算确定剩余10.88g固体的成分,写出计算过程。
您最近一年使用:0次
解题方法
3 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验,请回答下列问题:

(1)制备氯气的化学方程式为___________ 。
(2)淀粉—KI溶液中观察到的现象是___________ ,反应的化学方程式为___________ 。
(3)若干燥的有色布条不褪色,潮湿的有色布条褪色,则说明___________ 。
(4)工业上常用廉价的石灰乳吸收氯气制得漂白粉。漂白粉溶于水后,遇到空气中CO2的,即产生漂白、杀菌作用,用化学方程式表示漂白粉的漂白原理___________ 。
(5)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(b、c、d、e中重合部分代表物质间反应,且氯水足量)。

①a过程的化学方程式___________ 。
②d过程所观察到的现象为___________ ;c过程证明了氯水中存在的微粒是___________ 。
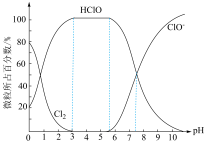
③已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、ClO三种微粒所占百分数与pH的关系如图,则用Cl2处理饮用水时,溶液的pH最佳控制范围是___________ 。
(6)实验室制取Cl2还可采用KMnO4与浓盐酸混合,其原理为: ,试回答下列问题:
,试回答下列问题:
①请用双线桥表示反应中电子转移:___________ ;
②反应中氧化剂与还原剂的物质的量之比___________ ,在标准状况下,当生成11.2LCl2时,被氧化的HCl的物质的量为___________ 。

(1)制备氯气的化学方程式为
(2)淀粉—KI溶液中观察到的现象是
(3)若干燥的有色布条不褪色,潮湿的有色布条褪色,则说明
(4)工业上常用廉价的石灰乳吸收氯气制得漂白粉。漂白粉溶于水后,遇到空气中CO2的,即产生漂白、杀菌作用,用化学方程式表示漂白粉的漂白原理
(5)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(b、c、d、e中重合部分代表物质间反应,且氯水足量)。

①a过程的化学方程式
②d过程所观察到的现象为
③已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、ClO三种微粒所占百分数与pH的关系如图,则用Cl2处理饮用水时,溶液的pH最佳控制范围是

(6)实验室制取Cl2还可采用KMnO4与浓盐酸混合,其原理为:
 ,试回答下列问题:
,试回答下列问题:①请用双线桥表示反应中电子转移:
②反应中氧化剂与还原剂的物质的量之比
您最近一年使用:0次
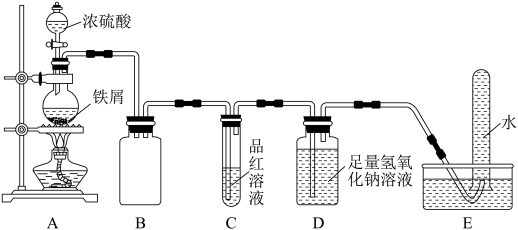
4 . 铁是人类使用量最大的一种金属。某学习小组在实验室利用如图所示装置进行过量铁屑与浓硫酸反应的实验,并检验产物。
查阅资料:常温下铁在浓硫酸中钝化,表面生成致密的 ,加热条件下,铁可以和浓硫酸反应。发生的反应有:
,加热条件下,铁可以和浓硫酸反应。发生的反应有:

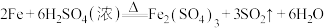
将铁屑放入圆底烧瓶,加入浓硫酸。开始时铁屑表面无明显变化,加热后铁屑表面开始产生大量气体,反应一段时间后铁屑表面气体减少直至反应停止。
(1)装置B的作用是_______ ,装置C的目的是_______ 。
(2)装置D中发生反应的离子方程式是_______ 。
(3)装置E中收集到一种无色无味的气体,此气体是_______ 。
(4)反应结束并待反应液冷却后,检验溶液中存在的金属阳离子。
方法1:取少量反应液于试管中,滴加NaOH溶液,溶液中先产生白色沉淀,然后变为灰绿色,最终变为红褐色沉淀。
方法2:取少量反应液于试管中,_______ (写出详细的实验方案、现象和结论,可以选用 的试剂有新制氯水、酸性高锰酸钾溶液,硫氰化钾溶液)。
(5)某实验小组制备了一定质量的 (含FeO杂质)样品,为测定其中
(含FeO杂质)样品,为测定其中 的质量分数,现进行如下实验:
的质量分数,现进行如下实验:
步骤1:称取0.20g样品,向样品中加入足量的盐酸使其完全溶解。
步骤2:向溶液中加入足量的KI溶液,充分反应。
步骤3:向溶液中加入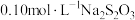 溶液,恰好完全反应时消耗
溶液,恰好完全反应时消耗 溶液体积为20.00mL生成
溶液体积为20.00mL生成 。
。
反应中发生的离子方程式为: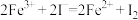
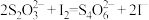
计算样品中所含 的质量分数
的质量分数_____ 。(写出计算过程)

查阅资料:常温下铁在浓硫酸中钝化,表面生成致密的
 ,加热条件下,铁可以和浓硫酸反应。发生的反应有:
,加热条件下,铁可以和浓硫酸反应。发生的反应有:
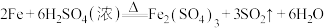
将铁屑放入圆底烧瓶,加入浓硫酸。开始时铁屑表面无明显变化,加热后铁屑表面开始产生大量气体,反应一段时间后铁屑表面气体减少直至反应停止。
(1)装置B的作用是
(2)装置D中发生反应的离子方程式是
(3)装置E中收集到一种无色无味的气体,此气体是
(4)反应结束并待反应液冷却后,检验溶液中存在的金属阳离子。
方法1:取少量反应液于试管中,滴加NaOH溶液,溶液中先产生白色沉淀,然后变为灰绿色,最终变为红褐色沉淀。
方法2:取少量反应液于试管中,
(5)某实验小组制备了一定质量的
 (含FeO杂质)样品,为测定其中
(含FeO杂质)样品,为测定其中 的质量分数,现进行如下实验:
的质量分数,现进行如下实验:步骤1:称取0.20g样品,向样品中加入足量的盐酸使其完全溶解。
步骤2:向溶液中加入足量的KI溶液,充分反应。
步骤3:向溶液中加入
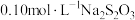 溶液,恰好完全反应时消耗
溶液,恰好完全反应时消耗 溶液体积为20.00mL生成
溶液体积为20.00mL生成 。
。反应中发生的离子方程式为:
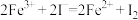
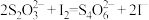
计算样品中所含
 的质量分数
的质量分数
您最近一年使用:0次
名校
解题方法
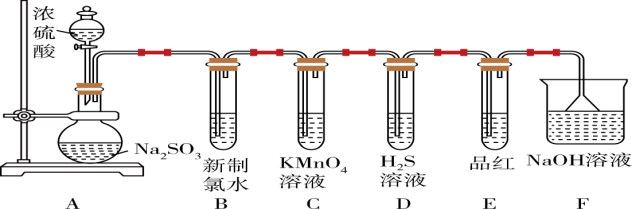
5 . 某化学兴趣小组为制备并探究 的性质,按下图所示装置进行实验。
的性质,按下图所示装置进行实验。
已知: (浓)
(浓)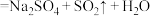
(1)装置A中盛放浓硫酸的仪器名称是_______ 。
(2)装置B中发生反应后的酸性将_______ (填“增强”、“不变”或“减弱”)。
(3)装置C中现象为_______ 。
(4)装置E目的是探究 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象_______ 。
(5)装置F中发生反应的离子方程式为_______ 。
 的性质,按下图所示装置进行实验。
的性质,按下图所示装置进行实验。
已知:
 (浓)
(浓)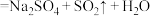
(1)装置A中盛放浓硫酸的仪器名称是
(2)装置B中发生反应后的酸性将
(3)装置C中现象为
(4)装置E目的是探究
 与品红作用的可逆性,请写出实验操作及现象
与品红作用的可逆性,请写出实验操作及现象(5)装置F中发生反应的离子方程式为
您最近一年使用:0次
名校
6 . 某化学学习小组欲探究铁及其化合物的氧化性和还原性,请协助他们完成实验报告。
实验目的:探究铁及其化合物的氧化性和还原性
实验设计及仪器:FeCl2溶液、FeCl3溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸、胶头滴管、试管
(1)实验记录(仿照①实验作答,填写划线部分)
(2)学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是____ (填写选项字母)。
(3)在实验②中,有部分同学在氯化亚铁溶液中滴入硫氰化钾溶液后出现血红色,你认为是什么原因____ ,你对实验员在配制氯化亚铁溶液时提出的建议是____ 。
(4)在配制氯化铁溶液时,含有少量Fe2+,为检验少量Fe2+的存在,请从下列物质中选择合适的试剂____ (填写选项字母)
A.AgNO3溶液 B.稀盐酸 C.KMnO4溶液
实验目的:探究铁及其化合物的氧化性和还原性
实验设计及仪器:FeCl2溶液、FeCl3溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸、胶头滴管、试管
(1)实验记录(仿照①实验作答,填写划线部分)
| 序号 | 实验设计 | 实验现象 | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变为浅绿色,生成无色无味气体 | Fe+2H+=Fe2++H2↑ | Fe具有还原性 |
| ② | FeCl2溶液中滴入KSCN溶液再加氯水 | 滴入KSCN溶液无明显变化,加入氯水立即变成血红色 | I | II |
| ③ | FeCl2溶液中加入锌片 | 锌片溶解,溶液的浅绿色逐渐褪去 | Zn+Fe2+=Zn2++Fe | III |
| ④ | IV | 铜片溶解且溶液的血红色逐渐褪去 | V | Fe3+具有氧化性 |
| A.Cl2 | B.Na | C.Mg2+ | D.H2O2 |
(4)在配制氯化铁溶液时,含有少量Fe2+,为检验少量Fe2+的存在,请从下列物质中选择合适的试剂
A.AgNO3溶液 B.稀盐酸 C.KMnO4溶液
您最近一年使用:0次
7 . 下列制取SO2、验证其性质的装置(尾气处理装置已省略)和原理不能达到实验目的的是( )
A.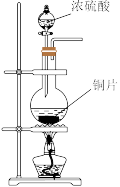 制取SO2 制取SO2 | B.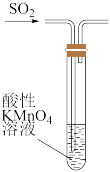 验证漂白性 验证漂白性 |
C. 验证还原性 验证还原性 | D.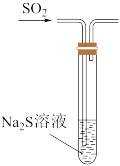 验证氧化性 验证氧化性 |
您最近一年使用:0次
2019-03-28更新
|
1322次组卷
|
13卷引用:江苏省句容市2022-2023学年高一上学期期末考试化学试题
江苏省句容市2022-2023学年高一上学期期末考试化学试题【市级联考】江苏省苏锡常镇四市2019届高三下学期第二次模拟考试化学试题江苏省镇江市2020届高三上学期期末考试化学试题江苏省南京市六校联合体2021届高三上学期11月联考化学试题江苏省南京市第一中学2021届高三年级上学期10月月考化学试题浙江省温丽地区2019-2020学年高三第一学期第一次联考化学试题2019-2020学年新人教版必修2第5章第1节《硫及其化合物》作业(已下线)3.2.2 硫酸 酸雨及其防治练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)天津一中2020届高三第二次月考化学试题天津市耀华中学2021届高三第二次月考化学试题新疆乌鲁木齐市第二十中学2020-2021学年高一上学期期末考试化学试题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练内蒙古自治区乌海市第一中学2023-2024学年高一下学期4月第一次月考化学试题
解题方法
8 . 回答下列问题。
Ⅰ.某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
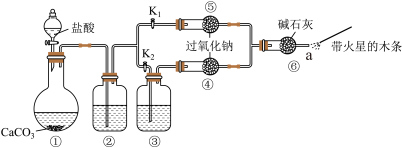
【装置分析】
(1)装置①中装盐酸的仪器叫___________ 。
(2)装置②中的试剂是___________ ,②中反应的化学方程式是___________ 。
(3)装置③中的试剂是___________ 。
【进行实验】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是___________ 、___________ 。
(5)过氧化钠跟二氧化碳反应的化学方程式:___________ 。
Ⅱ.欲探究Na2CO3和NaHCO3稳定性的相对强弱,两同学分别设计以下两组装置:

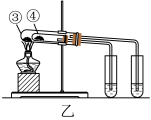
请回答:
(6)如甲图所示,分别用Na2CO3和NaHCO3做实验,试管②中的试剂是___________ (填字母)。
a.稀H2SO4 b.NaOH溶液 c.Ca(OH)2溶液
试管①中发生反应的化学方程式是___________ 。
(7)如乙图所示,试管④中装入的固体应该是___________ (填化学式)。
(8)通过上述实验,得出的结论是:Na2CO3比NaHCO3的稳定性___________ (填“强”或“弱”)。
Ⅰ.某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。

【装置分析】
(1)装置①中装盐酸的仪器叫
(2)装置②中的试剂是
(3)装置③中的试剂是
【进行实验】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
(5)过氧化钠跟二氧化碳反应的化学方程式:
Ⅱ.欲探究Na2CO3和NaHCO3稳定性的相对强弱,两同学分别设计以下两组装置:


请回答:
(6)如甲图所示,分别用Na2CO3和NaHCO3做实验,试管②中的试剂是
a.稀H2SO4 b.NaOH溶液 c.Ca(OH)2溶液
试管①中发生反应的化学方程式是
(7)如乙图所示,试管④中装入的固体应该是
(8)通过上述实验,得出的结论是:Na2CO3比NaHCO3的稳定性
您最近一年使用:0次
9 . 焦亚硫酸钠 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。
化学兴趣小组同学利用图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取 并探究
并探究 的性质。
的性质。
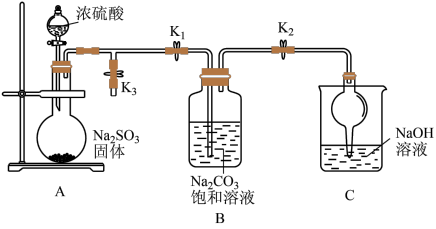
Ⅰ.打开 和
和 ,关闭
,关闭 ,制取
,制取 。
。
(1) 中O元素化合价为-2,其中S的化合价为
中O元素化合价为-2,其中S的化合价为___________ 。
(2)装置A中所发生反应的化学方程式为___________ ,装置C的作用是___________ 。
(3)B中通入过量 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应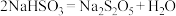 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为___________ 。
(4)B中所得 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有___________ 。
(5)装置C反应后烧杯中含有 和
和 ,验证该溶液中含有
,验证该溶液中含有 溶液的方法:取少量溶液,滴加足量的稀硫酸,
溶液的方法:取少量溶液,滴加足量的稀硫酸,___________ 。
Ⅱ.更换B瓶中的溶液,探究的性质。
(6)将B中溶液更换为品红的乙醇溶液,无明显现象,而将 通入品红的水溶液中,溶液褪色。可推知,
通入品红的水溶液中,溶液褪色。可推知,___________ 不能使品红褪色。
 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。化学兴趣小组同学利用图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取
 并探究
并探究 的性质。
的性质。
Ⅰ.打开
 和
和 ,关闭
,关闭 ,制取
,制取 。
。(1)
 中O元素化合价为-2,其中S的化合价为
中O元素化合价为-2,其中S的化合价为(2)装置A中所发生反应的化学方程式为
(3)B中通入过量
 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应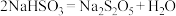 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为(4)B中所得
 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有(5)装置C反应后烧杯中含有
 和
和 ,验证该溶液中含有
,验证该溶液中含有 溶液的方法:取少量溶液,滴加足量的稀硫酸,
溶液的方法:取少量溶液,滴加足量的稀硫酸,Ⅱ.更换B瓶中的溶液,探究的性质。
(6)将B中溶液更换为品红的乙醇溶液,无明显现象,而将
 通入品红的水溶液中,溶液褪色。可推知,
通入品红的水溶液中,溶液褪色。可推知,
您最近一年使用:0次
2023-04-30更新
|
129次组卷
|
2卷引用:江苏省高邮市第一中学2022-2023学年高一上学期第三次阶段测试化学试题
10 . 甲、乙两同学欲验证乙醇的性质,现做如下实验:
I. 甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):
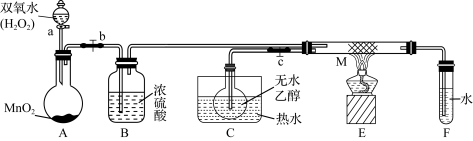
其实验操作:先按上图安装好,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
(1)A中发生反应的化学方程式为___________ , B的作用是___________ ;C中热水的作用是___________ 。
(2)M处发生反应的化学方程式为___________ 。
(3)从M管中可观察到的现象是___________ 。从中可认识到该实验过程中催化剂___________ (填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的___________ 。
(4)实验一段时间后,如果撤掉酒精灯,反应___________ (填“能”或“不能”)继续进行,其原因是___________ 。
II. 乙同学进行乙醇的沸点测定实验,装置如图所示,回答下列问题:

(5)盛乙醇的试管应浸入水浴中,水浴的温度应保持在___________(填字母)。
(6)测乙醇沸点时不把整个试管浸在水里的原因是___________ ;塞子豁口的作用是___________ 。
I. 甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):

其实验操作:先按上图安装好,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
(1)A中发生反应的化学方程式为
(2)M处发生反应的化学方程式为
(3)从M管中可观察到的现象是
(4)实验一段时间后,如果撤掉酒精灯,反应
II. 乙同学进行乙醇的沸点测定实验,装置如图所示,回答下列问题:

(5)盛乙醇的试管应浸入水浴中,水浴的温度应保持在___________(填字母)。
| A.100 ℃ | B.78.5 ℃ | C.80 ℃ | D.50 ℃ |
您最近一年使用:0次



