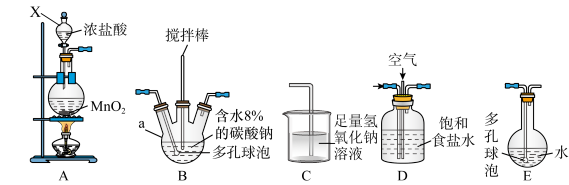
1 . 某校化学兴趣小组为研究氯气的性质,设计用如图所示的装置进行实验,其中a为干燥的红色试纸,b为湿润的红色试纸。

回答下列问题:
(1)装置I中仪器c的名称是______ ,实验室用二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置V的作用是_______ 。
(3)若产生的 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是________ 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置________ (填序号)。

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为_________ 。

回答下列问题:
(1)装置I中仪器c的名称是
(2)装置V的作用是
(3)若产生的
 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为
您最近一年使用:0次
名校
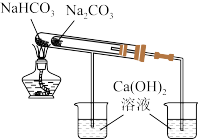
2 . 氧化二氯(Cl2O)是次氯酸的酸酐,在实验室中以  和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备
和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备  并用水吸收制备次氯酸溶液(装置如图所示)。
并用水吸收制备次氯酸溶液(装置如图所示)。
已知:①常温下, 是棕黄色、有刺激性气味的气体,熔点是-120.6℃ ,沸点是3.8℃,42℃以上分解生成
是棕黄色、有刺激性气味的气体,熔点是-120.6℃ ,沸点是3.8℃,42℃以上分解生成  和
和  易溶于水并与水反应生成
易溶于水并与水反应生成  O。
O。
②实验室制备原理:
回答下列问题:
(1)装置A中仪器X的名称为_______ 。
(2)若气体从左至右流动,装置的连接顺序是A→_______ (每个装置限用一次)。
(3)实验过程中,装置B需放在冷水中,其目的是_______ ;装置B和E中使用多孔球泡的优点是_______ 。
(4)实验中控制氯气与空气的体积比的方法是_______ 。
(5)装置E中采用棕色圆底烧瓶是因为_______ 。
(6)实验完成后取C中烧杯内溶液滴加品红溶液发现溶液褪色。该课题组设计实验探究溶液褪色的原因。
①a=_______
②由上述实验得出的结论是_______ 。
 和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备
和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备  并用水吸收制备次氯酸溶液(装置如图所示)。
并用水吸收制备次氯酸溶液(装置如图所示)。
已知:①常温下,
 是棕黄色、有刺激性气味的气体,熔点是-120.6℃ ,沸点是3.8℃,42℃以上分解生成
是棕黄色、有刺激性气味的气体,熔点是-120.6℃ ,沸点是3.8℃,42℃以上分解生成  和
和  易溶于水并与水反应生成
易溶于水并与水反应生成  O。
O。②实验室制备原理:

回答下列问题:
(1)装置A中仪器X的名称为
(2)若气体从左至右流动,装置的连接顺序是A→
(3)实验过程中,装置B需放在冷水中,其目的是
(4)实验中控制氯气与空气的体积比的方法是
(5)装置E中采用棕色圆底烧瓶是因为
(6)实验完成后取C中烧杯内溶液滴加品红溶液发现溶液褪色。该课题组设计实验探究溶液褪色的原因。
| 序号 | 0.1mol:L-1NaClO溶液/mL | 0.1mol·L-1NaCl溶液/mL | 0.1mol:L-1NaOH溶液/mL | H₂O/mL | 品红溶液 | 现象 |
| I | 5.0 | 0 | 0 | 5.0 | 3滴 | 较快褪色 |
| Ⅱ | 0 | 5.0 | a | 0 | 3滴 | 不褪色 |
| Ⅲ | 5.0 | 0 | 5.0 | 0 | 3滴 | 缓慢褪色 |
②由上述实验得出的结论是
您最近一年使用:0次
解题方法
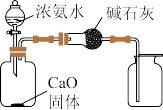
3 . 氯化亚铜(CuCl) 为白色粉末,其露置于空气中易被氧化为绿色的碱式氯化铜Cu2(OH)3Cl]。某兴趣小组高温加热分解氯化铜晶体(CuCl2·xH 2O)制备CuCl,其装置如下(加热仪器、夹持仪器省略)

回答下列问题:
(1)装有无水硫酸铜的仪器名称为______ ,装置 D 的作用是______ 。
(2)通入 HCl 气体的主要作用是______ 。
(3)实验过程中,装置C 中的现象为______ 。
(4)硬质玻璃管A 中发生主要反应的化学方程式为__________ 。
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=______ (精确到 0.1)。
②若加热时有固体溅出坩埚,则测得x 值______ 填“偏大”“不变”或“偏小”)。

回答下列问题:
(1)装有无水硫酸铜的仪器名称为
(2)通入 HCl 气体的主要作用是
(3)实验过程中,装置C 中的现象为
(4)硬质玻璃管A 中发生主要反应的化学方程式为
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=
②若加热时有固体溅出坩埚,则测得x 值
您最近一年使用:0次
2020-05-25更新
|
132次组卷
|
3卷引用:贵州省黔西南州兴义市义龙新区2021-2022高三上学期期末考试化学试题
4 . 实验是学习化学的重要途径。下列装置或操作能达到实验目的的是
A | B | C | D |
|
|
|
|
比较 和 和 的热稳定性 的热稳定性 | 验证浓硫酸的脱水性、强氧化性 的漂白性、还原性 的漂白性、还原性 | 制取并收集干燥纯净的 | 用氢氧化钠标准液测定盐酸的浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-29更新
|
138次组卷
|
2卷引用:贵州省黔东南苗族侗族自治州)2021-2022学年高二下学期期末联考化学试题
解题方法
5 . 目前,大气颗粒物的研究工作成为全国科技界关注的焦点。气溶胶中的有机酸(HCOOH,CH3COOH,HOOCCOOH)对于大气辐射强迫、能见度、气候变化等都有着重要的影响。
(1)区别溶液和胶体的实验步骤:__________
(2)草酸受热易分解,某小组对草酸受热分解产物进行探究:
①【猜想与假设】猜想1:分解产物是CO2、H2O
猜想2:分解产物是CO、H2O
猜想3:分解产物是CO2、CO
猜想4:分解产物是CO2、CO和H2O
根据质量守恒定律,以上猜想中,不可能的猜想是_______ 。
②同学按照如图装置观察到无水CuSO4变蓝,生成气体可燃烧,燃烧后能使澄清石灰水变浑浊,由此写出草酸分解的化学方程式_______ 。

(3)①人体血液含Ca2+。现抽取某人血样10mL,稀释后用草酸铵[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙(CaC2O4)沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解得到草酸(H2C2O4)溶液,用2.5×10-3 mol/LKMnO4溶液滴定得到的草酸至终点,共耗去2.0mLKMnO4溶液由上述实验数据可求得此人血液中Ca2+的物质的量浓度为_______ 。(提示:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)
②KMnO4溶液滴定得到的草酸至终点时的实验现象_______ 。
③用0.01mol/LNaOH与0.01mol/L草酸溶液等体积混合,当溶液呈中性时,混合液离子浓度从大到小顺序:_______ 。
(4)草酸电离方程式如下:H2C2O4 H++HC2O
H++HC2O ,请写出草酸的电离平衡常数表达式:
,请写出草酸的电离平衡常数表达式:_______ 。
(1)区别溶液和胶体的实验步骤:
(2)草酸受热易分解,某小组对草酸受热分解产物进行探究:
①【猜想与假设】猜想1:分解产物是CO2、H2O
猜想2:分解产物是CO、H2O
猜想3:分解产物是CO2、CO
猜想4:分解产物是CO2、CO和H2O
根据质量守恒定律,以上猜想中,不可能的猜想是
②同学按照如图装置观察到无水CuSO4变蓝,生成气体可燃烧,燃烧后能使澄清石灰水变浑浊,由此写出草酸分解的化学方程式

(3)①人体血液含Ca2+。现抽取某人血样10mL,稀释后用草酸铵[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙(CaC2O4)沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解得到草酸(H2C2O4)溶液,用2.5×10-3 mol/LKMnO4溶液滴定得到的草酸至终点,共耗去2.0mLKMnO4溶液由上述实验数据可求得此人血液中Ca2+的物质的量浓度为
②KMnO4溶液滴定得到的草酸至终点时的实验现象
③用0.01mol/LNaOH与0.01mol/L草酸溶液等体积混合,当溶液呈中性时,混合液离子浓度从大到小顺序:
(4)草酸电离方程式如下:H2C2O4
 H++HC2O
H++HC2O ,请写出草酸的电离平衡常数表达式:
,请写出草酸的电离平衡常数表达式:
您最近一年使用:0次
名校
解题方法
6 . 某同学根据Mg与 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,他设计了如图所示装置进行实验(已知
中燃烧,为了确定其产物,他设计了如图所示装置进行实验(已知 能被CO还原得到黑色的金属Pd)。
能被CO还原得到黑色的金属Pd)。
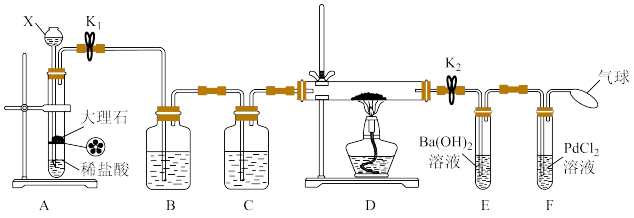
按如下顺序进行实验操作:
①打开 和
和 ,通入
,通入 待E中溶液变浑浊时,再点燃酒精灯;
待E中溶液变浑浊时,再点燃酒精灯;
②待金属钠完全燃烧后熄灭酒精灯,并冷却至室温;
③关闭 和
和 。
。
回答下列问题:
(1)仪器X的名称是___________ 。
(2)装置B中的试剂是___________ ,作用是___________ 。
(3)步骤①的目的是_______ ;若直接点燃酒精灯,反应中可能会生成一种淡黄色固体,写出这种固体与水反应的化学方程式:___________ 。
(4)点燃酒精灯后,观察到钠块表面变黑,熔融成金属小球,然后金属钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体(一种盐类物质)产生,一段时间后F中试管内壁也有黑色沉淀产生。
上述现象说明金属钠在 中燃烧的产物为
中燃烧的产物为___________ (填化学式);体现了金属钠的___________ (填物理性质)和___________ (填“氧化性”或“还原性”)。
 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,他设计了如图所示装置进行实验(已知
中燃烧,为了确定其产物,他设计了如图所示装置进行实验(已知 能被CO还原得到黑色的金属Pd)。
能被CO还原得到黑色的金属Pd)。
按如下顺序进行实验操作:
①打开
 和
和 ,通入
,通入 待E中溶液变浑浊时,再点燃酒精灯;
待E中溶液变浑浊时,再点燃酒精灯;②待金属钠完全燃烧后熄灭酒精灯,并冷却至室温;
③关闭
 和
和 。
。回答下列问题:
(1)仪器X的名称是
(2)装置B中的试剂是
(3)步骤①的目的是
(4)点燃酒精灯后,观察到钠块表面变黑,熔融成金属小球,然后金属钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体(一种盐类物质)产生,一段时间后F中试管内壁也有黑色沉淀产生。
上述现象说明金属钠在
 中燃烧的产物为
中燃烧的产物为
您最近一年使用:0次
解题方法
7 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题。
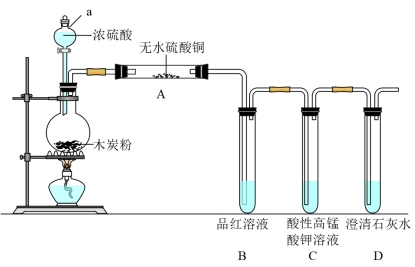
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式_______ 。
(2)仪器a的名称是_______ 。
(3)装置A中出现_______ 现象,证明气体产物中有 。
。
(4)C装置作用是_______ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)仪器a的名称是
(3)装置A中出现
 。
。(4)C装置作用是
您最近一年使用:0次
2022-04-15更新
|
978次组卷
|
4卷引用:贵州省“三新”改革联盟校2021-2022学年高一下学期联考试题(三) 化学试题
解题方法
8 . 某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应。
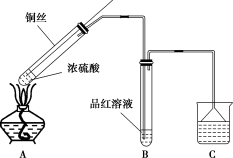
回答下列问题:
(1)铜与浓硫酸反应的化学方程式为___ 。
(2)B中观察到的现象为___ 。
(3)C中应加入的试剂为___ ,倒置漏斗的作用是___ 。
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是___ 。

回答下列问题:
(1)铜与浓硫酸反应的化学方程式为
(2)B中观察到的现象为
(3)C中应加入的试剂为
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是
您最近一年使用:0次
2021-05-26更新
|
264次组卷
|
4卷引用:贵州省黔西南州同源中学2021-2022学年高一下学期第一次月考化学试题
解题方法
9 . 为探究铜与稀硝酸反应的气体产物及亚硝酸对其反应速率的影响,进行如下实验。
实验一 探究铜与稀硝酸反应的气体产物实验装置如图所示,气密性已检查。

已知: ,该反应较缓慢,待生成一定量
,该反应较缓慢,待生成一定量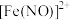 时突显明显棕色。
时突显明显棕色。
(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是___________ 。
(2)若装置 A中有 NO2气体生成,则装置 B中的实验现象为___________ 。
(3)若装置A中铜与稀硝酸反应只生成 NO气体,写出该反应的离子方程式___________ ,装置B中的实验现象为___________ 。
实验二 实验一的过程中发现铜与稀硝酸反应比较慢,A中产生无色气体。查阅文献得知铜与浓 HNO3反应一旦发生就变快,是因为开始生成的 NO2溶于水形成 HNO2(弱酸,不稳定),使反应加快。为了探究 HNO2对铜与稀硝酸反应速率的影响,采用实验一的实验装置和操作,设计了如下实验。
(4)已知NO2与 H2O反应生成 HNO2和另一种常见的强酸,写出其反应的化学方程式___________ 。
(5)上述实验②中加入1.0g NaNO2固体的作用是___________ 。
(6)实验测得 t1>t2,可得出的结论是___________ 。
实验一 探究铜与稀硝酸反应的气体产物实验装置如图所示,气密性已检查。

已知:
 ,该反应较缓慢,待生成一定量
,该反应较缓慢,待生成一定量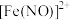 时突显明显棕色。
时突显明显棕色。(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是
(2)若装置 A中有 NO2气体生成,则装置 B中的实验现象为
(3)若装置A中铜与稀硝酸反应只生成 NO气体,写出该反应的离子方程式
实验二 实验一的过程中发现铜与稀硝酸反应比较慢,A中产生无色气体。查阅文献得知铜与浓 HNO3反应一旦发生就变快,是因为开始生成的 NO2溶于水形成 HNO2(弱酸,不稳定),使反应加快。为了探究 HNO2对铜与稀硝酸反应速率的影响,采用实验一的实验装置和操作,设计了如下实验。
| 实验序号 | 温度(℃) | 6mol/L硝酸(mL) | 铜片(g) | NaNO2(g) | B中溶液变色的时间(s) |
| ① | 25 | 20 | 5 | 0 | t1 |
| ② | 25 | 20 | 5 | 1.0 | t2 |
(5)上述实验②中加入1.0g NaNO2固体的作用是
(6)实验测得 t1>t2,可得出的结论是
您最近一年使用:0次
2021-03-04更新
|
754次组卷
|
5卷引用:贵州省思南县梵净山中学2022-2023学年高三上学期11月月考化学试题
贵州省思南县梵净山中学2022-2023学年高三上学期11月月考化学试题广东省梅州市2021届高三一模化学试卷广东省梅州市2021届高三下学期3月总复习质检化学试题(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)
10 . 某兴趣小组为丰富课本所学的SO2性质,设计了下列系列实验:
(1)用下图装置制取并收集SO2以验证其氧化性
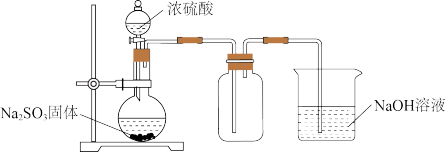
①Na2SO3久置于空气中易变质,体现了Na2SO3具有___________ 性。
②烧杯中NaOH溶液的作用是___________ 。
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为___________ 。
(2)用下图装置验证H2SO3比H2CO3酸性强
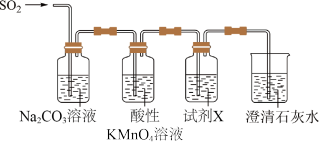
①试剂X是___________ ,其作用是___________ 。
②当观察到___________ ,即证明H2SO3比H2CO3酸性强。
(1)用下图装置制取并收集SO2以验证其氧化性

①Na2SO3久置于空气中易变质,体现了Na2SO3具有
②烧杯中NaOH溶液的作用是
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为
(2)用下图装置验证H2SO3比H2CO3酸性强

①试剂X是
②当观察到
您最近一年使用:0次
2020-12-17更新
|
503次组卷
|
4卷引用:贵州省六盘水市六枝特区2021-2022学年高一下学期期中教学质量检测化学试题