解题方法
1 . 某研究小组为探究 气体通入
气体通入 溶液的反应中产生白色沉淀的原因,设计了如下图实验:
溶液的反应中产生白色沉淀的原因,设计了如下图实验: 反应的化学方程式
反应的化学方程式___________ ;实验装置中缓冲瓶的作用是___________ 。
(2)小组同学通过分析认为白色沉淀是 ,然后对反应中起氧化作用的是何种物质进行了实验探究。向实验装置的烧杯中分别放入不同组成的溶液,进行多次实验。请补充表格中的实验步骤:
,然后对反应中起氧化作用的是何种物质进行了实验探究。向实验装置的烧杯中分别放入不同组成的溶液,进行多次实验。请补充表格中的实验步骤:
写出实验②中发生反应的离子方程式:___________ 。
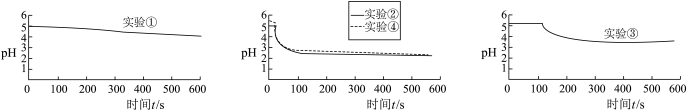
(3)上述4组实验中pH传感器得到的部分图像如下:___________ 。
②对比实验③、④的图像,依据___________ ,说明 在氧化反应中起到主要氧化作用。
在氧化反应中起到主要氧化作用。
③对比实验②④的pH变化情况,说明 对氧化反应
对氧化反应___________ (填“有影响”或“无影响”或“无法判断”)。
 气体通入
气体通入 溶液的反应中产生白色沉淀的原因,设计了如下图实验:
溶液的反应中产生白色沉淀的原因,设计了如下图实验: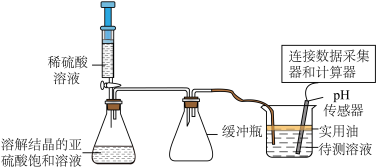
 反应的化学方程式
反应的化学方程式(2)小组同学通过分析认为白色沉淀是
 ,然后对反应中起氧化作用的是何种物质进行了实验探究。向实验装置的烧杯中分别放入不同组成的溶液,进行多次实验。请补充表格中的实验步骤:
,然后对反应中起氧化作用的是何种物质进行了实验探究。向实验装置的烧杯中分别放入不同组成的溶液,进行多次实验。请补充表格中的实验步骤:| 实验步骤 | 实验现象 |
①烧杯中加入煮沸的 溶液25mL,再加入25mL食用油,冷却至室温 溶液25mL,再加入25mL食用油,冷却至室温 | 无明显现象 |
| ②烧杯中加入未煮沸的 | 出现轻微浑浊 |
| ③烧杯中加入煮沸的 | 出现浑浊 |
④加入未煮沸的 溶液25mL 溶液25mL | 出现浑浊 |
(3)上述4组实验中pH传感器得到的部分图像如下:
②对比实验③、④的图像,依据
 在氧化反应中起到主要氧化作用。
在氧化反应中起到主要氧化作用。③对比实验②④的pH变化情况,说明
 对氧化反应
对氧化反应
您最近一年使用:0次
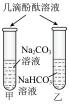
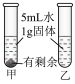
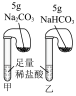
2 . 如图是某兴趣小组设计的验证 与
与 性质实验。下列说法错误的是
性质实验。下列说法错误的是
 与
与 性质实验。下列说法错误的是
性质实验。下列说法错误的是| 选项 | A | B | C | D |
| 实验装置 |
|
|
|
|
| 实验结论 | 溶液均呈红色甲、乙两试管中 | 甲装置中是 | 乙装置中气球膨胀的更大 | 烧杯乙中澄清石灰水变浑浊 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-15更新
|
131次组卷
|
2卷引用:安徽省淮南第四中学2023-2024学年高一上学期第二次段考化学试题
名校
3 . 在实验室里,某同学取一小块金属钠做钠与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是___________ ,所发生反应的化学方程式是___________ 。
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①___________ ,②___________ 。
(3)将一块绿豆粒大小的钠投入到滴加了石蕊试剂的水中,不可能观察到的现象是___________。
(4)根据上述实验过程中钠所发生的有关变化,试说明金属钠保存在煤油中的目的是___________ 。
(1)切开的金属钠暴露在空气中,最先观察到的现象是
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①
(3)将一块绿豆粒大小的钠投入到滴加了石蕊试剂的水中,不可能观察到的现象是___________。
| A.钠熔化成小球并在液面上游动 | B.发出“嘶嘶”声响 |
| C.小球最后消失 | D.溶液最后变红 |
您最近一年使用:0次
2023-12-31更新
|
72次组卷
|
2卷引用:安徽省芜湖市无为襄安中学2023-2024学年高一上学期11月期中化学试题
名校
4 . 1841年美国学者Fremy首次合成了 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。
实验(一)制备 ,装置如图所示:
,装置如图所示:___________ 。
(2)甲装置中副产物为氯化钾,写出生成 的离子方程式:
的离子方程式:___________ ,实验完毕后,对甲装置中混合液进行___________ 过滤、洗涤、低温干燥。
实验(二)探究 性质及应用。
性质及应用。
取10g草酸溶于40mL水中,加入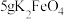 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有 ,经测定所得气体中还含有
,经测定所得气体中还含有 。
。
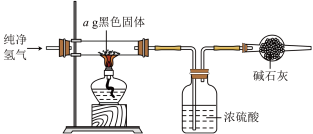
(3)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分,当黑色固体完全反应后,测得浓硫酸质量净增bg,当 等于
等于___________ (用最简分数比表示)时,黑色固体为 。
。 稳定性(用
稳定性(用 浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:
浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:___________ 。
②在相同条件下, 作消毒剂最佳温度是
作消毒剂最佳温度是___________ 。
(5)查阅资料可知, 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
方案1:在 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。
方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。___________ (填“1”或“2”)能证明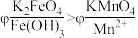 ,石墨极的电极反应式为
,石墨极的电极反应式为___________ 。
 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。实验(一)制备
 ,装置如图所示:
,装置如图所示: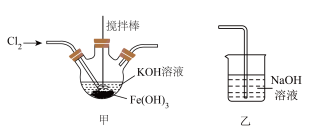
(2)甲装置中副产物为氯化钾,写出生成
 的离子方程式:
的离子方程式:实验(二)探究
 性质及应用。
性质及应用。取10g草酸溶于40mL水中,加入
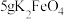 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有 ,经测定所得气体中还含有
,经测定所得气体中还含有 。
。(3)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分,当黑色固体完全反应后,测得浓硫酸质量净增bg,当
 等于
等于 。
。
 稳定性(用
稳定性(用 浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:
浓度表示)与pH关系如图,其消毒效率与温度关系如图所示: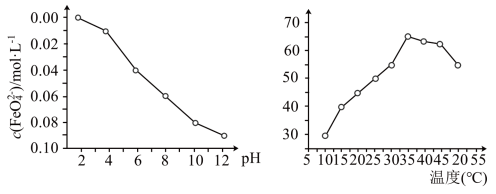
②在相同条件下,
 作消毒剂最佳温度是
作消毒剂最佳温度是(5)查阅资料可知,
 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)方案1:在
 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。
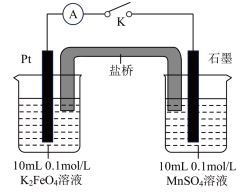
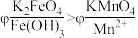 ,石墨极的电极反应式为
,石墨极的电极反应式为
您最近一年使用:0次
解题方法
5 . 某课外小组的同学利用如图所示装置制备SO2,并探究SO2的部分性质。
(1)仪器组装完毕后,必须进行的实验操作是___________ 。
(2)试剂1最好选择___________ (填标号)。
(3)实验过程中,装置Ⅱ中的实验现象为___________ ,SO2体现的化学性质为___________ (填“氧化性”或“还原性”)。
(4)某同学预测装置Ⅲ 中不会产生白色沉淀,随着实验的进行,装置Ⅲ 中产生了少量白色沉淀,该白色沉淀的化学式为___________ ,产生该白色沉淀的可能原因为___________ 。
(5)为测定空气中的SO2含量,实验小组将空气样品经过管道通入密闭容器中的100 mL 0.2000 mol/L的酸性KMnO4溶液中。若管道中空气流量为a L/min,经过b min溶液恰好褪色(假定样品中的SO2可被溶液充分吸收),则该空气样品中SO2的含量为___________ g/L(用含a、b的式子表示)。

(1)仪器组装完毕后,必须进行的实验操作是
(2)试剂1最好选择___________ (填标号)。
| A.30%盐酸 | B.50%硝酸 | C.70%硫酸 | D.98%硫酸 |
(4)某同学预测装置Ⅲ 中不会产生白色沉淀,随着实验的进行,装置Ⅲ 中产生了少量白色沉淀,该白色沉淀的化学式为
(5)为测定空气中的SO2含量,实验小组将空气样品经过管道通入密闭容器中的100 mL 0.2000 mol/L的酸性KMnO4溶液中。若管道中空气流量为a L/min,经过b min溶液恰好褪色(假定样品中的SO2可被溶液充分吸收),则该空气样品中SO2的含量为
您最近一年使用:0次
名校
解题方法
6 . 某化学小组设计了如图装置用于制取 并验证其性质。
并验证其性质。___________ ,仪器a连接的导管的作用是___________ 。
(2)装置A中反应的化学方程式为___________ 。
(3)若装置B中无明显现象,装置C中溶液红色褪色,则使品红的水溶液褪色的含硫微粒可能是___________ (填化学式)。
(4)装置D中溶液颜色由黄色变为浅绿色,发生反应的离子方程式为___________ 。
(5)装置E中盛有100 mL 0.100 mol/L的酸性 溶液,当
溶液,当 完全反应时,参加反应的
完全反应时,参加反应的 的质量为
的质量为___________ g。
(6)装置F的作用是___________ 。
 并验证其性质。
并验证其性质。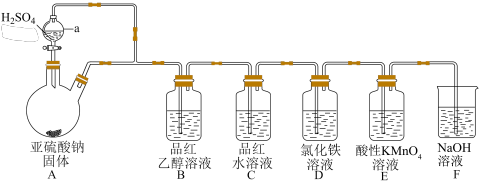
(2)装置A中反应的化学方程式为
(3)若装置B中无明显现象,装置C中溶液红色褪色,则使品红的水溶液褪色的含硫微粒可能是
(4)装置D中溶液颜色由黄色变为浅绿色,发生反应的离子方程式为
(5)装置E中盛有100 mL 0.100 mol/L的酸性
 溶液,当
溶液,当 完全反应时,参加反应的
完全反应时,参加反应的 的质量为
的质量为(6)装置F的作用是
您最近一年使用:0次
2023-07-01更新
|
157次组卷
|
2卷引用:安徽省马鞍山市2022-2023学年高一下学期6月期末考试化学试题
7 . 如图为实验室制取乙炔并验证其性质的装置图。下列说法错误的是
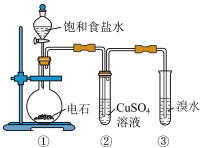
A.①中反应方程式为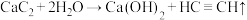 |
| B.②中溶液里会有黑色沉淀生成 |
| C.反应结束时,③中液体出现分层现象 |
| D.实验时可用长颈漏斗代替分液漏斗 |
您最近一年使用:0次
2023-05-21更新
|
73次组卷
|
2卷引用:安徽皖北省示范高中2022--2023学年高二下学期5月联考化学试题
8 . 为检验某漂白粉是否变质,进行下列探究实验:
实验1:取5g漂白粉样品于烧杯中,加足量蒸馏水并搅拌,观察到有固体不溶解。
实验2:静置,取少量实验1的上层清液于试管中。放入红色花瓣,观察到花瓣褪色。
实验3:另取5g漂白粉样品于试管中,滴加浓盐酸,观察到有气体产生。
下列说法正确的是
实验1:取5g漂白粉样品于烧杯中,加足量蒸馏水并搅拌,观察到有固体不溶解。
实验2:静置,取少量实验1的上层清液于试管中。放入红色花瓣,观察到花瓣褪色。
实验3:另取5g漂白粉样品于试管中,滴加浓盐酸,观察到有气体产生。
下列说法正确的是
| A.工业上用氯气和澄清石灰水制取漂白粉 |
| B.实验1和实验2说明漂白粉没有变质 |
| C.实验3中产生的气体只有氯气 |
D.实验3中下列反应的电子转移可表示为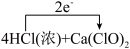 =CaCl2+2Cl2↑+2H2O =CaCl2+2Cl2↑+2H2O |
您最近一年使用:0次
2023-02-15更新
|
1021次组卷
|
11卷引用:安徽省六安市舒城晓天中学2023-2024学年高一上学期期中考试化学试卷
安徽省六安市舒城晓天中学2023-2024学年高一上学期期中考试化学试卷江苏省南京市2022-2023学年高一上学期期末学情调研测试化学试题(已下线)第07讲 氯气的性质和次氯酸-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)专题05 氯及其化合物【考点清单】(讲+练)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)(已下线)专题05 氯及其化合物【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)辽宁省丹东市凤城市第一中学2023-2024学年高三上学期10月测试化学试题江苏省江都区大桥中学2023-2024学年高一上学期期末复习模拟测试化学试题贵州省遵义市桐梓县荣兴高级中学2023-2024学年高一上学期第四次月考化学试题江苏省南京市金陵中学河西分校2023-2024学年高一上学期10月阶段检测化学试卷(已下线)专题04 氯气及氯的化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)(已下线)衔接点14 氯气的性质-2024年初升高化学无忧衔接(通用版)
名校
解题方法
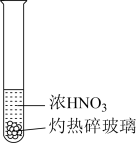
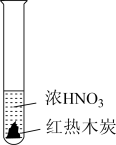
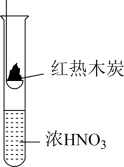
9 . 下述实验中均有红棕色气体产生,对比分析所得结论正确的是
|
|
|
| ① | ② | ③ |
| A.由①中的红棕色气体,推断产生的气体一定都是氮的氧化物 |
| B.②中产生红棕色气体说明②中木炭与浓硝酸产生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 |
D.③的气体产物中检测出 由此说明木炭一定与浓硝酸发生了反应 由此说明木炭一定与浓硝酸发生了反应 |
您最近一年使用:0次
2022-05-14更新
|
267次组卷
|
5卷引用:安徽省宿州市省、市示范高中2022-2023学年高一下学期期中考试化学试题