1 . 下列有关物质性质与用途具有对应关系的是
| A.次氯酸具有弱酸性,可用作有色物质的漂白剂 |
| B.硫酸铜溶液呈蓝色,可用作游泳池中水的消毒剂 |
| C.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
| D.铅具有还原性和导电性,可用作铅蓄电池的负极材料 |
您最近半年使用:0次
2019-05-17更新
|
100次组卷
|
4卷引用:江苏省七市(南通、泰州、扬州、徐州、淮安、宿迁、连云港)2019届高三第三次调研考试 化学试题
(已下线)江苏省七市(南通、泰州、扬州、徐州、淮安、宿迁、连云港)2019届高三第三次调研考试 化学试题江苏省徐州市王杰中学2021届高三12月份阶段性检测化学试题吉林省长春市九台师范高中2020-2021学年高一下学期第二阶段考试化学试题江苏省常熟市王淦昌高级中学2022-2023学年高二上学期10月月考化学试卷
名校
2 . 下列有关物质性质与用途具有对应关系的是
| A.MnO2不溶于水,可用作H2O2分解的催化剂 |
| B.SO2具有漂白性,可用于制溴工业中吸收Br2 |
| C.FeCl3溶液显酸性,可用于蚀刻铜制的电路板 |
| D.NH4NO3分解产生大量气体,可用作汽车安全气囊产气药 |
您最近半年使用:0次
2018-01-24更新
|
558次组卷
|
7卷引用:江苏南京市、盐城市2018届高三第一次模拟考试化学试题
2023高三·全国·专题练习
3 . 氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:
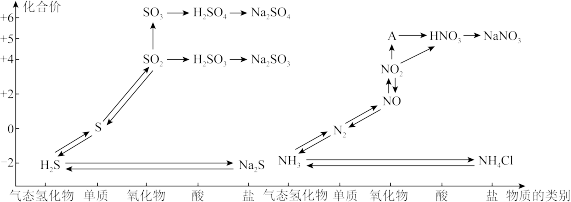
(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O 2HNO2
2HNO2
c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
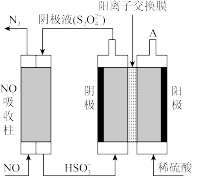
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质 NH3
NH3 HNO2
HNO2 HNO3
HNO3 N2
N2
请回答:
①过程Ⅲ发生反应的化学方程式为____ 。
②根据图1和图2,判断使用亚硝化菌的最佳条件为_______ 。
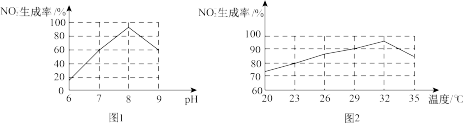
③利用微生物处理含氮废水的优点为_______ 。
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:_______ 。

(6)下图为制取氨气的装置和选用的试剂,其中错误的是_______ (填字母)。

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是_______ ,为了得到干燥的NH3,可用_______ 做干燥剂。若有5.35g氯化铵参加反应,则产生的气体在标准状况下的体积为_______ L。
(8)铵盐受热易分解,如图所示。
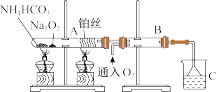
被加热的铂丝处发生反应的化学方程式为_______ 。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O
 2HNO2
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质
 NH3
NH3 HNO2
HNO2 HNO3
HNO3 N2
N2请回答:
①过程Ⅲ发生反应的化学方程式为
②根据图1和图2,判断使用亚硝化菌的最佳条件为
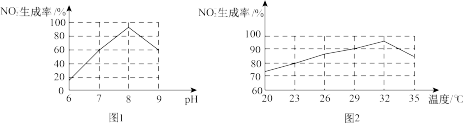
③利用微生物处理含氮废水的优点为
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:

(6)下图为制取氨气的装置和选用的试剂,其中错误的是

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是
(8)铵盐受热易分解,如图所示。
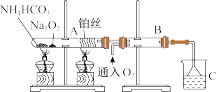
被加热的铂丝处发生反应的化学方程式为
您最近半年使用:0次
4 . 硫、氮、碳的氧化物都会引起环境问题,越来越引起人们的重视,如图1是氮元素的各种价态与物质类别的对应关系
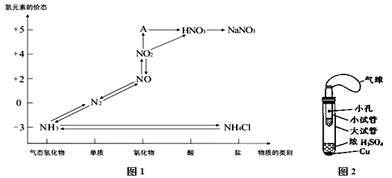
(1)根据A对应的化合价和物质类别,A为_________ (写分子式),从氦元素的化合价能否发生变化的角度判断,图1中既有氧化性又有还原性的化合物是_________ ;
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为_________________ ;
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式___________________ ;
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为__________ ;
A 双氧水(H2O2) B品红溶液 C 酸性高锰酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式______________ 。

(1)根据A对应的化合价和物质类别,A为
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为
A 双氧水(H2O2) B品红溶液 C 酸性高锰酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式
您最近半年使用:0次
5 . 化学在生产和生活中有着广泛的应用。下列对应关系错误的是
| 选项 | 化学性质 | 实际应用 |
| A | 镁铝合金导热性能好 | 镁铝合金常用于制窗框 |
| B | FeCl3的氧化性大于CuCl2 | FeCl3溶液用于蚀刻铜制线路板 |
| C | SO2具有还原性 | 海水制溴工业中用SO2的水溶液吸收Br2 |
| D | 铝易与氧结合且该反应放热 | 铝用于冶炼Cr、Mn等难熔金属 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2017-10-10更新
|
284次组卷
|
5卷引用:辽宁省重点高中协作校2018届高三上学期第一次阶段考试(10月) 化学试题
名校
6 . 氯化亚铁在冶金、医药制造、媒染剂等方面有着较为广泛的用途,氯化亚铁可以对许多分子进行激活反应,成为一种新型“明星分子”。回答下列问题:
(1)由 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取___________ g 固体在
固体在___________ (填试剂)中溶解后,加水稀释为 ,最后加入少量铁粉。
,最后加入少量铁粉。
(2)“无汞定铁法”标定 溶液浓度:
溶液浓度:
①将___________ (填酸式或碱式)滴定管先水洗,再润洗,最后盛装 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是___________ ,……正确安装滴定管。
②用移液管准确量取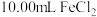 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是___________ 。
③用 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗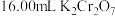 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式___________ 。 溶液的标定浓度为
溶液的标定浓度为___________ 。
(3)取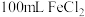 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为___________ 。
(4)已知:亚硫酰氯( )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: 后,先加热装置
后,先加热装置___________ (填“a”或“b”)。
②装置c、d连接在一起共同起到的作用___________ 。
③硬质玻璃试管b中发生反应的化学方程式___________ 。
④装置e中试剂为 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(1)由
 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取 固体在
固体在 ,最后加入少量铁粉。
,最后加入少量铁粉。(2)“无汞定铁法”标定
 溶液浓度:
溶液浓度:①将
 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是②用移液管准确量取
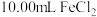 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是③用
 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗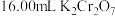 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式 溶液的标定浓度为
溶液的标定浓度为(3)取
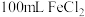 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为(4)已知:亚硫酰氯(
 )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: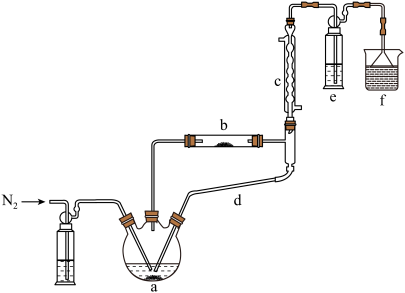
 后,先加热装置
后,先加热装置②装置c、d连接在一起共同起到的作用
③硬质玻璃试管b中发生反应的化学方程式
④装置e中试剂为
 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近半年使用:0次
7 . A、B、C、D是钠及其重要化合物,有着广泛的用途。已知B是常见的供氧剂,其相互转化关系如图所示(部分反应条件省略)。红热的铁能与水蒸气发生置换反应。回答下列问题:___________ 。
(2)B→C的化学方程式为___________ 。
(3)D→C的化学方程式为___________ 。
(4)若A为金属钠, 完全转化成D(涉及的其它反应物均足量),则生成D的质量为
完全转化成D(涉及的其它反应物均足量),则生成D的质量为___________ g。
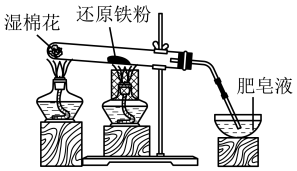
(5)某同学探究铁与水蒸气的反应,进行了如下实验:___________ (填标号)。
A.先点燃湿棉花处的酒精灯,一段时间后再点燃还原铁粉处的酒精灯
B.先点燃还原铁粉处的酒精灯,一段时间后再点燃湿棉花处的酒精灯
C.同时点燃湿棉花处和还原铁粉处的酒精灯
②能否根据肥皂液冒气泡来证明铁与水蒸气发生了反应?___________ (填“能”或“不能”)。
③实验结束恢复到室温后,能否用磁铁将未参加反应的铁粉从反应后的固体中分离出来?___________ (填“能”或“不能”)。

(2)B→C的化学方程式为
(3)D→C的化学方程式为
(4)若A为金属钠,
 完全转化成D(涉及的其它反应物均足量),则生成D的质量为
完全转化成D(涉及的其它反应物均足量),则生成D的质量为(5)某同学探究铁与水蒸气的反应,进行了如下实验:
A.先点燃湿棉花处的酒精灯,一段时间后再点燃还原铁粉处的酒精灯
B.先点燃还原铁粉处的酒精灯,一段时间后再点燃湿棉花处的酒精灯
C.同时点燃湿棉花处和还原铁粉处的酒精灯
②能否根据肥皂液冒气泡来证明铁与水蒸气发生了反应?
③实验结束恢复到室温后,能否用磁铁将未参加反应的铁粉从反应后的固体中分离出来?
您最近半年使用:0次
解题方法
8 . 焦亚硫酸钠(Na2S2O5)在化学工业中用途广泛。其一种制备流程如下:
(1)SO2分子的VSEPR模型为___________ 。
(2)“NaHCO3制备”所用实验装置(夹持仪器已省略)如下图:___________ 。
②饱和碳酸氢钠溶液的作用是___________ 。
③三颈烧瓶中生成NaHCO3反应的化学方程式为___________ (NaHCO3为沉淀物)。
(3)“Na2S2O5制备”反应过程分四步:
步骤I.在碳酸钠溶液中通入SO2至pH为4.1,生成NaHSO3溶液;
步骤Ⅱ.停止通SO2,向NaHSO3溶液中再加入Na2CO3溶液调至pH为7~8,转化为Na2SO3;
步骤Ⅲ.继续通入SO2至pH达4.1,又生成NaHSO3溶液;
步骤Ⅳ.当溶液中NaHSO3含量达到过饱和浓度时析出Na2S2O5。
①步骤I测量溶液的pH=4.1所用仪器是___________ 。
②写出步骤Ⅱ中反应的离子方程式:___________ 。
③写出I~Ⅳ步骤中总反应的化学方程式:___________ 。
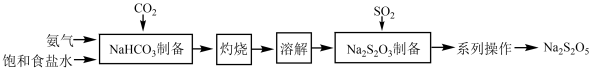
(1)SO2分子的VSEPR模型为
(2)“NaHCO3制备”所用实验装置(夹持仪器已省略)如下图:
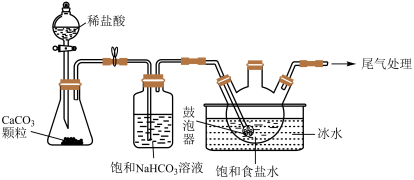
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成NaHCO3反应的化学方程式为
(3)“Na2S2O5制备”反应过程分四步:
步骤I.在碳酸钠溶液中通入SO2至pH为4.1,生成NaHSO3溶液;
步骤Ⅱ.停止通SO2,向NaHSO3溶液中再加入Na2CO3溶液调至pH为7~8,转化为Na2SO3;
步骤Ⅲ.继续通入SO2至pH达4.1,又生成NaHSO3溶液;
步骤Ⅳ.当溶液中NaHSO3含量达到过饱和浓度时析出Na2S2O5。
①步骤I测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出I~Ⅳ步骤中总反应的化学方程式:
您最近半年使用:0次
9 . 镁及其合金是用途很广的金属材料,可以通过以下步骤从海水中提取镁。
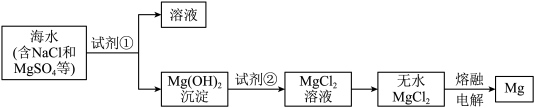
下列说法不正确 的是

下列说法
| A.试剂①可以选用石灰乳 |
B.加入试剂①后,能够分离得到 沉淀的方法是过滤 沉淀的方法是过滤 |
C. 溶液通过蒸发结晶可得到无水 溶液通过蒸发结晶可得到无水 |
D.电解熔融 所得副产物 所得副产物 是工业制备试剂②的主要原料 是工业制备试剂②的主要原料 |
您最近半年使用:0次
2024-04-18更新
|
113次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
10 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 以上。工业制硅,先制得粗硅,再制得高纯硅。
以上。工业制硅,先制得粗硅,再制得高纯硅。
I.请回答:
(1)工业制粗硅反应的化学方程式为_______ ,制取的高纯硅可用于_______ (写出硅的一种用途)。
(2)工业制粗硅的中间产物 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和一种气体单质,请写出化学反应方程式
和一种气体单质,请写出化学反应方程式_______ 。
II.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
,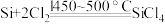
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(3)A中装浓盐酸的仪器名称是_______ 。
(4)装置B的作用是_______ 。
(5)为了更好的收集产品,可以将试剂瓶E放在_______ 中使四氯化硅液化收集。
(6)能否将装置G改成如图装置来吸收尾气?_______ (填“能”或“不能”),原因:_______ 。
 以上。工业制硅,先制得粗硅,再制得高纯硅。
以上。工业制硅,先制得粗硅,再制得高纯硅。I.请回答:
(1)工业制粗硅反应的化学方程式为
(2)工业制粗硅的中间产物
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和一种气体单质,请写出化学反应方程式
和一种气体单质,请写出化学反应方程式II.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。

①
 ,
,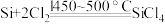
②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(3)A中装浓盐酸的仪器名称是
(4)装置B的作用是
(5)为了更好的收集产品,可以将试剂瓶E放在
(6)能否将装置G改成如图装置来吸收尾气?
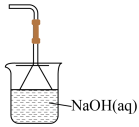
您最近半年使用:0次



