1 . 某学生设计下列实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
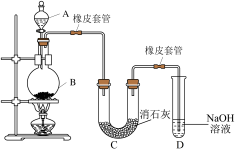
(1)A仪器的名称是___________ ,所盛试剂是___________ 。
(2)漂白粉将在U形管中产生,其化学方程式是___________ 。
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②试判断另一个副反应是___________ (写出此反应方程式)。为避免此副反应的发生,可采取的措施是___________ 。

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应是
您最近半年使用:0次
解题方法
2 . 某合金废料主要含铁、铜、铝,为从合金废料中得到Fe2O3、Al2O3和金属Cu等产品,某化学兴趣小组按如图所示工艺流程进行实验(杂质不与稀硫酸反应)。(提示:Al3++4OH-=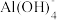 )
)

请回答下列问题:
(1)固体A主要含有的物质是___________ 。
(2)B到C发生反应的离子方程式为_______ ,溶液C中的阳离子主要有__________ 。
(3)若D为NaOH,则溶液E中铝元素的存在形式是___________ (填化学式)。
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
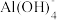 )
)
请回答下列问题:
(1)固体A主要含有的物质是
(2)B到C发生反应的离子方程式为
(3)若D为NaOH,则溶液E中铝元素的存在形式是
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
| A.蒸发皿 | B.烧杯 | C.坩埚 | D.试管 |
您最近半年使用:0次
3 . 孔雀石的主要成分是CuCO3·Cu(OH)2,某小组以孔雀石、锌粒、废稀硫酸为原料制备铜,设计了如下两套方案:
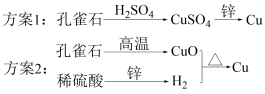
下列说法错误的是

下列说法错误的是
| A.方案1和方案2都发生了置换反应 |
| B.从安全角度考虑,方案1优于方案2 |
| C.理论上,方案2中等质量的锌可以制备等质量的铜 |
| D.方案2消耗的能量大于方案1消耗的能量 |
您最近半年使用:0次
4 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是__________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式________ 。“滤液②”中含有的金属离子是_________ 。
(2)“转化”中可替代H2O2的物质是___________。
(3)若工艺流程改为先“调pH”后“转化”,即

则“滤液③”中可能含有的杂质离子为___________ 。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=___________ 。如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是___________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式___________ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“转化”中可替代H2O2的物质是___________。
| A.酸性KMnO4溶液 | B.O2 | C.硝酸 | D.新制氯水 |

则“滤液③”中可能含有的杂质离子为
(4)利用上述表格数据,计算Ni(OH)2的Ksp=
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近半年使用:0次
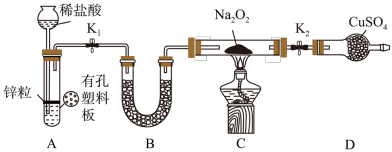
5 . 某同学结合所学知识探究 与
与 能否反应,设计装置如图,下列说法正确的是
能否反应,设计装置如图,下列说法正确的是
 与
与 能否反应,设计装置如图,下列说法正确的是
能否反应,设计装置如图,下列说法正确的是
| A.装置A气密性的检查方法:直接向长颈漏斗中加水,当漏斗中液面高于试管中液面,说明气密性良好 |
B.装置A也可直接用于Cu与浓硫酸反应制取 |
C.为达到实验目的需在装置B中盛放无水 |
| D.装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度 |
您最近半年使用:0次
2023-01-14更新
|
430次组卷
|
4卷引用:微专题(九) 气体制备与性质的综合
名校
解题方法
6 . 某学习小组欲制备氯水和漂白粉,并利用所制溶液进行相关实验探究。实验装置如图所示。回答有关问题。

(1)装置A中生成氯气的离子方程式为_______ 。
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为_______ 。装置C装入的试剂是蒸馏水,用于制备氯水。装置D中盛有_______ ,可以在防止氯气泄露污染空气的同时制备漂白粉。
(3)若装置A中用8.7gMnO2与足量浓盐酸混合加热,当MnO2完全反应完,生成的氯气在标况下的体积为_______ L,则被氧化的HCl的质量是_______ g,反应中转移的电子为_______ mol。
(4)小组同学用上述实验中得到的氯水进行如下实验
根据该小组的实验报告,回答下列问题:
①实验i中发生反应的离子方程式为_______ 。
②实验ii的结论是否严谨?_______ (填“是”或“否”),理由是_______ 。
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:_______ 。
如要证明到底是什么原因使溶液褪色,还需进一步设计实验验证。

(1)装置A中生成氯气的离子方程式为
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为
(3)若装置A中用8.7gMnO2与足量浓盐酸混合加热,当MnO2完全反应完,生成的氯气在标况下的体积为
(4)小组同学用上述实验中得到的氯水进行如下实验
| 实验序号 | 试剂和操作 | 实验现象 | 结论 |
| i | 在4mLNaBr溶液中加入1mL氯水 | 溶液变黄色 | 氯气的氧化性比溴强 |
| ii | 在4mLKI溶液中加入实验i所得黄色溶液 | 溶液变为棕黄色 | 溴的氧化性比碘强 |
| iii | 在滴有酚酞的NaOH溶液中滴加氯水 | 当氯水滴到一定量时,溶液红色突然褪去 | 氯水显酸性 |
①实验i中发生反应的离子方程式为
②实验ii的结论是否严谨?
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:
如要证明到底是什么原因使溶液褪色,还需进一步设计实验验证。
您最近半年使用:0次
名校
解题方法
7 . 用废铁屑制备磁性氧化铁( ),制取过程如图:
),制取过程如图:
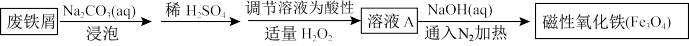
已知: 的作用是洗去废铁屑表面的油污。
的作用是洗去废铁屑表面的油污。
下列说法不正确的是
 ),制取过程如图:
),制取过程如图: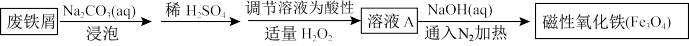
已知:
 的作用是洗去废铁屑表面的油污。
的作用是洗去废铁屑表面的油污。下列说法不正确的是
A.实验室可用铁与水蒸气在高温条件下制取 |
B.检验A中的 可以用KSCN溶液 可以用KSCN溶液 |
C.加 时发生反应的方程式为 时发生反应的方程式为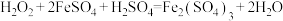 |
D.制备 的反应 的反应 是氧化还原反应 是氧化还原反应 |
您最近半年使用:0次
2023-01-07更新
|
492次组卷
|
4卷引用:作业(十八) 铁盐和亚铁盐
解题方法
8 . 如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。

(1)A装置为CO2的发生装置,反应的离子方程式为_____ 。
(2)B装置可除去A装置中可能挥发出的_____ ,反应的离子方程式为_____ 。
(3)C装置为O2的发生装置,反应的化学方程式为_____ 、_____ 。
(4)D装置可除去C装置中未反应的_____ ,反应的离子方程式为_____ 。
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为_____ 。

(1)A装置为CO2的发生装置,反应的离子方程式为
(2)B装置可除去A装置中可能挥发出的
(3)C装置为O2的发生装置,反应的化学方程式为
(4)D装置可除去C装置中未反应的
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为
您最近半年使用:0次
解题方法
9 . 下图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化。
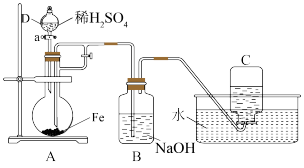
请回答下列问题:
(1)仪器D的名称为________ 。
(2)如何控制仪器D滴加稀硫酸的速度__________ 。
(3)A中反应一段时间后,关闭a,在B中即可得到Fe(OH)2。关闭a的操作不可太早,原因是__________ 。
(4)实验完毕,拔去B装置中的橡胶塞,通入空气,此时B装置中发生反应的化学方程式为__________ 。
(5)简述制取Fe(OH)2的过程及原理:__________ 。
(6)在下图中,装置④中FeSO4溶液上方加一层苯的作用是________ 。装置__________ (填序号)能较长时间观察到Fe(OH)2白色沉淀。


请回答下列问题:
(1)仪器D的名称为
(2)如何控制仪器D滴加稀硫酸的速度
(3)A中反应一段时间后,关闭a,在B中即可得到Fe(OH)2。关闭a的操作不可太早,原因是
(4)实验完毕,拔去B装置中的橡胶塞,通入空气,此时B装置中发生反应的化学方程式为
(5)简述制取Fe(OH)2的过程及原理:
(6)在下图中,装置④中FeSO4溶液上方加一层苯的作用是

您最近半年使用:0次
2022-12-05更新
|
537次组卷
|
2卷引用:作业(十七) 铁的单质、氧化物、氢氧化物
解题方法
10 . 已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下面示意图中的装置可以实现该反应。
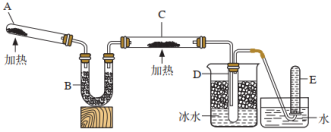
A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是____ 。
(2)实验时在C中观察到的现象是____ ,发生反应的化学方程式是_____ 。
(3)实验时在D中观察到的现象是____ ,收集到的物质是____ 。

A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是
(2)实验时在C中观察到的现象是
(3)实验时在D中观察到的现象是
您最近半年使用:0次



