23-24高一下·全国·课后作业
1 . 关于以下实验装置,说法不正确的是
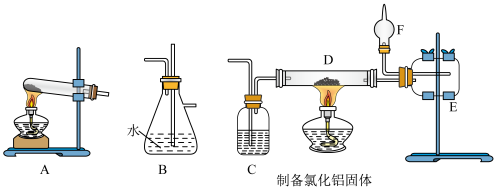

| A.用装置A盛装NH4Cl粉末来制取氨气,并用向下排气法收集 |
| B.装置B既可以防止倒吸,又可以检查实验时装置B后的装置是否发生堵塞 |
| C.装置C、F中盛装的试剂分别为浓硫酸、碱石灰,装置C用来除去Cl2中的水蒸气,装置F用来防止空气中的水蒸气进入装置E |
| D.装置D中的产物受热易升华,最好用粗短导管连接装置D、E |
您最近半年使用:0次
解题方法
2 . 1,2-二溴乙烷(CH2BrCH2Br)在常温下是无色液体,密度比水大,沸点是131.4 ℃,熔点是9.79 ℃,不溶于水。在实验室中可以用如图所示装置来制备1,2-二溴乙烷。其中烧杯D中小试管装有液溴(表面覆盖少量水)。
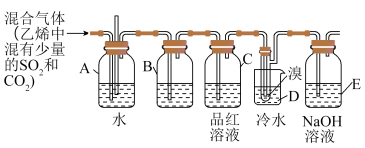
(1)写出制备1,2-二溴乙烷的化学方程式___________ 。
(2)A装置一个作用是可以检查实验进行时D中小试管里的导管是否发生堵塞。另一作用是___________ 。
(3)容器B中所装试剂为___________ 溶液,容器E中NaOH溶液的作用是___________ 。
(4)反应过程中应用冷水冷却装置D,如过度冷却(如用冰水),其后果是___________ 。

(1)写出制备1,2-二溴乙烷的化学方程式
(2)A装置一个作用是可以检查实验进行时D中小试管里的导管是否发生堵塞。另一作用是
(3)容器B中所装试剂为
(4)反应过程中应用冷水冷却装置D,如过度冷却(如用冰水),其后果是
您最近半年使用:0次
3 . Ⅰ.某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
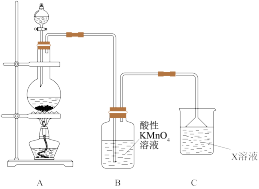
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为___________ 。C装置的作用___________ 。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是___________ 。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为___________ 。
(3)验证该气体的实验方案如下:
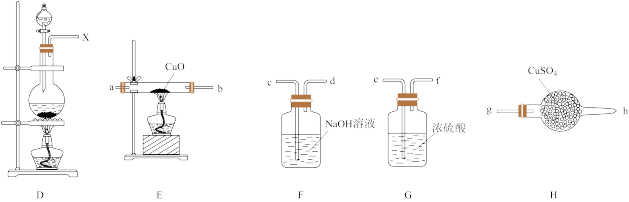
①装置连接顺序:________
X→___________→___________→___________→___________→a→b→___________。
②能证明上述假设成立的实验现象是___________ 。
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处___________ 。

(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是
(3)验证该气体的实验方案如下:

①装置连接顺序:
X→___________→___________→___________→___________→a→b→___________。
②能证明上述假设成立的实验现象是
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处
您最近半年使用:0次
4 . 某学生设计下列实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
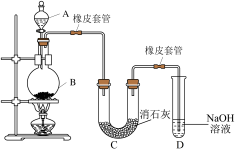
(1)A仪器的名称是___________ ,所盛试剂是___________ 。
(2)漂白粉将在U形管中产生,其化学方程式是___________ 。
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②试判断另一个副反应是___________ (写出此反应方程式)。为避免此副反应的发生,可采取的措施是___________ 。

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应是
您最近半年使用:0次
解题方法
5 . 某合金废料主要含铁、铜、铝,为从合金废料中得到Fe2O3、Al2O3和金属Cu等产品,某化学兴趣小组按如图所示工艺流程进行实验(杂质不与稀硫酸反应)。(提示:Al3++4OH-=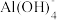 )
)

请回答下列问题:
(1)固体A主要含有的物质是___________ 。
(2)B到C发生反应的离子方程式为_______ ,溶液C中的阳离子主要有__________ 。
(3)若D为NaOH,则溶液E中铝元素的存在形式是___________ (填化学式)。
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
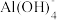 )
)
请回答下列问题:
(1)固体A主要含有的物质是
(2)B到C发生反应的离子方程式为
(3)若D为NaOH,则溶液E中铝元素的存在形式是
(4)灼烧沉淀F时所用主要仪器之一是___________(填字母)。
| A.蒸发皿 | B.烧杯 | C.坩埚 | D.试管 |
您最近半年使用:0次
6 . 孔雀石的主要成分是CuCO3·Cu(OH)2,某小组以孔雀石、锌粒、废稀硫酸为原料制备铜,设计了如下两套方案:
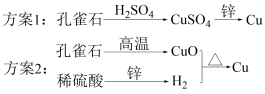
下列说法错误的是

下列说法错误的是
| A.方案1和方案2都发生了置换反应 |
| B.从安全角度考虑,方案1优于方案2 |
| C.理论上,方案2中等质量的锌可以制备等质量的铜 |
| D.方案2消耗的能量大于方案1消耗的能量 |
您最近半年使用:0次
7 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是__________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式________ 。“滤液②”中含有的金属离子是_________ 。
(2)“转化”中可替代H2O2的物质是___________。
(3)若工艺流程改为先“调pH”后“转化”,即

则“滤液③”中可能含有的杂质离子为___________ 。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=___________ 。如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是___________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式___________ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“转化”中可替代H2O2的物质是___________。
| A.酸性KMnO4溶液 | B.O2 | C.硝酸 | D.新制氯水 |

则“滤液③”中可能含有的杂质离子为
(4)利用上述表格数据,计算Ni(OH)2的Ksp=
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近半年使用:0次
22-23高二·全国·课时练习
解题方法
8 . 某实验小组用如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯),反应原理为
 。
。
实验步骤:①浓硝酸与浓硫酸按体积比1∶3配制混合溶液(即混酸)共40 mL;
②在三颈烧瓶中加入13 g甲苯(易挥发),按如图所示装好药品和其他仪器;
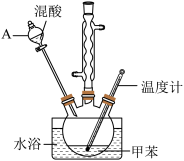
③向三颈烧瓶中加入混酸;
④控制温度约为50~55 ℃,反应大约10 min,三颈烧瓶底部有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15 g。
相关物质的性质如下:
(1)仪器A的名称是_______ 。
(2)若实验后在三颈烧瓶中收集的产物较少,可能的原因是_______ 。
(3)分离反应后产物的方案如下:

操作1的名称是_______ ,操作2中不需要用到下列仪器中的_______ (填字母)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(4)本实验中邻、对硝基甲苯的产率为_______ (保留小数点后一位)。
 。
。实验步骤:①浓硝酸与浓硫酸按体积比1∶3配制混合溶液(即混酸)共40 mL;
②在三颈烧瓶中加入13 g甲苯(易挥发),按如图所示装好药品和其他仪器;

③向三颈烧瓶中加入混酸;
④控制温度约为50~55 ℃,反应大约10 min,三颈烧瓶底部有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15 g。
相关物质的性质如下:
| 有机物 | 熔点 | 沸点/℃ | 溶解性 |
| 甲苯 | 0.866 | 110.6 | 不溶于水 |
| 对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
(2)若实验后在三颈烧瓶中收集的产物较少,可能的原因是
(3)分离反应后产物的方案如下:

操作1的名称是
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(4)本实验中邻、对硝基甲苯的产率为
您最近半年使用:0次
22-23高二下·全国·课时练习
解题方法
9 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
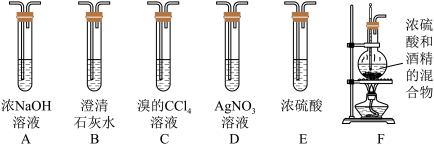
(1)实验中,混合浓硫酸与乙醇的方法是将_______ 慢慢加入另一种物质中;加热F装置时必须使液体温度_______ 。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:_______ 。
(3)为实现上述实验目的,装置的连接顺序为F→_______ →D(各装置限用一次)。
(4)当C中观察到_______ 时,表明单质溴能与乙烯反应;当D中_______ 时,表明C中发生的是取代反应;若D中没有出现前面所描述的现象时,表明C中发生的是_______ 反应。
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有_______ 个。
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体

(1)实验中,混合浓硫酸与乙醇的方法是将
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:
(3)为实现上述实验目的,装置的连接顺序为F→
(4)当C中观察到
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体
您最近半年使用:0次
10 . 晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅的过程如下:
I.高温下用过量的碳还原二氧化硅制得粗硅;
II.粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl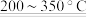 SiHCl3+H2);
SiHCl3+H2);
III.SiHCl3与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCl3能与水剧烈反应。
(1)第一步用焦炭与石英砂制取粗硅,其反应的化学方程式为_______ ;上述反应中的氧化剂是_______ ,还原剂是_______ 。
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为_______ 。
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是_______ ,装置C中的烧杯需要加热,目的是_______ 。
②反应一段时间后,装置D中观察到的现象是_______ ,装置D不能采用普通玻璃管的原因是_______ ,装置D中发生反应的化学方程式是_______ 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及_____ 。
I.高温下用过量的碳还原二氧化硅制得粗硅;
II.粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl
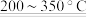 SiHCl3+H2);
SiHCl3+H2);III.SiHCl3与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCl3能与水剧烈反应。
(1)第一步用焦炭与石英砂制取粗硅,其反应的化学方程式为
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
您最近半年使用:0次



