名校
1 . 从海水(含 )中提溴
)中提溴 ,常用
,常用 做吸收剂。
做吸收剂。
资料:ⅰ. 在碱性溶液中可转化为
在碱性溶液中可转化为 (有强氧化性)和
(有强氧化性)和 。
。
ⅱ. ,深红棕色液体,易挥发。
,深红棕色液体,易挥发。
(1)向 溶液中滴加酚酞,溶液变红,说明
溶液中滴加酚酞,溶液变红,说明 溶液呈
溶液呈_______ 性。
(2)从海水中提溴的流程示意如下:
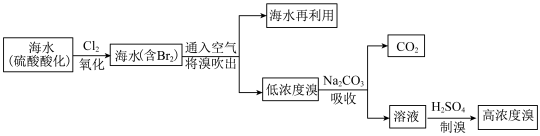
①海水中含大量 、
、 、
、 、
、 、
、 等离子,硫酸酸化能除去的离子是
等离子,硫酸酸化能除去的离子是_______ 。
②“氧化”过程体现出氧化性,
_______  (填“>”或“<”)。
(填“>”或“<”)。
③ 可用热空气吹出,原因是
可用热空气吹出,原因是_______ 。
④低浓度溴中含 、
、 ,吸收过程反应如下:
,吸收过程反应如下:
ⅰ.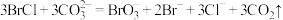
ⅱ._______
⑤“制溴”过程生成 的离子方程式是
的离子方程式是_______ 。
⑥“制溴”过程,用 而不用
而不用 ,可能的原因是
,可能的原因是_______ 。
 )中提溴
)中提溴 ,常用
,常用 做吸收剂。
做吸收剂。资料:ⅰ.
 在碱性溶液中可转化为
在碱性溶液中可转化为 (有强氧化性)和
(有强氧化性)和 。
。ⅱ.
 ,深红棕色液体,易挥发。
,深红棕色液体,易挥发。(1)向
 溶液中滴加酚酞,溶液变红,说明
溶液中滴加酚酞,溶液变红,说明 溶液呈
溶液呈(2)从海水中提溴的流程示意如下:

①海水中含大量
 、
、 、
、 、
、 、
、 等离子,硫酸酸化能除去的离子是
等离子,硫酸酸化能除去的离子是②“氧化”过程体现出氧化性,

 (填“>”或“<”)。
(填“>”或“<”)。③
 可用热空气吹出,原因是
可用热空气吹出,原因是④低浓度溴中含
 、
、 ,吸收过程反应如下:
,吸收过程反应如下:ⅰ.
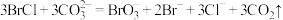
ⅱ.
⑤“制溴”过程生成
 的离子方程式是
的离子方程式是⑥“制溴”过程,用
 而不用
而不用 ,可能的原因是
,可能的原因是
您最近一年使用:0次
2023-06-05更新
|
85次组卷
|
2卷引用:北京市顺义区第一中学2022-2023学年高一下学期月考化学试题
名校
解题方法
2 . 中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其工艺流程如下图所示,试回答下列问题:
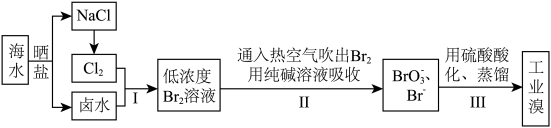
(1)海水日晒得到的盐因为含有较多杂质,称为粗盐。为了得到精制盐,可以用_______ 的办法除去其中的泥沙等不溶物。
(2)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是____________ 。
(3)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________ 。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(4)流程Ⅱ中涉及的离子反应方程式如下,请在下面横线内填入适当的化学计量数:___ Br2+___  =
= ___  +
+___ Br-+___ CO2↑
(5)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:___________________ 。
(6)流程Ⅲ蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________________ 。

(1)海水日晒得到的盐因为含有较多杂质,称为粗盐。为了得到精制盐,可以用
(2)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(3)步骤②通入热空气或水蒸气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(4)流程Ⅱ中涉及的离子反应方程式如下,请在下面横线内填入适当的化学计量数:
 =
=  +
+(5)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
(6)流程Ⅲ蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
您最近一年使用:0次
2020-10-09更新
|
271次组卷
|
3卷引用:山东省枣庄市第八中学2020-2021学年高一4月月考化学试题
名校
解题方法
3 . 已知海水中的溴含量约为 65 mg·L-1,从海水中提取溴的工业流程如下:
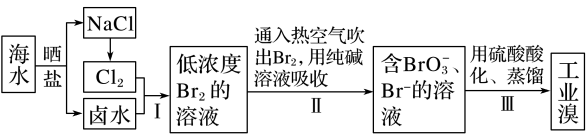
(1)写出步骤Ⅰ的离子方程式________________ 。
(2)步骤Ⅱ通入热空气吹出 Br2,利用了溴的_________________ (填序号)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在横线上填入正确的化学计量数:______ Br2+______ CO32-=______ BrO3-+______ Br-+______ CO2↑
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为_______________ 。
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有________________ (填字母)。
A.乙醇 B.四氯化碳 C.醋酸 D.苯

(1)写出步骤Ⅰ的离子方程式
(2)步骤Ⅱ通入热空气吹出 Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在横线上填入正确的化学计量数:
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有
A.乙醇 B.四氯化碳 C.醋酸 D.苯
您最近一年使用:0次
名校
解题方法
4 . 粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
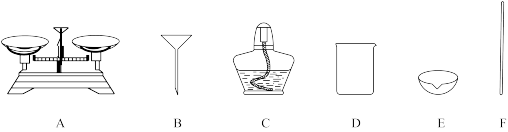
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。
(3)称量食盐应放在仪器A的___________ 盘,蒸发时防止液滴飞溅的操作是___________ 。
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
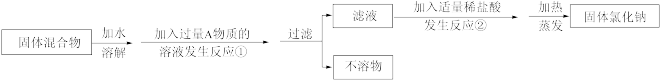
(4)写出A物质的化学式:___________ ,写出A物质的俗称:___________ 。
(5)写出反应②的化学方程式:___________ 。
(6)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填“增大”、“不变”或“减少”)。
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍过量 ):
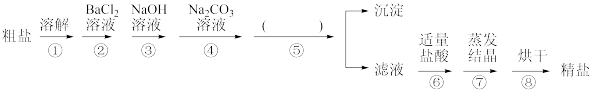
根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是___________ 。
(9)第⑤步操作的名称是___________ 。
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、___________ 、酒精灯。
(11)实验中加入“Na2CO3溶液”的目的是___________ 。
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):___________ 。
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:
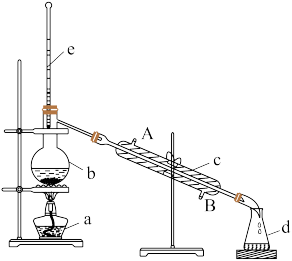
(13)仪器c的名称是___________ 。
(14)该分离混合物的原理是利用___________ 不同,通过加热的方式使其分离。
(15)冷水进水端是___________ 端( 填 A或B )
(16)为防暴沸需向___________ (填仪器名称)中加入___________ (填物品)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。

(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是
(3)称量食盐应放在仪器A的
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(4)写出A物质的化学式:
(5)写出反应②的化学方程式:
(6)反应①中加入过量A物质的目的是
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍

根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是
(9)第⑤步操作的名称是
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、
(11)实验中加入“Na2CO3溶液”的目的是
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:

(13)仪器c的名称是
(14)该分离混合物的原理是利用
(15)冷水进水端是
(16)为防暴沸需向
您最近一年使用:0次
5 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图:

(1)为除去粗盐中的杂质( 、
、 、
、 ),加入的试剂顺序正确的是
),加入的试剂顺序正确的是______ (填序号)。
A.NaOH溶液→ 溶液→
溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸
B. 溶液→NaOH溶液→
溶液→NaOH溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸
C.NaOH溶液→ 溶液→
溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸
D. 溶液→NaOH溶液→
溶液→NaOH溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸
(2)制备钠单质的方法之一是电解熔融NaCl,写出电解的化学方程式:_________ 。
(3)某化学兴趣小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料; 的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图实验装置:
的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图实验装置:
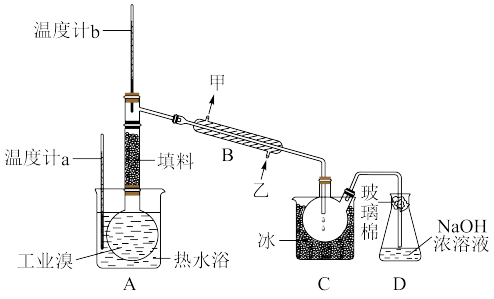
①图中仪器B的名称是_______ ,冷却水的出口为________ (填“甲”或“乙”)。
②C中液体的颜色为________ 。
③D装置的作用是_________ 。
(4)已知某溶液中 、
、 、
、 的物质的量之比为2:3:4,现欲使溶液中的
的物质的量之比为2:3:4,现欲使溶液中的 、
、 、
、 的物质的量之比变成4:3:2,那么需要通入
的物质的量之比变成4:3:2,那么需要通入 的物质的量是原溶液中
的物质的量是原溶液中 的物质的量的
的物质的量的______ (填序号)。
A. B.
B. C.
C. D.
D.

(1)为除去粗盐中的杂质(
 、
、 、
、 ),加入的试剂顺序正确的是
),加入的试剂顺序正确的是A.NaOH溶液→
 溶液→
溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸B.
 溶液→NaOH溶液→
溶液→NaOH溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸C.NaOH溶液→
 溶液→
溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸D.
 溶液→NaOH溶液→
溶液→NaOH溶液→ 溶液→过滤后加盐酸
溶液→过滤后加盐酸(2)制备钠单质的方法之一是电解熔融NaCl,写出电解的化学方程式:
(3)某化学兴趣小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料;
 的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图实验装置:
的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图实验装置:
①图中仪器B的名称是
②C中液体的颜色为
③D装置的作用是
(4)已知某溶液中
 、
、 、
、 的物质的量之比为2:3:4,现欲使溶液中的
的物质的量之比为2:3:4,现欲使溶液中的 、
、 、
、 的物质的量之比变成4:3:2,那么需要通入
的物质的量之比变成4:3:2,那么需要通入 的物质的量是原溶液中
的物质的量是原溶液中 的物质的量的
的物质的量的A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
2020-09-25更新
|
459次组卷
|
2卷引用:河南省豫西名校2020-2021学年高一下期第二次联考化学试题
名校
6 . 海洋是一个远未完全开发的巨大化学资源宝库。
(1)无需经过化学变化就能从海水中获得的物质是________ (填序号)
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO 等,要除去这些离子,下列加入药品顺序正确的是
等,要除去这些离子,下列加入药品顺序正确的是________ (填序号)
A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:
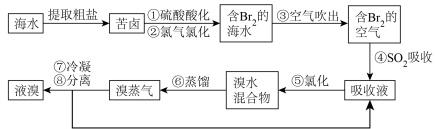
①写出由“苦卤”变成“含溴海水”的离子方程式________
②写出④发生反应的化学方程式________
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:

图中仪器B冷却水的出口为______ (填“甲”或“乙”),D装置的作用是__________ ,反应的离子方程式为__________ ,整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________ 。
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的__________
(1)无需经过化学变化就能从海水中获得的物质是
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO
 等,要除去这些离子,下列加入药品顺序正确的是
等,要除去这些离子,下列加入药品顺序正确的是A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:

①写出由“苦卤”变成“含溴海水”的离子方程式
②写出④发生反应的化学方程式
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:

图中仪器B冷却水的出口为
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的
您最近一年使用:0次
2020-06-28更新
|
216次组卷
|
2卷引用:湖南省娄底市双峰县第一中学2019-2020学年高一第二次月考化学试题
名校
解题方法
7 . 海水是十分重要的自然资源。下图是对海水的部分利用,有关说法不正确的是
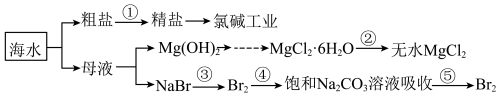

| A.海水晒盐得到粗盐和母液的过程属于物理变化 |
| B.粗盐(含MgCl2、CaCl2、Na2SO4以及泥沙等杂质)提纯为精盐加入试剂顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→稀盐酸 |
| C.工业上采用电解熔融MgCl2制得金属镁 |
| D.步骤③可以通入Cl2,因为氧化性:Cl2强于Br2 |
您最近一年使用:0次
8 . 海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。如图是海水综合利用的部分流程图,据图回答问题:
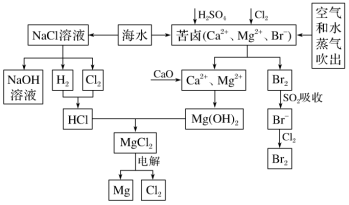
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、 等离子,为分别除去这些离子,所加试剂及有关操作的先后顺序为(试剂写化学式):
等离子,为分别除去这些离子,所加试剂及有关操作的先后顺序为(试剂写化学式):_______ 、_______ 、NaOH、过滤、HCl。
(2)电解饱和食盐水的离子方程式为____________ 。
(3)制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2+6H2O,该反应要在HCl气氛中进行,原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_________________________ 。
(4)金属镁着火不能用泡沫灭火器、干粉灭火器灭火,其原因是_____ 。(用化学方程式解释说明)
(5)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,发生反应生成H2SO4和HBr,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为______ 。
(6)也有工艺是在吹出Br2后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,同时有CO2放出,该反应的离子方程式是_____________________ ;最后再用H2SO4处理得到Br2,之后加入CCl4进行Br2的萃取,最终用________ 方法得到单质Br2。

(1)由海水晒制的粗盐中含有Ca2+、Mg2+、
 等离子,为分别除去这些离子,所加试剂及有关操作的先后顺序为(试剂写化学式):
等离子,为分别除去这些离子,所加试剂及有关操作的先后顺序为(试剂写化学式):(2)电解饱和食盐水的离子方程式为
(3)制取MgCl2的过程中涉及反应:MgCl2·6H2O
 MgCl2+6H2O,该反应要在HCl气氛中进行,原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是(4)金属镁着火不能用泡沫灭火器、干粉灭火器灭火,其原因是
(5)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,发生反应生成H2SO4和HBr,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为
(6)也有工艺是在吹出Br2后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,同时有CO2放出,该反应的离子方程式是
您最近一年使用:0次
9 . 海水中含有丰富的化学资源,可从中提取多种化工原料。某工厂对海水资源综合开发利用的部分工艺流程如图所示,下列说法不正确的是


A.步骤①可先依次加入过量 、 、 和 和 溶液,过滤后再加入适量盐酸调节 溶液,过滤后再加入适量盐酸调节 |
| B.步骤②发生的反应是氯碱工业的主要反应 |
C.步骤③通入 可制得 可制得 ,说明 ,说明 的氧化性大于 的氧化性大于 |
D.工业上可通过电解 溶液的方法获得镁单质 溶液的方法获得镁单质 |
您最近一年使用:0次
10 . 海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。下图是海水综合利用的部分流程图,据图回答问题:
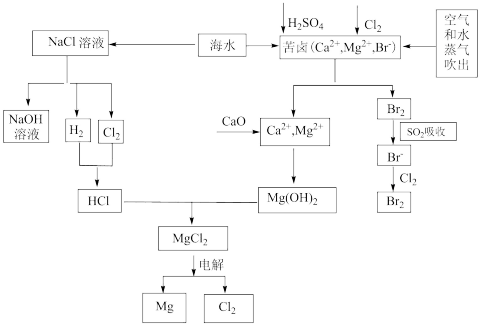
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式)_____________________ 。
(2)①目前较先进的电解制碱法是离子交换膜电解法,即用阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是______________ ,电解饱和食盐水的化学反应方程式为_____________ 。
②制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是_____________________ 。
(3)苦卤中先通入Cl2置换出Br2 ,为什么吹出后用SO2吸收转化为Br-再用Cl2置换,其理由是_________ ,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为_______________ 。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是_____________ ;最后再用H2SO4处理得到Br2 ,之后加入CCl4进行Br2的萃取,最终用_____________ 方法得到单质Br2。

(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式)
(2)①目前较先进的电解制碱法是离子交换膜电解法,即用阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是
②制取MgCl2的过程中涉及反应:MgCl2·6H2O
 MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是(3)苦卤中先通入Cl2置换出Br2 ,为什么吹出后用SO2吸收转化为Br-再用Cl2置换,其理由是
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是
您最近一年使用:0次



