1 . 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
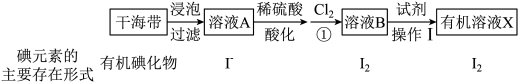
(1)提碘的原料一般选择海带或海藻,是因为___________ 。
(2)操作I中,实验室可用如图仪器将 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为___________ ,该步操作的名称为___________ ;下图所示的有机溶剂可以是___________ (填涂编号),选择依据是___________ ;分离液体时上层的溶液要从___________ 口(填“上”或者“下”)倒出在另一个烧杯中。

A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加___________ ,如出现___________ 现象,则证明 能代替氯水。
能代替氯水。

(1)提碘的原料一般选择海带或海藻,是因为
(2)操作I中,实验室可用如图仪器将
 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为
A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明
 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加 能代替氯水。
能代替氯水。
您最近半年使用:0次
2 . I.溴有“海洋元素”之称,海水中溴含量为65mg•L-1。空气吹出法工艺是目前“海水提溴”的最主要方法之一,其步骤如下:
(1)步骤①中获得Br2的离子方程式为___________ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是___________ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2,共有___________ 个电子转移(用a和 的代数式表示)。
的代数式表示)。
Ⅱ.碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的实验流程如下:___________ 、___________ 。
(5)“试剂a”通常应具有一定的___________ 性。
(6)由于“溶液B”中I2的含量较低,“操作Ⅱ”能将I2 “富集、浓缩”到“有机溶液X”中。已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___________ (填试剂标号)。
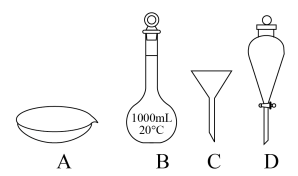
(7)“操作Ⅱ”宜选用的装置是___________ (填标号)。___________ 。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2,共有
 的代数式表示)。
的代数式表示)。Ⅱ.碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的实验流程如下:

(5)“试剂a”通常应具有一定的
(6)由于“溶液B”中I2的含量较低,“操作Ⅱ”能将I2 “富集、浓缩”到“有机溶液X”中。已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶,不与I2反应 | 与水不互溶,不与 I2反应 | 与水不互溶,不与I2反应 | 与水不互溶,与I2反应 |
(7)“操作Ⅱ”宜选用的装置是
您最近半年使用:0次
3 . 海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如下:

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是________ ;请你设计实验证明“浸取"已经进行完全:________ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为________ 。
(3)“萃取”时,CCl4层的颜色为________ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:________ 。
(4)“酸化”后生成含I2的悬浊液,需要经过________ (填操作名称)操作得到I2。
(5)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有________ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近半年使用:0次
4 . 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是_______ (填序号)。
(2)海带中含有碘元素。实验室提取碘的步骤如图所示:

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤_______ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式_______ 。提取碘的过程中,不能选择乙醇代替CCl4提取碘单质的原因_______ 。
(1)无需经过化学变化就能从海水中获得的物质是
| A.食盐 | B.溴 | C.烧碱 | D.纯碱 |

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤
②写出步骤④反应的离子方程式
您最近半年使用:0次
解题方法
5 . 卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液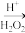 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带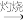 海带灰
海带灰 悬浊液
悬浊液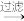 滤液
滤液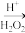 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
您最近半年使用:0次
名校
解题方法
6 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
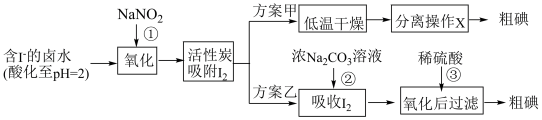
资料显示:Ⅰ.pH=2时,NaNO2溶液只能将I-氧化为I2;
Ⅱ. ;
;
Ⅲ.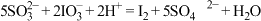 ;
;
(1)反应①生成一种无色气体,遇空气变为红棕色。则反应①的离子方程式是________ 。
(2)方案甲中,根据I2的特性,分离操作X的名称是________ 。
(3)已知I2在碱性溶液中反应生成I-和 。反应②的离子方程式是
。反应②的离子方程式是________ 。
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是________ 。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、 。请设计实验检验滤液中的
。请设计实验检验滤液中的 ,将实验方案补充完整。
,将实验方案补充完整。
可供选择的试剂:稀H2SO4、淀粉溶液、Na2SO3溶液
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B.________ 。

资料显示:Ⅰ.pH=2时,NaNO2溶液只能将I-氧化为I2;
Ⅱ.
 ;
;Ⅲ.
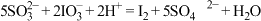 ;
;(1)反应①生成一种无色气体,遇空气变为红棕色。则反应①的离子方程式是
(2)方案甲中,根据I2的特性,分离操作X的名称是
(3)已知I2在碱性溶液中反应生成I-和
 。反应②的离子方程式是
。反应②的离子方程式是(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、
 。请设计实验检验滤液中的
。请设计实验检验滤液中的 ,将实验方案补充完整。
,将实验方案补充完整。可供选择的试剂:稀H2SO4、淀粉溶液、Na2SO3溶液
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B.
您最近半年使用:0次
7 . 化学实验源于生活。下列实验方案设计、现象与结论均正确的是
| 选项 | 目的 | 方案设计 | 现象结论 |
| A | 检验鸡皮中是否含有脂肪 | 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 | 一段时间后鸡皮变黄,说明鸡皮中含有脂肪 |
| B | 检验火柴头中是否含有氯元素 | 将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀 、 、 溶液 溶液 | 若有白色沉淀产生,说明火柴头中含有氯元素 |
| C | 检验海带中的碘元素 | 向海带灰的浸取液中通入适量氯气,再加入 萃取 萃取 | 若下层出现紫红色,则海带中含有碘元素 |
| D | 检验黑木耳中的铁元素 | 取少量黑木耳剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硫酸后再加入KSCN溶液 | 若溶液未变红,说明黑木耳中不含三价铁元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 实验室海带提碘的实验中不涉及的操作是
| A.浸泡 | B.萃取 | C.过滤 | D.蒸发 |
您最近半年使用:0次
9 . 海带中含有丰富的碘,某中学实验小组为了提取和检验海带灰中的碘,设计了以下实验流程。(已知:海带灰中的碘元素主要以 形式存在)
形式存在)
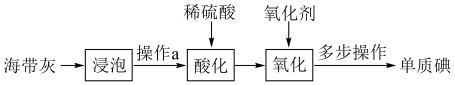
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是___________ (写一条即可)。
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要___________ 。
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: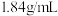 )的体积约为
)的体积约为___________  。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)
②配制过程的部分操作如下图,则操作步骤的正确顺序为___________ 。(用字母序号表示)
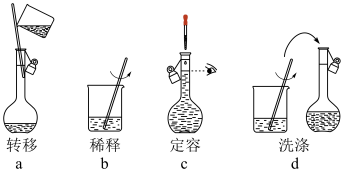
③下列有关配制上述稀硫酸的描述正确的是___________
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为___________ 。
②若选用 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法___________ 。
 形式存在)
形式存在)
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制
 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: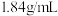 )的体积约为
)的体积约为 。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)②配制过程的部分操作如下图,则操作步骤的正确顺序为

③下列有关配制上述稀硫酸的描述正确的是
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用
 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为②若选用
 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法
您最近半年使用:0次
名校
10 . I.从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。

(1)海水所得粗盐中含 、
、 、
、 等杂质,为了有效除去
等杂质,为了有效除去 、
、 、
、 ,加入试剂的合理顺序为
,加入试剂的合理顺序为___________ 。
A.先加 ,后加
,后加 ,再加
,再加 试剂
试剂
B.先加 ,后加
,后加 试剂,再加
试剂,再加
C.先加 试剂,后加
试剂,后加 ,再加
,再加
(2)要除去 ,必须添加钡试剂,该钡试剂可以是
,必须添加钡试剂,该钡试剂可以是___________ 。
A. B.
B. C.
C.
a.写出用 制取氢氧化镁的化学方程式:
制取氢氧化镁的化学方程式:___________ 。
b.写出氯碱工业原理的离子方程式:___________ 。
II.海藻中提取碘的流程如图:

(3)指出提取碘的过程中有关实验操作名称:①___________ ,③___________ ;写出过程②中有关反应的离子方程式___________ 。

(1)海水所得粗盐中含
 、
、 、
、 等杂质,为了有效除去
等杂质,为了有效除去 、
、 、
、 ,加入试剂的合理顺序为
,加入试剂的合理顺序为A.先加
 ,后加
,后加 ,再加
,再加 试剂
试剂B.先加
 ,后加
,后加 试剂,再加
试剂,再加
C.先加
 试剂,后加
试剂,后加 ,再加
,再加
(2)要除去
 ,必须添加钡试剂,该钡试剂可以是
,必须添加钡试剂,该钡试剂可以是A.
 B.
B. C.
C.
a.写出用
 制取氢氧化镁的化学方程式:
制取氢氧化镁的化学方程式:b.写出氯碱工业原理的离子方程式:
II.海藻中提取碘的流程如图:

(3)指出提取碘的过程中有关实验操作名称:①
您最近半年使用:0次



