1 . 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
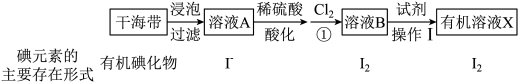
(1)提碘的原料一般选择海带或海藻,是因为___________ 。
(2)操作I中,实验室可用如图仪器将 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为___________ ,该步操作的名称为___________ ;下图所示的有机溶剂可以是___________ (填涂编号),选择依据是___________ ;分离液体时上层的溶液要从___________ 口(填“上”或者“下”)倒出在另一个烧杯中。

A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加___________ ,如出现___________ 现象,则证明 能代替氯水。
能代替氯水。

(1)提碘的原料一般选择海带或海藻,是因为
(2)操作I中,实验室可用如图仪器将
 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为
A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明
 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加 能代替氯水。
能代替氯水。
您最近半年使用:0次
2024高三下·全国·专题练习
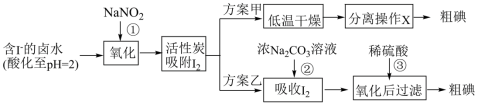
2 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
Ⅱ. ;
;
Ⅲ.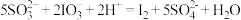 ;
;
方案甲中,根据I2的特性,分离操作X的名称是________ 。
Ⅱ.
 ;
;Ⅲ.
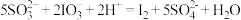 ;
;方案甲中,根据I2的特性,分离操作X的名称是
您最近半年使用:0次
名校
3 . 按要求填空:
(1)现有8个微粒: ;
; ;
;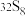 ;
;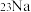 ;
;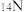 ;
; ;
; ;
; ;
;
表示核素的符号共______ 种;互为同位素的是______ 。
(2)现有以下物质:① ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
其中由离子键和非极性共价键构成的物质是______ (填序号,下同),属于共价化合物的是______ 。
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是______ (填序号),仅离子键被破坏的是______ (填序号)。
(4)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。反应结束后,再加入 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为______ ,可以观察到 层呈
层呈______ 色。
(1)现有8个微粒:
 ;
; ;
;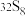 ;
;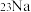 ;
;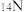 ;
; ;
; ;
; ;
;表示核素的符号共
(2)现有以下物质:①
 ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。其中由离子键和非极性共价键构成的物质是
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是
(4)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为 层呈
层呈
您最近半年使用:0次
名校
4 . 碘是国防、工业、农业、医药等部门和行业所依赖的重要原料,海水提碘是从海藻中提取元素碘的技术。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)
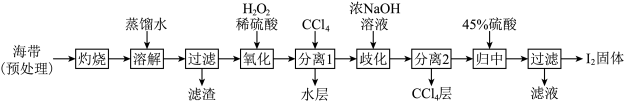
(1)“氧化”过程涉及到的离子方程式是________ ,请设计一种检验氧化后所得溶液含I2的方法:________ 。
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为________ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为________ 。
Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为________ kJ。

(4)Bodensteins研究了反应: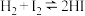 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
前40min的平均速率v(HI)=________ 。
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为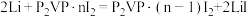 ,其工作原理如图所示:
,其工作原理如图所示:
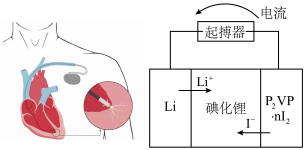
①正极发生的电极反应式为________ ;
②放电时,转移0.6×6.02×1023个电子,负极质量减少________ g。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)

(1)“氧化”过程涉及到的离子方程式是
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为

(4)Bodensteins研究了反应:
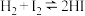 。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:
。温度为T时,在体积均为10L的密闭容器中进行实验,测得气体混合物中氢气的物质的量与反应时间t的关系如表:| 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 |
| 1molH2(g)、1molI2(g) | n(H2)mol | 1 | 0.5 | 0.32 | 0.24 | 0.20 |
Ⅲ.生命延续-心脏起搏器中的Li-I2电池
(5)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为
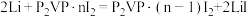 ,其工作原理如图所示:
,其工作原理如图所示:
①正极发生的电极反应式为
②放电时,转移0.6×6.02×1023个电子,负极质量减少
您最近半年使用:0次
5 . 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是_______ (填序号)。
(2)海带中含有碘元素。实验室提取碘的步骤如图所示:

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤_______ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式_______ 。提取碘的过程中,不能选择乙醇代替CCl4提取碘单质的原因_______ 。
(1)无需经过化学变化就能从海水中获得的物质是
| A.食盐 | B.溴 | C.烧碱 | D.纯碱 |

①海带灰中含有硫酸镁、碳酸钠等,在实验步骤
②写出步骤④反应的离子方程式
您最近半年使用:0次
解题方法
6 . 卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带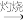 海带灰
海带灰 悬浊液
悬浊液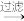 滤液
滤液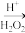 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带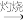 海带灰
海带灰 悬浊液
悬浊液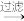 滤液
滤液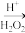 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
您最近半年使用:0次
23-24高一下·全国·课前预习
解题方法
7 . 海水提碘
“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是_____ 。
②该流程可循环利用的物质是_____ 。
③采用方案乙得到纯碘的产率较低,原因是_____ 。
“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次
解题方法
8 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
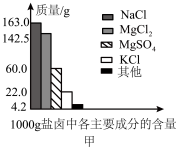
(1)根据图甲所示,写出盐卤中含量最多的盐为___________ (填化学式)其电子式为___________
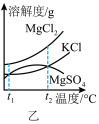
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是___________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
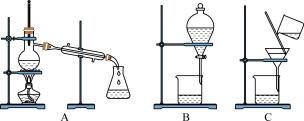
粗盐的提纯应选择图___________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是___________ 。
A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。
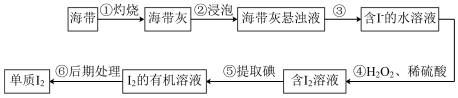
(4)实验步骤①会用到下列仪器中的___________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,___________ 。
(6)“提取碘”存在以下两种方案。
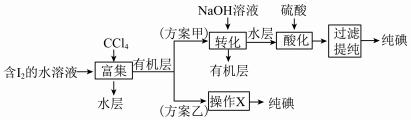
①方案乙中“操作X”的名称是___________ 。
②该流程可循环利用的物质是___________ 。
③采用方案乙得到纯碘的产率较低,原因是___________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是
(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,
(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次
2023高三·全国·专题练习
9 . 一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
海藻提碘可得到 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
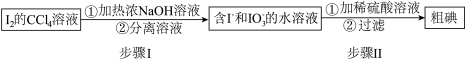
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ 。
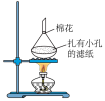
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。
海藻提碘可得到
 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

您最近半年使用:0次
10 . 人类的生产、生活离不开化学。
(1)从海水中提取溴的工业流程如图:

①请列举两种海水淡化的方法:___________ 、___________ 。
②步骤Ⅰ中发生反应的离子方程式为___________ 。
③已知步骤Ⅰ中已获得游离态的溴,通过步骤Ⅱ在吸收塔中得到化合态的溴,其目的是___________ 。
④吹出塔中通入热空气吹出 ,利用了
,利用了 的
的___________ (填序号);吸收塔中吸收 ,利用了
,利用了 的
的___________ (填序号)。
a.氧化性b.还原性c.挥发性d.腐蚀性
(2)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①由海带转化成海带灰,需要的主要仪器是___________ (填写序号并写出仪器名称)。

②若过程Ⅰ用 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为___________
③过程Ⅱ采用的分离方法和操作是___________ 、___________ 。
此过程中可以选用的溶剂是___________ (填序号)。
a.乙醇b.四氯化碳c.水d.苯
(1)从海水中提取溴的工业流程如图:

①请列举两种海水淡化的方法:
②步骤Ⅰ中发生反应的离子方程式为
③已知步骤Ⅰ中已获得游离态的溴,通过步骤Ⅱ在吸收塔中得到化合态的溴,其目的是
④吹出塔中通入热空气吹出
 ,利用了
,利用了 的
的 ,利用了
,利用了 的
的a.氧化性b.还原性c.挥发性d.腐蚀性
(2)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①由海带转化成海带灰,需要的主要仪器是

②若过程Ⅰ用
 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为③过程Ⅱ采用的分离方法和操作是
此过程中可以选用的溶剂是
a.乙醇b.四氯化碳c.水d.苯
您最近半年使用:0次



