8. 某工厂回收的锂离子电池废料的主要成分为钛酸锂(Li
4Ti
5O
12),也含C、Mn、Ni等元素。以该电池废料为原料可制备高纯度的碳酸锂和二氧化钛产品,工艺流程如下图所示。
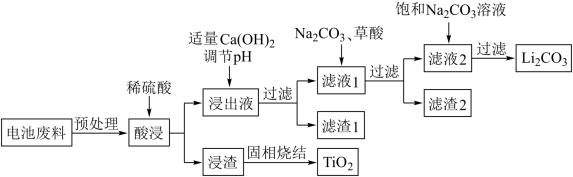
回答下列问题。
(1)对电池废料进行预处理,粉碎的目的是
__。
(2)“酸浸”后,锂进入浸出液,钛主要以正钛酸(H
4TiO
4,不溶于水)的形式存在。“酸浸”过程中生成正钛酸的化学方程式为
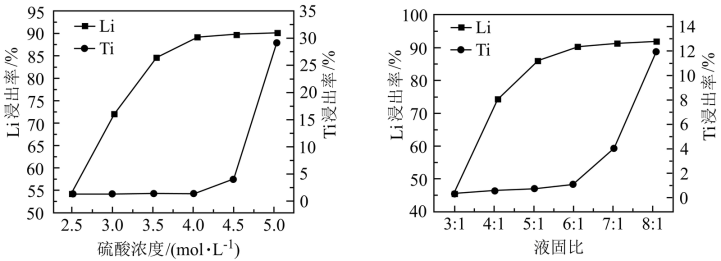
____。“酸浸”过程中,硫酸浓度、液固比对Li和Ti浸出率(进入溶液中的某元素质量占固体中该元素总质量的百分数)的影响如下图所示。其中最适宜的硫酸浓度及液固比分别为
__mol·L
-1、
___。
(3)已知25℃时,K
sp[Ni(OH)
2]=5.5×10
-16,K
sp[Mn(OH)
2]=1.9×10
-13.向“浸出液”中加入适量Ca(OH)
2调节溶液pH,除去溶有的少量Mn
2+、Ni
2+,当Mn
2+沉淀完全时(c=1×10
-5mol·L
-1),溶液中Ni
2+浓度为
__mol∙L
-1(保留小数点后1位)。结合生产实际分析,选择Ca(OH)
2而不选择NaOH作沉淀剂的原因是
_。
(4)向“滤液1”中加入适量Na
2CO
3溶液和草酸溶液,可生成两种沉淀,则“滤渣2”的成分为
___、
_____________。
(5)“浸渣”固相烧结生成TiO
2的化学方程式为
__。