11. 化学反应往往伴随着能量的变化,请完成以下问题
Ⅰ.已知:2H
2(g)+O
2(g)=2H
2O(g) ΔΗ=-483.6kJ·mol
-1 ,N
2(g)+2O
2(g)=2NO
2(g) ΔΗ=+67.7kJ·mol
-1;则反应4H
2(g)+2NO
2(g)=N
2(g)+4H
2O(g)的反应热ΔΗ=
_______。
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H
2(g) =CH
3OH(g),反应过程中的能量变化情况如图所示。
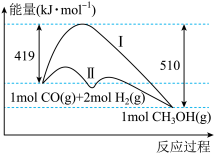
(1)曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。该反应是
_______(填“吸热”或“放热”)反应。计算当反应生成1.5molCH
3OH(g)时,能量变化值是
_______kJ。
(2)选择适宜的催化剂
_______(填“能”或“不能”)改变该反应的反应热。
(3)推测反应CH
3OH(g) =CO(g)+2H
2(g)是
_______(填“吸热”或“放热”)反应。
III.断开1molH—H键、1molN—H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH
2与足量N
2反应生成NH
3需
_______(填“吸收”或“放出”)能量
_______kJ。(小数点后保留两位数字),事实上,反应的热量总小于理论值,理由是
_______。