18. 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈发生反应:2NOCl+H
2O=NO+NO
2+2HCl,常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。某研究性学习小组在实验室中按照下图所示装置制备NOCl,并测定其纯度。请按照要求回答下列问题:
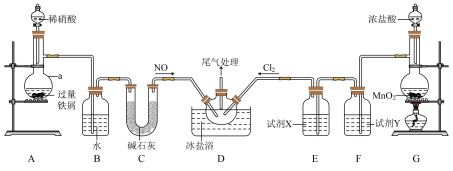
(1)a中反应的离子方程式为
_______。亚硝酰氯的结构式为
_______。
(2)装置D中,将三颈烧瓶浸在-10℃冰盐水中的目的是
_______。
(3)装置C、E中碱石灰和试剂X的作用是
_______。
(4)反应结束后用NaOH溶液吸收尾气,写出NOCl和NaOH的化学反应方程式:
_______。(已知:NO+NO
2+2NaOH=2NaNO
2+H
2O)。
(5)氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,反应产生黑色沉淀,写出该反应的离子反应方程式:
_______。
(6)测量产物NOCl的纯度:取三颈烧瓶中所得产物mg溶于水,配成250mL溶液,取出25.00mL,与VmLcmol·L
-1的AgNO
3溶液恰好完全反应,则产物中NOCl纯度的计算式为
_______。