2016届神州智达高三仿真模拟考试(1)理综化学试卷
全国
高三
一模
2017-07-27
940次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用、化学反应原理、化学实验基础、化学与STSE
2016届神州智达高三仿真模拟考试(1)理综化学试卷
全国
高三
一模
2017-07-27
940次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用、化学反应原理、化学实验基础、化学与STSE
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
1. 1856年,英国传教士威康臣先生在译著《格物探源》中提到:“天地万物皆以六十四种元质配合而成,如金银铜铁养轻淡炭等皆是元质,皆由微渺而造”,“ 微渺”即现代之“原子”。下列说法中不正确的是
| A.“元质”即现代之“元素”,现在人类发现的化学元素多于六十四种 |
| B.“养、轻、淡”即“氧、氢、氮”三种元素,现代的元素命名更具科学性 |
| C.上文中提到的八种“元质”包括四种金属“元质”和四种非金属“元质” |
| D.“微渺”因极其微小,故“微渺”是组成物质的基本微粒,不可再分 |
您最近一年使用:0次
2016-12-09更新
|
352次组卷
|
3卷引用:2016届神州智达高三仿真模拟考试(1)理综化学试卷
单选题
|
适中(0.65)
解题方法
2. 某有机物的结构简式为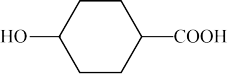 ,关于它的叙述中正确的是
,关于它的叙述中正确的是
 ,关于它的叙述中正确的是
,关于它的叙述中正确的是| A.1mol该有机物最多能够和2molNaOH发生反应 |
| B.和乙醇发生酯化反应时,羧基中的-OH将被CH3CH2-取代 |
| C.铜做催化剂并加热的条件下,羟基中的氢氧键会断裂 |
D.和 互为同分异构体 互为同分异构体 |
您最近一年使用:0次
单选题
|
适中(0.65)
3. NA为阿伏加德罗常数的值。下列说法中正确的是
| A.2.24L16O2中含有的中子数为1.6NA |
| B.23g乙醇中含有的共用电子对数为4NA |
| C.100mL1mol/L的Na2CO3溶液中含有的阴离子数为0.1NA |
| D.足量NaOH溶液吸收lmolCl2时,转移电子数为2NA |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 几种短周期元素的原子半径及主要化合价如下表:
下列叙述不正确的是
| 元素符号 | A | B | C | D | E |
| 原子半径/pm | 185 | 160 | 97 | 70 | 66 |
| 主要化合价 | +1 | +2 | -1 | -3,+3,+5 | -2 |
| A.元素A、B最高价氧化物对应的水化物的碱性A>B |
| B.一定条件下,D单质与E的常见单质直接生成DE2 |
| C.D、E和氢三种元素能够形成离子化合物 |
| D.A、E形成的化合物中可能含有两种不同类型的化学键 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 某兴趣小组做了“以铜为电极电解饱和食盐水”实验探究电解原理,装置如图所示。实验现象:接通电源30s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10,一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料(已知:相同温度下CuCl的溶解度大于CuOH)
下列说法错误的是

查阅资料(已知:相同温度下CuCl的溶解度大于CuOH)
| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜(不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
| A.电解过程中氯离子向阳极移动 |
| B.电解开始时阳极Cu 放电生成Cu2+ |
| C.阴极反应为2H2O+2e-=H2↑+2OH- |
| D.随溶液pH升高CuCl逐渐转化为CuOH |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 在实验室进行下列实验,括号内的实验用品都能用到的是
| 选项 | 实验 | 仪器用品 |
| A | 海带提取碘 | 分液漏斗、酒精灯、带铁圈的铁架台、烧杯 |
| B | 石油分馏 | 蒸发皿、酒精灯、冷凝管、锥形瓶 |
| C | 钠与乙醇的反应 | 试管、镊子、小刀、酒精灯 |
| D | 实验室制取乙酸乙酯 | 酒精灯、试管、铁架台、温度计 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.64)
7. 向盛有100mL2mol/L稀硫酸的烧杯中加入6g铁片,经一段时间后测得生成2.24L氢气(标准状况),若此时间段内用H2SO4表示该反应的平均反应速率为0.2 mol/(L·min)。下列说法正确的是
| A.生成了2.24L氢气(标准状况)的时间是5min |
| B.该时间段内用Fe表示该反应的平均反应速率为0.2mol/(L·min) |
| C.若反应开始时加入一些硫酸铜溶液,能够加快该反应速率且不影响生成氢气的总量 |
| D.若用等体积的浓硫酸代替2mol/L稀硫酸,能够加快该反应速率 |
【知识点】 影响化学反应速率的因素
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 乳酸( )是一种独特的调味剂,有很强的防腐、保鲜功效。常温下乳酸为无色液体,能与水、乙醇混溶。
)是一种独特的调味剂,有很强的防腐、保鲜功效。常温下乳酸为无色液体,能与水、乙醇混溶。
(1)将铜丝在空气中灼烧至表面呈黑色,趁热伸入乳酸中,铜丝的颜色变为______ ,证明乳酸分子中含有羟基。该反应的化学方程式为_____________________ 。
(2)请设计实验证明乳酸分子中含有羧基:_____________________ 。
(3)[CH3CH(OH)COO]2Fe(乳酸亚铁)是一种常用的补铁利,可通过乳酸与碳酸亚铁反应制得。如图装置(加热和夹持装置略去)A中装有稀硫酸,烧瓶B中装有铁屑,向三颈瓶C中加入碳酸亚铁固体和乳酸溶液并加热至75℃,将A中稀硫酸滴入B中开始反应。

①仪器A的名称是______________ 。
②仪器A、B组成的装置的作用是_______________ 。
③C中发生反应的化学方程式为_________________ 。
④该实验中尾气处理的方法为_________________ 。
⑤某兴趣小组用KMnO4滴定法测定样品中Fe2+含量进而计算产品中乳酸亚铁的质量分数,结果发现产品的质量分数总是大于100%,其原因可能是____________________ 。
 )是一种独特的调味剂,有很强的防腐、保鲜功效。常温下乳酸为无色液体,能与水、乙醇混溶。
)是一种独特的调味剂,有很强的防腐、保鲜功效。常温下乳酸为无色液体,能与水、乙醇混溶。(1)将铜丝在空气中灼烧至表面呈黑色,趁热伸入乳酸中,铜丝的颜色变为
(2)请设计实验证明乳酸分子中含有羧基:
(3)[CH3CH(OH)COO]2Fe(乳酸亚铁)是一种常用的补铁利,可通过乳酸与碳酸亚铁反应制得。如图装置(加热和夹持装置略去)A中装有稀硫酸,烧瓶B中装有铁屑,向三颈瓶C中加入碳酸亚铁固体和乳酸溶液并加热至75℃,将A中稀硫酸滴入B中开始反应。

①仪器A的名称是
②仪器A、B组成的装置的作用是
③C中发生反应的化学方程式为
④该实验中尾气处理的方法为
⑤某兴趣小组用KMnO4滴定法测定样品中Fe2+含量进而计算产品中乳酸亚铁的质量分数,结果发现产品的质量分数总是大于100%,其原因可能是
【知识点】 氧化还原反应有关计算 仪器使用与实验安全 物质的检验 综合实验设计与评价解读
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
9. 溴化钙易溶于水,易潮解.可用作阻燃剂、制冷剂。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:
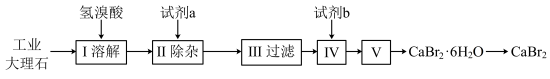
回答下列问题:
(1)若79Br原子的中子数是44 ,则Br-中的质子数是________ ;溴在元素周期表中的位置是_________ 。
(2)步骤I使用26%的氢溴酸来溶解大理石,在不改变氢溴酸的前提下,欲提高浸出速率,可采取的办法有:将块状大理石粉碎、搅拌、___________ 。
(3)已知步骤Ⅲ的滤液中不含NH ,步骤Ⅱ加入的试剂a是
,步骤Ⅱ加入的试剂a是 ______ ,之后还需控制溶液的pH约为8.0,目的是___________________ 。
(4)步骤Ⅳ中加入的试剂b是氢溴酸,其作用是调节溶液至中性。为了得到CaBr2·6H2O,步骤V所含的操作依次是_________ 、__________ 、过滤。
(5)所得产品溴化钙的纯度可以通过如下步骤测定:
①称取4.00g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应;④过滤、洗涤干燥;⑤称量。所得碳酸钙质量为1.56g,则溴化钙的质量分数为________ ,若实验操作不规范,使溴化钙样品部分潮解,则测定结果会_____ (填偏大、偏小或没有影响)。

回答下列问题:
(1)若79Br原子的中子数是44 ,则Br-中的质子数是
(2)步骤I使用26%的氢溴酸来溶解大理石,在不改变氢溴酸的前提下,欲提高浸出速率,可采取的办法有:将块状大理石粉碎、搅拌、
(3)已知步骤Ⅲ的滤液中不含NH
 ,步骤Ⅱ加入的试剂a是
,步骤Ⅱ加入的试剂a是 (4)步骤Ⅳ中加入的试剂b是氢溴酸,其作用是调节溶液至中性。为了得到CaBr2·6H2O,步骤V所含的操作依次是
(5)所得产品溴化钙的纯度可以通过如下步骤测定:
①称取4.00g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应;④过滤、洗涤干燥;⑤称量。所得碳酸钙质量为1.56g,则溴化钙的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
10. 研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭(石墨)作用生成CO,CO可用于炼铁等。
已知:①Fe2O3(s)+ 3C(石墨)=2Fe(s)+ 3CO(g)△H 1 = +489.0 kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) △H 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为__________________________ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
若向体积为1L的恒容密闭容器中按下表中三种投料方式投料,发生上述反应.反应温度对CO2平衡转化率影响的曲线(如下图)。
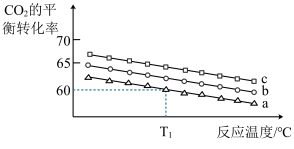
① 该反应的△H_______ 0(填“>”“<”或“=” ),曲线C对应的投料是第_________ 组。
② T1℃ 时,曲线a对应的化学平衡常数K=_________ (保留两位有效数字)。
③ 若500℃ 时该反应的平衡常数K= 2.5,T1℃________ 500℃ (填“>”“<”或“=”)。
(3)用电化学的方法也可以将CO2变废为宝,用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应式为____________ 。
(4)用石灰水就能够将CO2转变成CaCO3,若Ksp(CaCO3)=2.8×10-9,饱和石灰水的物质的量浓度为0.01mol/L,则向1L饱和石灰水中通入_______ mLCO2(标准状况),溶液中开始出现沉淀(不考虑反应过程中溶液体积的变化)。
(1)将CO2与焦炭(石墨)作用生成CO,CO可用于炼铁等。
已知:①Fe2O3(s)+ 3C(石墨)=2Fe(s)+ 3CO(g)△H 1 = +489.0 kJ·mol-1
②C(石墨)+CO2(g)=2CO(g) △H 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g)
 CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H若向体积为1L的恒容密闭容器中按下表中三种投料方式投料,发生上述反应.反应温度对CO2平衡转化率影响的曲线(如下图)。

| 组序号 | 1 | 2 | 3 |
| n(CO2) | 1mol | 1mol | 1mol |
| n(H2) | 3mol | 4mol | 6mol |
② T1℃ 时,曲线a对应的化学平衡常数K=
③ 若500℃ 时该反应的平衡常数K= 2.5,T1℃
(3)用电化学的方法也可以将CO2变废为宝,用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应式为
(4)用石灰水就能够将CO2转变成CaCO3,若Ksp(CaCO3)=2.8×10-9,饱和石灰水的物质的量浓度为0.01mol/L,则向1L饱和石灰水中通入
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
11. 铝铁合金可在某些航天器件中替代钛铝合金,大幅度降低成本。如下实验流程可利用废弃的钛铝合金制备聚合硫酸铁和明矾:

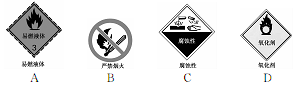
(1)流程中试剂X应为________ 溶液,发生反应的方程式为__________________ 。“浸泡、过滤”车间墙壁上应张贴如下哪种标志__________ (填写序号)。
(2)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是_________ 。
②浓缩时向其中加入一定量的乙醇,加入乙醇的目的是____________ 。
③加入试剂Y的目的是调节pH,所加试剂Y为___________ ;溶液的pH对[Fe2(OH)x(SO4)y]n中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因:___________ 。

(3)铝铁合金制品出厂前一般要经过“发黑”处理,工艺原理是在金属表面形成一层致密的金属氧化物薄膜,有助于合金的防腐,若用电解法对铝铁合金进行“发黑”处理,则铝铁合金制品应连接电解池的___________ (选填“阳极”或“阴极”)。
(4)若11.0g某铝铁合金样品溶于足量盐酸,标准状况下放出8.96L气体,则合金中铝、铁的物质的量之比为___________ 。

(1)流程中试剂X应为

(2)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是
②浓缩时向其中加入一定量的乙醇,加入乙醇的目的是
③加入试剂Y的目的是调节pH,所加试剂Y为

(3)铝铁合金制品出厂前一般要经过“发黑”处理,工艺原理是在金属表面形成一层致密的金属氧化物薄膜,有助于合金的防腐,若用电解法对铝铁合金进行“发黑”处理,则铝铁合金制品应连接电解池的
(4)若11.0g某铝铁合金样品溶于足量盐酸,标准状况下放出8.96L气体,则合金中铝、铁的物质的量之比为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
12. 氧化锌(ZnO)、氮化镓(GaN)等组成的新型多相催化剂能利用可见光将水分解成氢气和氧气。

(1)氧原子最外层上电子云形状有_________ 种,原子中所有电子共占有__________ 个原子轨道。
(2)氧、氮两种元素中,电负性较大的是__________ ,试从原子结构角度解释其原因:_________________ 。在“冰融化成水”的过程中,被破坏的微粒间的作用主要是____________ 。
(3)基态Zn2+核外电子排布式为____________________ ,ZnO有三种晶体结构,某种ZnO晶体的晶胞如图1所示,熔点1975℃(分解),沸点2360℃,则此种ZnO固体属于_______ 晶体,晶胞中与O2-距离最近的Zn2+有_________ 个,ZnO是两性氧化物,能跟强碱溶液反应生成[Zn(OH)4]2-,不考虑空间构型,[Zn(OH)4]2-的结构可用示意图表示为___________ 。
(4)氮化镓的晶体结构如图2所示,其中氮原子的杂化轨道类型是___________ ;N、Ga原子之间存在配位键,该配位键中提供电子对的原子是____________ 。

(1)氧原子最外层上电子云形状有
(2)氧、氮两种元素中,电负性较大的是
(3)基态Zn2+核外电子排布式为
(4)氮化镓的晶体结构如图2所示,其中氮原子的杂化轨道类型是
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
解题方法
13. 有机物H具有很好的弹性、耐磨性和电绝缘性,常原来制作纤维或无纺布等,由甲苯制取有机物H或有机物E的合成路线如图所示:

已知:
(1)
(2)CH3CHO+CH3CHO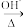 CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
(3)化合物A苯环上的一氯代物只有两种。
(4)两分子G 能形成六元环酯。
请回答下列问题:
(1)有机物A的结构简式是_____________ ,C中含有的官能团有______________ (写名称)。
(2)③的反应条件是___________ 。④的反应类型为______________ 。
(3)写出B与新制Cu(OH)2反应的化学方程式_____________ .
(4)化合物E的核磁共振氢谱显示有_________ 个峰,一个E分子中最多有_________ 个碳原子位于同一平面。
(5)化合物G有多种同分异构体,化合物G同时满足以下三种条件的同分异构体(除G外)还有_________ 种,请任意写出其中一种的结构简式____________ 。
①苯环上只有两个取代基且苯环上的一氯取代物只有两种;
②具有和G相同的官能团;
③能够发生消去反应
(6)参照题干的合成路线,请设计由乙醛为起始原料制备丁酸的合成终线(无机试剂任选):__________ 。

已知:
(1)

(2)CH3CHO+CH3CHO
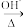 CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O(3)化合物A苯环上的一氯代物只有两种。
(4)两分子G 能形成六元环酯。
请回答下列问题:
(1)有机物A的结构简式是
(2)③的反应条件是
(3)写出B与新制Cu(OH)2反应的化学方程式
(4)化合物E的核磁共振氢谱显示有
(5)化合物G有多种同分异构体,化合物G同时满足以下三种条件的同分异构体(除G外)还有
①苯环上只有两个取代基且苯环上的一氯取代物只有两种;
②具有和G相同的官能团;
③能够发生消去反应
(6)参照题干的合成路线,请设计由乙醛为起始原料制备丁酸的合成终线(无机试剂任选):
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用、化学反应原理、化学实验基础、化学与STSE
试卷题型(共 13题)
题型
数量
单选题
7
解答题
6
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 元素符号、元素名称的书写 化学用语综合判断 原子的构成 元素、核素、同位素 | |
| 2 | 0.65 | 同分异构现象、同分异构体的概念 酯化反应 醇的催化氧化 羧酸化学性质 | |
| 3 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 物质结构中化学键数目的计算 | |
| 4 | 0.65 | 过氧化钠 元素周期律、元素周期表的推断 金属与非金属在周期表中位置及其性质递变的规律 离子晶体 | |
| 5 | 0.65 | 电解池概念及组成 电解原理 电解原理的应用 综合实验设计与评价 | |
| 6 | 0.65 | 乙醇与钠反应的机理 乙酸乙酯制备实验的装置及操作 蒸馏与分馏 海带中碘的提取及检验 | |
| 7 | 0.64 | 影响化学反应速率的因素 | |
| 二、解答题 | |||
| 8 | 0.65 | 氧化还原反应有关计算 仪器使用与实验安全 物质的检验 综合实验设计与评价 | 实验探究题 |
| 9 | 0.65 | 元素周期表结构 常见无机物的制备 | 工业流程题 |
| 10 | 0.65 | 盖斯定律与热化学方程式 化学平衡的有关计算 溶度积常数相关计算 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 11 | 0.65 | 盐类水解的应用 电解原理 仪器使用与实验安全 常见无机物的制备 | 工业流程题 |
| 12 | 0.65 | 物质结构与性质综合考查 元素性质与电负性的关系 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 13 | 0.4 | 同分异构体的数目的确定 有机分子中原子共面的判断 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |



