19. 铝镁合金已成为轮船制造、化工生产等行业的重要材料。某研究性学习小组的三位同学为测定某含镁3%~5%的铝铁合金(不含其他元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。(已知:金属镁的性质活泼,能与空气中的氮气和二氧化碳反应。)
探究一
实验方案:
(1)铝镁合金

测定剩余固体质量。实验中发生反应的化学方程式是
___________。
称取5.4g铝镁合金粉末样品,投入体积为v浓度为2.0mol/L的NaOH溶液中,充分反应。为保证合金充分反应,NaOH溶液的体积V≥
___________mL。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
___________(填“偏大”或“偏小”)。
(3)如何洗涤沉淀:
___________。
探究二
实验方案:铝镁合金
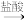
测定生成气体的体积(实验装置如图所示)。

(4)某同学提出该实验装置不够完善,应在A、B之间添加一个除酸雾的装置。你的意见是
___________(填“需要”或“不需要”)。
(5)为使测定结果尽可能精确,实验中应注意的问题有:___________
| A.检查装置的气密性 |
| B.加入足量盐酸 |
| C.调整量气管C的高度,使C中液面与B中液面相平 |
| D.待冷却至室温再读体积。 |
探究三
实验方案:称量xg铝镁合金粉末,放入装有足量氧气的容器中使其充分灼烧。
(6)欲计算镁的质量分数,该实验中还需测定的数据是
___________。
(7)若用空气代替O
2进行实验,对测定结果是否有影响?
___________(填“是”或“否”)。