河南省TOP二十名校2024届高三下学期5月冲刺(一)理综试卷-高中化学
河南
高三
模拟预测
2024-05-21
181次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、物质结构与性质、化学反应原理、化学实验基础
河南省TOP二十名校2024届高三下学期5月冲刺(一)理综试卷-高中化学
河南
高三
模拟预测
2024-05-21
181次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 2023年是共建“一带一路”倡议提出10周年。下列古代“丝绸之路”有关商品的主要成分属于无机物的是
| A.玉器 | B.丝绸 | C.香料 | D.皮草 |
【知识点】 无机物与有机物解读 化学科学对人类文明发展的意义解读
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
2. 我国科研团队合成的一种抗病毒的天然仿生有机物(G)的结构如图所示。下列叙述正确的是
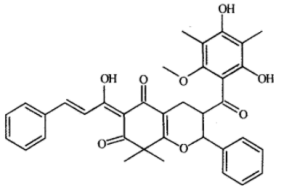
| A.G分子含3个手性碳原子 |
| B.G中有3种官能团 |
C.G遇 溶液发生显色反应 溶液发生显色反应 |
| D.G分子中所有碳原子可能共平面 |
【知识点】 常见官能团名称、组成及结构解读
您最近一年使用:0次
单选题
|
适中(0.65)
3. 法莫替丁片是一种治疗消化性溃疡病的药物,其有效成分(T)的结构简式如图所示。下列叙述正确的是
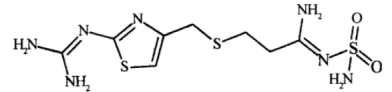
A.T中N原子都是 杂化,S原子都是 杂化,S原子都是 杂化 杂化 |
B. 中N原子最多能与质子 中N原子最多能与质子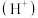 形成 形成 配位键 配位键 |
C. 分子含 分子含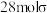 键 键 |
D.第一电离能: |
您最近一年使用:0次
单选题
|
较难(0.4)
名校
解题方法
4. 某小组采用电化学法制备有机物,装置如图所示。双极膜是由阴膜和阳膜组成的,双极膜中水电离出的阴、阳离子在电场中向两极迁移。下列叙述正确的是

| A.a极与电源负极连接 |
B.制备1mol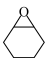 时双极膜内质量减少18g 时双极膜内质量减少18g |
C.b极的电极反应式为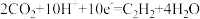 |
D.每转移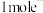 ,生成 ,生成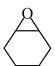 、 、 的物质的量之比为1:5 的物质的量之比为1:5 |
您最近一年使用:0次
2024-02-02更新
|
432次组卷
|
4卷引用:广东省湛江市2023-2024学年高三上学期1月期末化学试题
广东省湛江市2023-2024学年高三上学期1月期末化学试题福建省厦门第一中学2023-2024学年高三下学期2月第一次月考化学试卷(已下线)化学(天津卷03)-2024年高考化学押题预测卷河南省TOP二十名校2024届高三下学期5月冲刺(一)理综试卷-高中化学
单选题
|
适中(0.65)
5. 根据下列实验操作和现象,得出结论正确的是
| 选项 | 操作及现象 | 结论 |
| A | 在 溶液中滴加盐酸酸化的 溶液中滴加盐酸酸化的 溶液,产生白色沉淀 溶液,产生白色沉淀 | 原溶液含有 |
| B | 在锌和稀硫酸的混液中滴 浊液,产生气体速率加快 浊液,产生气体速率加快 |  作催化剂 作催化剂 |
| C | 在苯酚浊液中滴加 溶液,振荡,溶液变澄清 溶液,振荡,溶液变澄清 | 苯环活化了羟基 |
| D | 镁条能在干冰制作灯笼中剧烈燃烧,发出白光 |  能支持燃料燃烧 能支持燃料燃烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 以氯化亚铁为催化剂,可催化三氟甲基烯烃硼化一脱氟反应合成偕二氟烯丙基硼酸酯,可能的反应机理如图所示(已知: 、
、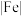 代表
代表 )。
)。
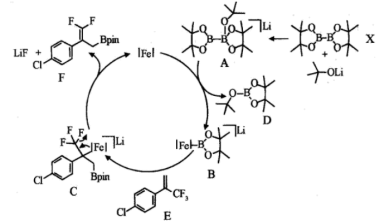
A.该合成反应的原子利用率为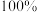 |
| B.物质D分子中氧硼原子构成平面三角形 |
| C.A和X分子在核磁共振氢谱上都只有1组峰 |
D.将E替换为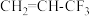 ,反应可得 ,反应可得 |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 常温下,分别在 溶液中滴加
溶液中滴加 溶液,
溶液, ,X代表
,X代表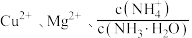 与
与 关系如图所示。已知:
关系如图所示。已知: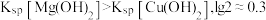 。下列叙述错误的是
。下列叙述错误的是
 溶液中滴加
溶液中滴加 溶液,
溶液, ,X代表
,X代表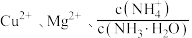 与
与 关系如图所示。已知:
关系如图所示。已知: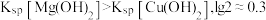 。下列叙述错误的是
。下列叙述错误的是
A. 代表 代表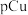 与 与 的关系 的关系 |
B.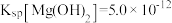 |
C.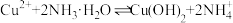 的平衡常数 的平衡常数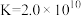 |
D.M点对应的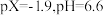 |
您最近一年使用:0次
2024-05-21更新
|
43次组卷
|
2卷引用:河南省TOP二十名校2024届高三下学期5月冲刺(一)理综试卷-高中化学
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
8. 纯镍常用作锂离子电池的正极材料以及有机合成的催化剂。以废镍合金为原料(主要成分是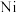 和
和 ,还有少量
,还有少量 和
和 等)制备高纯度镍的流程如下:
等)制备高纯度镍的流程如下: 升高,
升高, 被氧化速率增大,同时
被氧化速率增大,同时 水解生成
水解生成 胶体增多且能吸附
胶体增多且能吸附 。回答下列问题:
。回答下列问题:
(1)“酸浸”中稀硫酸的作用有调节 、减少
、减少 胶体、
胶体、_______ 。
(2)“氧化”中 的作用是
的作用是_______ (用离子方程式表示)。该过程通常需控制 小于3的条件下进行,
小于3的条件下进行, 为
为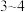 时镍的回收率降低,其主要原因是
时镍的回收率降低,其主要原因是_______ 。
(3)已知:常温下,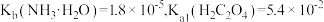 ,
,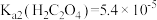 。
。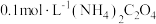 溶液
溶液
_______ (填“>”“<”或“=”)7,此溶液中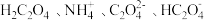 浓度由大到小排序为
浓度由大到小排序为_______ 。
(4)制备等质量 ,还原
,还原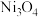 的
的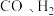 的质量之比为
的质量之比为_______ 。
(5)工业上,提纯镍粉的原理是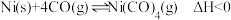 ,如图所示(分子膜只允许气体分子通过,不允许固体杂质和镍粉通过)。
,如图所示(分子膜只允许气体分子通过,不允许固体杂质和镍粉通过)。
_______ (填“>”“<”或“=”) ,判断依据是
,判断依据是_______ 。
(6)铌镍合金可用于喷射引擎、燃气涡轮发动机、火箭组件和耐热燃烧器材等,在航空航天领域有着重要应用。一种铌镍合金晶胞如图所示。_______  (只列计算式即可)。
(只列计算式即可)。
 和
和 ,还有少量
,还有少量 和
和 等)制备高纯度镍的流程如下:
等)制备高纯度镍的流程如下: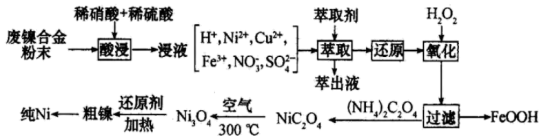
 升高,
升高, 被氧化速率增大,同时
被氧化速率增大,同时 水解生成
水解生成 胶体增多且能吸附
胶体增多且能吸附 。回答下列问题:
。回答下列问题:(1)“酸浸”中稀硫酸的作用有调节
 、减少
、减少 胶体、
胶体、(2)“氧化”中
 的作用是
的作用是 小于3的条件下进行,
小于3的条件下进行, 为
为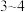 时镍的回收率降低,其主要原因是
时镍的回收率降低,其主要原因是(3)已知:常温下,
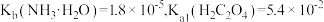 ,
,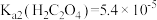 。
。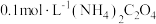 溶液
溶液
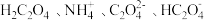 浓度由大到小排序为
浓度由大到小排序为(4)制备等质量
 ,还原
,还原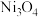 的
的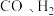 的质量之比为
的质量之比为(5)工业上,提纯镍粉的原理是
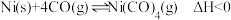 ,如图所示(分子膜只允许气体分子通过,不允许固体杂质和镍粉通过)。
,如图所示(分子膜只允许气体分子通过,不允许固体杂质和镍粉通过)。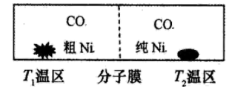

 ,判断依据是
,判断依据是(6)铌镍合金可用于喷射引擎、燃气涡轮发动机、火箭组件和耐热燃烧器材等,在航空航天领域有着重要应用。一种铌镍合金晶胞如图所示。
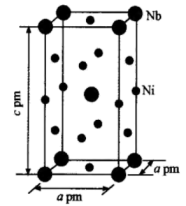
 (只列计算式即可)。
(只列计算式即可)。
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
9. 过二硫酸钾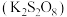 是一种常用的氧化剂。某小组设计实验制备
是一种常用的氧化剂。某小组设计实验制备 、探究其性质并测定
、探究其性质并测定 产品纯度。回答下列问题:
产品纯度。回答下列问题:
实验(一):制备 。
。
实验原理: ,装置如图所示。
,装置如图所示。 溶于
溶于 蒸馏水中,然后冷却溶液至
蒸馏水中,然后冷却溶液至 以下,将
以下,将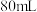 溶液轻轻倒入大试管中,装上铂丝阳极、铂片阴极。试管围置在烧杯的冰盐浴中,通电(
溶液轻轻倒入大试管中,装上铂丝阳极、铂片阴极。试管围置在烧杯的冰盐浴中,通电(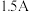 左右的电流)2小时。将沉淀收集在小的砂芯漏斗中(不能用水洗涤),抽干晶体,相继用乙醇和乙醚洗涤,在干燥器内干燥,称重。
左右的电流)2小时。将沉淀收集在小的砂芯漏斗中(不能用水洗涤),抽干晶体,相继用乙醇和乙醚洗涤,在干燥器内干燥,称重。
实验现象:电解过程中,阴极产生气体,阳极也逸出微量气体,溶液中析出晶体。
(1)已知阳极放电顺序: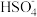 优先于
优先于 。阳极最先发生的电极反应式为
。阳极最先发生的电极反应式为_______ 。电解过程中,阴、阳极产生气体体积比_______ (填“大于”“小于”或“等于”)  (同温同压)。
(同温同压)。
实验(二):探究 的性质。
的性质。
(2)实验a说明 在沸水中不稳定,与水反应生成
在沸水中不稳定,与水反应生成 和
和_______ (填化学式)。
(3)实验b说明 具有
具有_______ 性,写出离子方程式:_______ ,此反应是检验 的特征反应。
的特征反应。
实验(三):测定 产品纯度。
产品纯度。
称取 产品溶于水配制
产品溶于水配制 溶液,准确量取
溶液,准确量取 配制溶液于锥形瓶中,加入过量
配制溶液于锥形瓶中,加入过量 溶液,振荡,滴几滴淀粉溶液,用
溶液,振荡,滴几滴淀粉溶液,用 标准
标准 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 。有关反应为
。有关反应为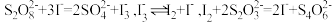 。
。
(4)本实验滴定终点现象是_______ 。
(5)该产品纯度为_______  。若其他操作均正确,滴定前仰视读数,终点时俯视读数,则测得结果
。若其他操作均正确,滴定前仰视读数,终点时俯视读数,则测得结果_______ (填“偏高”“偏低”或“无影响”)。
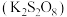 是一种常用的氧化剂。某小组设计实验制备
是一种常用的氧化剂。某小组设计实验制备 、探究其性质并测定
、探究其性质并测定 产品纯度。回答下列问题:
产品纯度。回答下列问题:实验(一):制备
 。
。实验原理:
 ,装置如图所示。
,装置如图所示。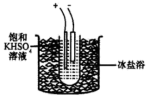
 溶于
溶于 蒸馏水中,然后冷却溶液至
蒸馏水中,然后冷却溶液至 以下,将
以下,将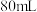 溶液轻轻倒入大试管中,装上铂丝阳极、铂片阴极。试管围置在烧杯的冰盐浴中,通电(
溶液轻轻倒入大试管中,装上铂丝阳极、铂片阴极。试管围置在烧杯的冰盐浴中,通电(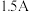 左右的电流)2小时。将沉淀收集在小的砂芯漏斗中(不能用水洗涤),抽干晶体,相继用乙醇和乙醚洗涤,在干燥器内干燥,称重。
左右的电流)2小时。将沉淀收集在小的砂芯漏斗中(不能用水洗涤),抽干晶体,相继用乙醇和乙醚洗涤,在干燥器内干燥,称重。实验现象:电解过程中,阴极产生气体,阳极也逸出微量气体,溶液中析出晶体。
(1)已知阳极放电顺序:
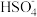 优先于
优先于 。阳极最先发生的电极反应式为
。阳极最先发生的电极反应式为 (同温同压)。
(同温同压)。实验(二):探究
 的性质。
的性质。| 序号 | 实验操作及现象 |
| a | 加热 溶液至沸腾,有气体生成,一段时间后,冷却至常温;取少量溶液,测定溶液 溶液至沸腾,有气体生成,一段时间后,冷却至常温;取少量溶液,测定溶液 。向该溶液中滴加盐酸酸化,再滴加 。向该溶液中滴加盐酸酸化,再滴加 溶液,产生白色沉淀。 溶液,产生白色沉淀。 |
| b | 在 溶液中滴加 溶液中滴加 溶液,振荡,无明显现象;再滴加几滴 溶液,振荡,无明显现象;再滴加几滴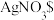 浊液(作催化剂),溶液变紫红色。 浊液(作催化剂),溶液变紫红色。 |
 在沸水中不稳定,与水反应生成
在沸水中不稳定,与水反应生成 和
和(3)实验b说明
 具有
具有 的特征反应。
的特征反应。实验(三):测定
 产品纯度。
产品纯度。称取
 产品溶于水配制
产品溶于水配制 溶液,准确量取
溶液,准确量取 配制溶液于锥形瓶中,加入过量
配制溶液于锥形瓶中,加入过量 溶液,振荡,滴几滴淀粉溶液,用
溶液,振荡,滴几滴淀粉溶液,用 标准
标准 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 。有关反应为
。有关反应为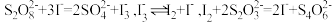 。
。(4)本实验滴定终点现象是
(5)该产品纯度为
 。若其他操作均正确,滴定前仰视读数,终点时俯视读数,则测得结果
。若其他操作均正确,滴定前仰视读数,终点时俯视读数,则测得结果
您最近一年使用:0次
10. 乙醛 是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:
是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:
(1)已知:①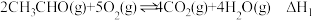
②
③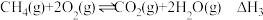
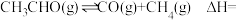
_______ 。
(2)在镍催化下,乙醛与氢气反应生成乙醇。在恒温恒容反应器中充入一定量 和
和 发生反应:
发生反应: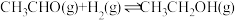 。下列叙述错误的是_______(填标号)。
。下列叙述错误的是_______(填标号)。
(3) 速率方程
速率方程 (k为速率常数,只与温度、催化剂有关;n为反应级数)。
(k为速率常数,只与温度、催化剂有关;n为反应级数)。
①阿伦尼乌斯就关于速率常数与活化能 、温度(T)的关系提出经验关系式:
、温度(T)的关系提出经验关系式: (R为常数,k为速率常数,
(R为常数,k为速率常数, 为活化能,T为温度)。一定温度下,在
为活化能,T为温度)。一定温度下,在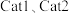 (催化剂)作用下,
(催化剂)作用下,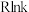 与
与 关系如图所示。
关系如图所示。_______ (填“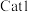 ”或“
”或“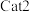 ”),判断依据是
”),判断依据是_______ 。
②为了测定反应级数(n),实验测得 在一系列不同浓度时的初始反应速率数据如下:
在一系列不同浓度时的初始反应速率数据如下:
已知:一步进行的反应称为基元反应,基元反应中反应级数等于反应物的化学计量数之和。下列叙述正确的是_______ (填标号)。
A.该总反应为二级反应
B.速率常数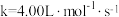
C.上述反应不是基元反应
D.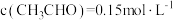 时
时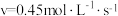
(4)一定温度下,保持总压强为 ,向反应器充入
,向反应器充入 和
和 的混合气体(
的混合气体( 不参与反应)发生反应
不参与反应)发生反应 ,测得
,测得 平衡转化率与起始投料比
平衡转化率与起始投料比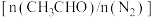 的关系如图所示。
的关系如图所示。 的平衡转化率随着投料比增大而减小的原因是
的平衡转化率随着投料比增大而减小的原因是_______ 。该温度下,上述反应M点平衡常数
_______  。(
。( 为用分压计算的平衡常数,分压=总压×物质的量分数)
为用分压计算的平衡常数,分压=总压×物质的量分数)
(5) 时,向反应器充入一定量
时,向反应器充入一定量 发生反应
发生反应 ,测得单位时间内
,测得单位时间内 转化率与压强关系如图所示。解释
转化率与压强关系如图所示。解释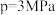 时
时 的转化率达到峰值的原因:
的转化率达到峰值的原因:_______ 。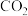 制备乙醛,其阴极的电极反应式为
制备乙醛,其阴极的电极反应式为_______ 。
 是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:
是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:(1)已知:①
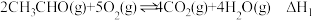
②

③
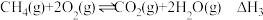
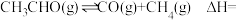
(2)在镍催化下,乙醛与氢气反应生成乙醇。在恒温恒容反应器中充入一定量
 和
和 发生反应:
发生反应: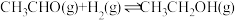 。下列叙述错误的是_______(填标号)。
。下列叙述错误的是_______(填标号)。| A.气体压强不随时间变化时达到平衡状态 |
| B.平衡后充入氖气,平衡向逆反应方向移动 |
| C.上述可逆反应的正反应是嫡增反应 |
D.平衡后,充入少量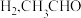 平衡转化率增大 平衡转化率增大 |
(3)
 速率方程
速率方程 (k为速率常数,只与温度、催化剂有关;n为反应级数)。
(k为速率常数,只与温度、催化剂有关;n为反应级数)。①阿伦尼乌斯就关于速率常数与活化能
 、温度(T)的关系提出经验关系式:
、温度(T)的关系提出经验关系式: (R为常数,k为速率常数,
(R为常数,k为速率常数, 为活化能,T为温度)。一定温度下,在
为活化能,T为温度)。一定温度下,在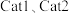 (催化剂)作用下,
(催化剂)作用下,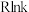 与
与 关系如图所示。
关系如图所示。
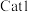 ”或“
”或“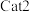 ”),判断依据是
”),判断依据是②为了测定反应级数(n),实验测得
 在一系列不同浓度时的初始反应速率数据如下:
在一系列不同浓度时的初始反应速率数据如下: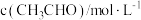 | 0.1 | 0.2 | 0.3 | 0.4 |
 | 0.020 | 0.080 | 0.182 | 0.318 |
A.该总反应为二级反应
B.速率常数
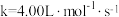
C.上述反应不是基元反应
D.
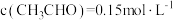 时
时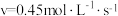
(4)一定温度下,保持总压强为
 ,向反应器充入
,向反应器充入 和
和 的混合气体(
的混合气体( 不参与反应)发生反应
不参与反应)发生反应 ,测得
,测得 平衡转化率与起始投料比
平衡转化率与起始投料比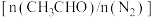 的关系如图所示。
的关系如图所示。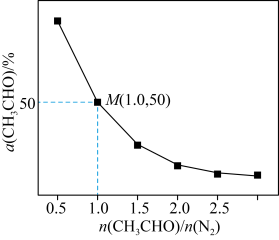
 的平衡转化率随着投料比增大而减小的原因是
的平衡转化率随着投料比增大而减小的原因是
 。(
。( 为用分压计算的平衡常数,分压=总压×物质的量分数)
为用分压计算的平衡常数,分压=总压×物质的量分数)(5)
 时,向反应器充入一定量
时,向反应器充入一定量 发生反应
发生反应 ,测得单位时间内
,测得单位时间内 转化率与压强关系如图所示。解释
转化率与压强关系如图所示。解释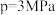 时
时 的转化率达到峰值的原因:
的转化率达到峰值的原因: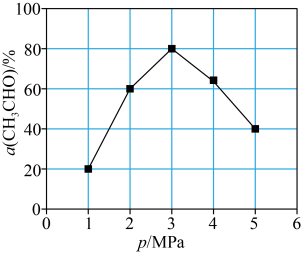
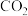 制备乙醛,其阴极的电极反应式为
制备乙醛,其阴极的电极反应式为
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
解题方法
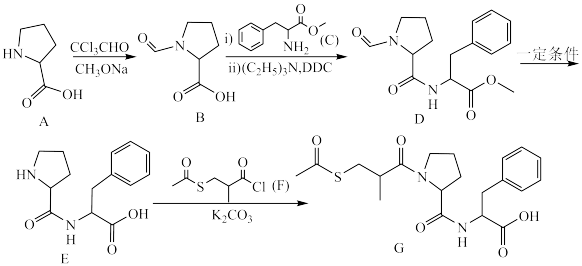
11. 阿拉普利(G)是血管紧张转化酶抑制剂,一种合成路线如下:
(1)G中 杂化的原子除C外还有
杂化的原子除C外还有_____ ,A的沸点高于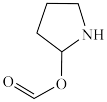 ,其原因是
,其原因是_____ 。
(2)C中所含官能团有_______ (填名称)。
(3) 同时生成氯仿,其反应类型是
同时生成氯仿,其反应类型是_______ , 中
中 的作用是
的作用是_______ 。
(4)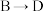 的化学方程式为
的化学方程式为_______ 。
(5)在B的同分异构体中,同时具备下列条件的结构有(不包括立体异构体)_______ (填标号)。
①含五元环且环上含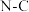 键;②
键;② 有机物与足量银氨溶液共热最多生成
有机物与足量银氨溶液共热最多生成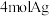 ;③含有酯基。
;③含有酯基。
a.10种 b.11种 c.12种 d.13种
(6)已知: 。以对二甲苯、
。以对二甲苯、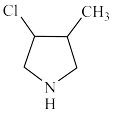 为原料合成
为原料合成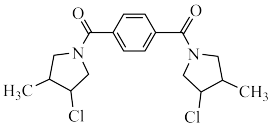 ,设计合成路线:
,设计合成路线:_______ 。(其他试剂自选)
(1)G中
 杂化的原子除C外还有
杂化的原子除C外还有 ,其原因是
,其原因是(2)C中所含官能团有
(3)
 同时生成氯仿,其反应类型是
同时生成氯仿,其反应类型是 中
中 的作用是
的作用是(4)
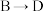 的化学方程式为
的化学方程式为(5)在B的同分异构体中,同时具备下列条件的结构有(不包括立体异构体)
①含五元环且环上含
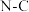 键;②
键;② 有机物与足量银氨溶液共热最多生成
有机物与足量银氨溶液共热最多生成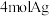 ;③含有酯基。
;③含有酯基。a.10种 b.11种 c.12种 d.13种
(6)已知:
 。以对二甲苯、
。以对二甲苯、 为原料合成
为原料合成 ,设计合成路线:
,设计合成路线:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、化学与STSE、有机化学基础、物质结构与性质、化学反应原理、化学实验基础
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 无机物与有机物 化学科学对人类文明发展的意义 | |
| 2 | 0.94 | 常见官能团名称、组成及结构 | |
| 3 | 0.65 | 电离能变化规律 利用杂化轨道理论判断分子的空间构型 简单配合物的成键 | |
| 4 | 0.4 | 电解原理的应用 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | |
| 5 | 0.65 | 催化剂对化学反应速率的影响 苯酚的弱酸性 化学实验方案的设计与评价 | |
| 6 | 0.65 | 核磁共振氢谱 有机物的合成 利用杂化轨道理论判断分子的空间构型 | |
| 7 | 0.65 | 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 溶度积规则及其应用 | |
| 二、解答题 | |||
| 8 | 0.4 | 盐溶液中离子浓度大小的比较 晶胞的有关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 酸碱中和滴定原理的应用 电解池电极反应式及化学方程式的书写与判断 物质含量的测定 | 实验探究题 |
| 10 | 0.15 | 盖斯定律与热化学方程式 催化剂对化学反应速率的影响 化学平衡的移动及其影响因素 化学平衡常数的有关计算 | 原理综合题 |
| 11 | 0.65 | 有机反应类型 根据要求书写同分异构体 根据题给物质选择合适合成路线 多官能团有机物的结构与性质 | 有机推断题 |



