山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
山东
高一
期末
2018-03-02
383次
整体难度:
容易
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础
山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
山东
高一
期末
2018-03-02
383次
整体难度:
容易
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
您最近一年使用:0次
单选题
|
较易(0.85)
4. 下列问题与氮的氧化物的排放无关的是
| A.酸雨 | B.温室效应 |
| C.光化学烟雾 | D.臭氧空洞 |
您最近一年使用:0次
单选题
|
较易(0.85)
5. 下列变化中,需要加入适当的还原剂才能完成的是
| A.FeCl3→FeCl2 | B.Cu→Cu2(OH)2CO3 |
| C.SO3→H2SO4 | D.HCl→Cl2 |
【知识点】 氧化还原反应的应用
您最近一年使用:0次
2018-02-24更新
|
174次组卷
|
4卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题(已下线)【走进新高考】(人教版必修一)第二章 化学计量在实验中的应用 单元练习02新疆巴州三中2018-2019学年高一上学期期末考试化学试题新疆喀什第二中学2018-2019学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
6. 同温同压下,在两个容积相同的容器中,一个盛有CO2气体,另一个盛有N2和CO的混合气体。两容器内的气体一定具有相同的
| A.原子数 | B.密度 | C.质量 | D.分子数 |
【知识点】 阿伏加德罗定律的应用解读
您最近一年使用:0次
2018-02-24更新
|
169次组卷
|
3卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第一单元 从实验学化学单元测试 A卷江西省赣州市会昌县第五中学2020-2021学年高一上学期第二次月考化学试题
单选题
|
较易(0.85)
名校
7. 《本草纲目拾遗》中在药物名“鼻冲水”条目下写道:“贮以玻璃瓶,紧塞其口,勿使漏气,则药力不减。气甚辛烈,触人脑,非有病不可嗅”;在“刀创水”条目下写道:“治金创,此水涂伤口,好敛合如故”。这里所说的“鼻冲水”“刀创水”分别指的是
| A.氢氟酸、食盐水 | B.食醋、石灰水 | C.氨水、碘酒 | D.稀硫酸、稀硝酸 |
【知识点】 化学科学对人类文明发展的意义解读
您最近一年使用:0次
2018-02-24更新
|
198次组卷
|
2卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
单选题
|
适中(0.65)
8. 在实验室里按如图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则R是
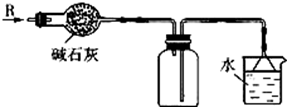

| A.H2 | B.NH3 | C.Cl2 | D.HCl |
【知识点】 常见气体的制备与收集解读
您最近一年使用:0次
单选题
|
较易(0.85)
9. 下列关于试剂保存的说法中错误的是
| A.浓硝酸保存在棕色试剂瓶中,放阴凉冷暗处 |
| B.液溴保存在棕色磨口试剂瓶中,并加入少量水密封保存 |
| C.烧碱溶液保存在用玻璃塞的玻璃试剂瓶中 |
| D.氢氟酸保存在抗酸塑料瓶中 |
【知识点】 仪器使用与实验安全
您最近一年使用:0次
单选题
|
适中(0.65)
10. 向100 mL 18 mol•L-1的H2SO4溶液中加入足量的铜片并加热,充分反应后,生成SO2气体的物质的量为
| A.小于0.90 mol | B.0.90 mol |
| C.1.80 mol | D.大于0.90 mol小于1.80 mol |
【知识点】 硫酸
您最近一年使用:0次
单选题
|
适中(0.65)
11. 对下列事实的解释错误的是
| A.氨气极易溶于水,氨气能够做“喷泉”实验 |
| B.常温下,浓硝酸可用铝罐来贮存,说明常温下浓硝酸不与铝发生反应 |
| C.向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有脱水性 |
| D.氯气不能使干的有色布条褪色,能使湿润的有色布条褪色,说明次氯酸具有漂白性 |
您最近一年使用:0次
单选题
|
适中(0.65)
12. 下列有关实验的描述中,错误的是
| A.钠在氧气或氯气中燃烧,都能观察到黄色火焰 |
| B.钠放入水中后,沉在水下缓缓冒出气体 |
| C.为了检验某FeCl2溶液是否变质,可取少量溶液加入KSCN溶液观察是否变红 |
| D.向某溶液中加入烧碱溶液,加热后生成使湿润红色石蕊试纸变蓝的气体,说明原溶液中有NH4+ |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 下列关于铜及其化合物的说法中不正确的是
| A.高温下黑色的氧化铜转化为红色氧化亚铜,说明氧化亚铜热稳定性强于氧化铜 |
| B.铜在干燥的空气中性质稳定,但在潮湿的空气中易被腐蚀,生成铜绿 |
| C.无水硫酸铜可用来检验水蒸气的存在 |
| D.铜与氯气、氧气和硫分别反应,得到产物中铜的化合价均为+2价 |
【知识点】 铜的其他化合物
您最近一年使用:0次
单选题
|
适中(0.65)
您最近一年使用:0次
单选题
|
适中(0.65)
名校
15. 下列实验结果与图像不相符的是


| A.向含有盐酸、氯化镁和氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量 |
| B.向澄清石灰水中通入二氧化碳气体直至过量 |
| C.向氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量 |
| D.向氯化铝的溶液中逐渐加入氨水直至过量 |
您最近一年使用:0次
2018-02-24更新
|
804次组卷
|
5卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
单选题
|
较易(0.85)
名校
16. 下列离子方程式的书写正确的是
| A.铁片投入稀硫酸中2Fe+6H+ = 2Fe 3++3H2↑ |
| B.食醋与氨水反应:NH3·H2O+H+= NH4++H2O |
| C.过量铁粉与稀硝酸反应:3Fe+8H++2NO3-= 3Fe 2++2NO↑+4H2O |
| D.向Ba(OH)2溶液滴加NaHSO4溶液至Ba2+恰好沉淀:Ba2++2H++2OH-+SO42- = BaSO4↓+2H2O |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2018-02-24更新
|
139次组卷
|
2卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
单选题
|
适中(0.65)
名校
解题方法
18. 某溶液中有Cu2+、Mg2+、Fe2+和Al3+四种离子,若向其中加入足量的过氧化钠搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
| A.Cu2+ | B.Mg2+ | C.Fe2+ | D.Al3+ |
您最近一年使用:0次
2021-01-02更新
|
125次组卷
|
5卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
19. 材料与生产、生活和科技密切相关。回答下列问题:
(1)复合材料中往往一种材料作为基体,另一种材料作为增强剂。下列物质中属于复合材料的是_________ (填标号)。
A.钢化玻璃 B.玻璃钢 C.钢筋混凝土 D.玻璃
(2)无机非金属材料与我们的生活联系密切。我国具有独立知识产权的电脑芯片“龙芯一号”填补了我国计算机史上空白,“龙芯一号”材料的化学式为______ ;传统的无机非金属材料在日常生活中有着广泛的运用。玻璃和水泥的生产中均用到的原料的名称是____ ,其中碳酸钠在玻璃熔炉中反应的化学方程式为____________ 。
(3)随着科学技术的发展,具有特殊结构、功能的新型无机非金属材料被研制出来。碳化硅陶瓷(SiC)是一种耐高温陶瓷,反应原理为SiO2+3C SiC+2CO↑,氧化剂与还原剂的物质的量之比为
SiC+2CO↑,氧化剂与还原剂的物质的量之比为________ 。
(4)金属材料的应用更是广泛。①工业常用30%FeCl3溶液腐蚀绝缘板上铜箔,制造印刷电路板。腐蚀废液中含有Fe3+、Fe2+、Cu2+离子。当向腐蚀液中加入足量的Fe粉,一定不存在的离子是_________ ;用实验判定腐蚀液中含有Fe2+离子_____________ 。
②某硬铝合金中含有铝、镁、铜、硅,下图为测定硬铝合金中铝的含量的流程图:
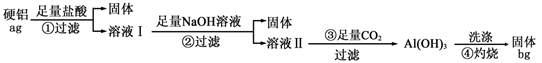
由溶液Ⅰ生成溶液Ⅱ中的溶质的离子方程式为__________________ ;该合金中铝的含量为_________ 。
(1)复合材料中往往一种材料作为基体,另一种材料作为增强剂。下列物质中属于复合材料的是
A.钢化玻璃 B.玻璃钢 C.钢筋混凝土 D.玻璃
(2)无机非金属材料与我们的生活联系密切。我国具有独立知识产权的电脑芯片“龙芯一号”填补了我国计算机史上空白,“龙芯一号”材料的化学式为
(3)随着科学技术的发展,具有特殊结构、功能的新型无机非金属材料被研制出来。碳化硅陶瓷(SiC)是一种耐高温陶瓷,反应原理为SiO2+3C
 SiC+2CO↑,氧化剂与还原剂的物质的量之比为
SiC+2CO↑,氧化剂与还原剂的物质的量之比为(4)金属材料的应用更是广泛。①工业常用30%FeCl3溶液腐蚀绝缘板上铜箔,制造印刷电路板。腐蚀废液中含有Fe3+、Fe2+、Cu2+离子。当向腐蚀液中加入足量的Fe粉,一定不存在的离子是
②某硬铝合金中含有铝、镁、铜、硅,下图为测定硬铝合金中铝的含量的流程图:

由溶液Ⅰ生成溶液Ⅱ中的溶质的离子方程式为
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
20. 实验是进行化学研究的重要手段之一。请回答下列问题:
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是_________ (填标号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有________________ 。
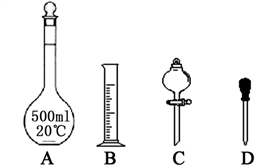
②在容量瓶的使用方法中,下列操作正确的是_______ (填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃 棒引流注入容量瓶中,然后加水。
棒引流注入容量瓶中,然后加水。
(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。
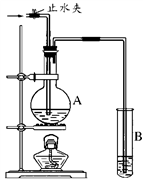
①向A中通入足量的SO2气体,然后加热,A中的现象_____________ 。
②向A中通入足量的Cl2气体,然后加热,A中的现象是_____________ 。
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是______________________ 。
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为____________ ;B中发生反应的离子方程式__________________________________________ 。
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是

②在容量瓶的使用方法中,下列操作正确的是
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃
 棒引流注入容量瓶中,然后加水。
棒引流注入容量瓶中,然后加水。(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。

①向A中通入足量的SO2气体,然后加热,A中的现象
②向A中通入足量的Cl2气体,然后加热,A中的现象是
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为
【知识点】 一定物质的量浓度的溶液的配制 化学实验探究 物质性质的探究解读
您最近一年使用:0次
四、填空题 添加题型下试题
填空题
|
适中(0.65)
21. 善于归纳元素及其化合物之间的转化关系,对学习元素化合物具有重要意义。回答下列问题:
(1)置换反应是中学常见基本反应类型之一。
①写出金属单质置换出非金属单质的离子反应方程式_____________ ;
②写出非金属单质置换出非金属单质的化学方程式_____________ 。
(2)“三角转化”是单质及其化合物之间相互转化中常见的转化关系之一。现有如图转化关系。
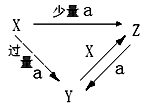
①若Z是一种能够与血红蛋白结合造成人体缺氧的气体。则a的名称为___________ ;
②若X是一种常见金属单质,a为一种含氧酸。Y转化为Z的离子方程式___________ 。
③若X是一种强碱,a是一种酸性氧化物。Z转化为Y的离子反应方程式____________ ;
(3)在下图的转化关系中,A、B、C、D、E为含有一种相同元素的五种物质。
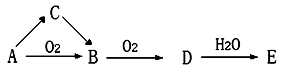
①若A为淡黄色固体单质,则B→D的化学方程式为_____________ ;
②若A常温下为气体单质,收集气体B采用的方法为________ ;若将32 g铜投入稍过量的E的浓溶液中,产生气体的体积为11.2 L(STP),参加反应的硝酸的物质的量为_____ ;
(1)置换反应是中学常见基本反应类型之一。
①写出金属单质置换出非金属单质的离子反应方程式
②写出非金属单质置换出非金属单质的化学方程式
(2)“三角转化”是单质及其化合物之间相互转化中常见的转化关系之一。现有如图转化关系。

①若Z是一种能够与血红蛋白结合造成人体缺氧的气体。则a的名称为
②若X是一种常见金属单质,a为一种含氧酸。Y转化为Z的离子方程式
③若X是一种强碱,a是一种酸性氧化物。Z转化为Y的离子反应方程式
(3)在下图的转化关系中,A、B、C、D、E为含有一种相同元素的五种物质。

①若A为淡黄色固体单质,则B→D的化学方程式为
②若A常温下为气体单质,收集气体B采用的方法为
您最近一年使用:0次
五、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
22. 制取物质、探究物质的性质是学习化学必备的素养之一。
回答下列问题。
(1)实验室从含碘废液(除水外含CCl4、I2、I-等)中回收碘,其实验流程如下。

回答下列问题:
①物质X的名称为________ ;
②操作Ⅰ选用的装置为______ (填标号);
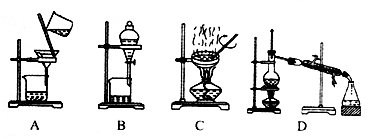
③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为___ 。
④氧化剂Y可用Cl2,也可以用H2O2。将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为________ 。
(2)某研究小组查阅资料知:氧化性的强弱顺序为:Cl2>IO3->I2。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。
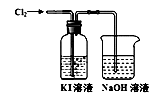
①NaOH溶液的作用是______ ,反应的离子方程式为___________ 。
②溶液由黄色最后变为无色所发生反应的离子方程式为____________ 。
回答下列问题。
(1)实验室从含碘废液(除水外含CCl4、I2、I-等)中回收碘,其实验流程如下。

回答下列问题:
①物质X的名称为
②操作Ⅰ选用的装置为

③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为
④氧化剂Y可用Cl2,也可以用H2O2。将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为
(2)某研究小组查阅资料知:氧化性的强弱顺序为:Cl2>IO3->I2。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。

①NaOH溶液的作用是
②溶液由黄色最后变为无色所发生反应的离子方程式为
【知识点】 氧化还原反应的应用 氧化还原反应有关计算 物质分离、提纯综合应用解读
您最近一年使用:0次
2018-02-24更新
|
546次组卷
|
4卷引用:山东省枣庄市薛城区2017-2018学年高一上学期期末化学试题
试卷分析
整体难度:适中
考查范围:化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 22题)
题型
数量
单选题
18
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 海水资源综合利用 | |
| 2 | 0.85 | 非电解质、电解质物质类别判断 | |
| 3 | 0.85 | 胶体的性质和应用 | |
| 4 | 0.85 | 硫、氮氧化物对人体、环境的危害 酸雨 大气污染来源及危害 | |
| 5 | 0.85 | 氧化还原反应的应用 | |
| 6 | 0.65 | 阿伏加德罗定律的应用 | |
| 7 | 0.85 | 化学科学对人类文明发展的意义 | |
| 8 | 0.65 | 常见气体的制备与收集 | |
| 9 | 0.85 | 仪器使用与实验安全 | |
| 10 | 0.65 | 硫酸 | |
| 11 | 0.65 | 氯气 氨气 浓硫酸的脱水性 铝的钝化 | |
| 12 | 0.65 | 铵根离子的检验 钠 铁盐的检验 | |
| 13 | 0.65 | 铜的其他化合物 | |
| 14 | 0.65 | 综合实验设计与评价 | |
| 15 | 0.65 | 含镁化合物 其他含铝化合物 铝盐与强碱溶液反应 | |
| 16 | 0.85 | 离子方程式的正误判断 | |
| 17 | 0.65 | 钠的化学性质 过氧化钠 铝热反应 | |
| 18 | 0.65 | 过氧化钠与水的反应 含镁化合物 铝盐与强碱溶液反应 Fe2+的还原性 | |
| 二、填空题 | |||
| 19 | 0.65 | 二氧化硅的化学性质 铝盐与强碱溶液反应 Fe2+的鉴别及其应用 | |
| 21 | 0.65 | 四种基本反应类型 无机综合推断 含硫化合物之间的转化 铁的其他化合物 | |
| 三、解答题 | |||
| 20 | 0.65 | 一定物质的量浓度的溶液的配制 化学实验探究 物质性质的探究 | 实验探究题 |
| 22 | 0.65 | 氧化还原反应的应用 氧化还原反应有关计算 物质分离、提纯综合应用 | 实验探究题 |

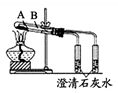 判定碳酸钠比碳酸氢钠稳定性
判定碳酸钠比碳酸氢钠稳定性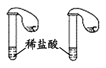 鉴别碳酸钠和碳酸氢钠
鉴别碳酸钠和碳酸氢钠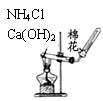 实验室制取氨气
实验室制取氨气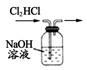 除去氯气中的氯化氢
除去氯气中的氯化氢

