10. 甲醇是一种可再生能源,又是一种重要的化工原料.具有广阔的开发和应用前景。工业上可用如下方法合成甲醇:CO(g)+2H
2(g)

CH
3OH(g).
(1)已知:①2CH
3OH(l)+3O
2(g)

2CO
2(g)+4H
2O(g) △H=-1275.6kJ·mol
-1;
②2CO(g)+O
2(g)

2CO
2(g) △H=-566.0kJ·mol
-1;
③H
2O(l)=H
2O(g) △H=+44.0kJ·mol
-1.
则甲醇液体不完全燃烧生成CO和液态水的热化学方程式为
__________。
(2)在一定温度下,向2L密闭容器中充人1mol CO和2mol H
2,发生反应CO(g)+2H
2(g)
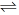
CH
3OH(g),5min反应达到平衡,此时CO的转化率为80%。
①前5min内甲醇的平均反应速率为
__________;已知该反应在低温下能自发进行,则反应的△H
_______0(填“>”“<”或“=”)。
②在该温度下反应的平衡常数K=
__________。
③某时刻向该平衡体系中加入CO、H
2、CH
3OH各0.2mol后,则v
正__________v
逆(填“>”“=”或“<”)。
④当反应达到平衡时,
__________(填字母)。
a.混合气体的压强不再发生变化b.反应物不再转化为生成物
c.v
正(CO)=2v
逆(H
2) d.v(H
2)=2v(CH
3OH)
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3) "甲醇---过氧化氢燃料电池"的结构主要包括燃料腔、氧化剂腔和质子交换膜三部分.放电过程中其中一个腔中生成了CO
2。
①放电过程中生成H
+的反应,发生在
__________腔中,该腔中的电极反应式为
__________.
②该电池工作过程中,当消耗甲醇4.8g时.电路中通过的电量为
__________(法拉第常数F=9.65×10
4C·mol
-1)