河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
河北
高一
阶段练习
2020-04-18
300次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、物质结构与性质、认识化学科学
河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
河北
高一
阶段练习
2020-04-18
300次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、物质结构与性质、认识化学科学
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
1. 从2019年烧到2020年的澳大利亚山火终于熄灭了,在此次火灾中产生了大量的大气污染物:①浓烟中的炭粒 ②氮的氧化物 ③碳的氧化物 ④硫的氧化物,其中会导致雨水酸化的有害、有毒气体是
| A.①③ | B.②④ | C.③④ | D.①② |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
2. 下列说法正确的是
| A.化学反应中的能量变化都表现为热量变化 |
| B.化学反应发生过程中一定有能量变化 |
| C.放热反应在常温条件下一定都能发生 |
| D.化学反应吸收或放出热量的多少与参加反应的物质的多少无关 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
3. 下列粒子含有的电子数和质子数均与F— 的相同的是
| A.OH- | B.Na+ | C.H2O | D.NH4+ |
【知识点】 原子的基本构成解读 原子中相关数值及其之间的相互关系解读
您最近一年使用:0次
2020-04-15更新
|
68次组卷
|
2卷引用:河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
单选题
|
较易(0.85)
名校
4. 下列对化学反应的理解不正确的是
| A.从化学键的角度分析,化学反应中一定有旧键的断裂和新键的形成 |
| B.从能量的角度分析,化学反应中一定有能量的变化 |
| C.从物质的种类分析,化学反应中一定有新物质的生成 |
| D.从微观角度分析,化学反应中一定有分子种类的变化 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
5. 下列关于物质分类的叙述正确的是
| A.凡是含有共价键的化合物一定是共价化合物 |
| B.凡是含有离子键的化合物一定是离子化合物 |
| C.凡是非金属单质一定含有共价键 |
| D.凡是含氧酸都是强电解质 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
7. 短周期主族元素X、Y 具有相同的电子层数且原子序数Y>X,下列有关叙述正确的是
| A.若X、Y 形成的常见简单离子分别为X+ 、Y3+ ,则离子半径:X+ <Y3+ |
| B.若X的最高价含氧酸是强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的常见单质在常温下是气体,则 Y元素形成的常见单质在常温下一定也是气体 |
| D.若X(OH)m 是强碱,则Y(OH)n 也一定是强碱 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
8. 下列关于氢键及范德华力的叙述正确的是
| A.氢键比范德华力强,它们都属于化学键 |
| B.分子间形成的氢键会使物质的熔点和沸点升高 |
| C.HF分子间只存在氢键,没有范德华力 |
| D.由于 HF分子间存在氢键,所以 HF比 H2O 更稳定 |
【知识点】 分子间作用力 氢键 氢键概念及特征解读 氢键对物质性质的影响解读
您最近一年使用:0次
2020-04-15更新
|
167次组卷
|
3卷引用:河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
单选题
|
较易(0.85)
名校
9. 下列变化中有化学键的断裂的是
| A.HCl溶于水 | B.酒精的挥发 | C.干冰的升华 | D.裁剪布料 |
【知识点】 化学键与化学反应中的能量关系解读 常见能量转化形式解读
您最近一年使用:0次
2020-04-15更新
|
480次组卷
|
4卷引用:河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
单选题
|
适中(0.65)
名校
10. 对于反应2Na2O2+2H2O = 4NaOH+O2↑中化学键的变化判断正确的是
| A.只有离子键的断裂和形成 |
| B.只有共价键的断裂和形成 |
| C.既有离子键和共价键的断裂,又有离子键和共价键的形成 |
| D.既有离子键和极性键的断裂,又有离子键和极性键的形成 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
11. 下列关于40Ar、40K、40Ca说法正确的是
| A.具有相同的质子数 |
| B.具有相同的质量数 |
| C.具有相同的中子数 |
| D.互为同位素 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
12. 下列热化学方程式中,△H 能正确表示对应物质的燃烧热的是
A.CO2 (g)=CO(g)+ O2(g) △H=+283.0kJ·mol-1 O2(g) △H=+283.0kJ·mol-1 |
B.S(s)+ O2(g)=SO3(g) △H=-396kJ·mol-1 O2(g)=SO3(g) △H=-396kJ·mol-1 |
C.H2(g)+ O2(g)=H2O(g) △H=-241.8kJ·mol-1 O2(g)=H2O(g) △H=-241.8kJ·mol-1 |
| D.CH4(g)+2O2(g) = CO2(g)+2H2O(l) △H =—890.3kJ·mol-1 |
【知识点】 表示燃烧热的热化学方程式书写解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
13. 卤素互化物具有和卤素相似的化学性质。下列有关BrCl的说法错误的是
| A.BrCl中的溴元素显+1价 |
| B.BrCl中的原子均符合8电子稳定结构 |
| C.BrCl、Cl2、Br2 的熔、沸点大小:Br2>BrCl>Cl2 |
| D.BrCl与 H2O 反应的生成物为 HBr和 HClO |
【知识点】 拟卤素解读 同主族元素性质递变规律理解及应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
14. 已知:C(s)的燃烧热△H = —393.5kJ·mol—1,C(s)+  O2 (g) = CO(g) △H = —110.5kJ·mol—1。测得某次实验中m g炭粉燃烧所得气体中,CO 和 CO2的体积比为1:2,则与这些炭完全燃烧(只生成CO2)相比较,损失的能量是
O2 (g) = CO(g) △H = —110.5kJ·mol—1。测得某次实验中m g炭粉燃烧所得气体中,CO 和 CO2的体积比为1:2,则与这些炭完全燃烧(只生成CO2)相比较,损失的能量是
 O2 (g) = CO(g) △H = —110.5kJ·mol—1。测得某次实验中m g炭粉燃烧所得气体中,CO 和 CO2的体积比为1:2,则与这些炭完全燃烧(只生成CO2)相比较,损失的能量是
O2 (g) = CO(g) △H = —110.5kJ·mol—1。测得某次实验中m g炭粉燃烧所得气体中,CO 和 CO2的体积比为1:2,则与这些炭完全燃烧(只生成CO2)相比较,损失的能量是A.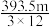 kJ kJ | B.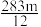 kJ kJ | C.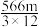 kJ kJ | D.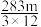 kJ kJ |
【知识点】 燃烧热的计算解读 依据热化学方程式的计算解读
您最近一年使用:0次
2020-04-15更新
|
100次组卷
|
2卷引用:河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
单选题
|
较易(0.85)
名校
15. 氯氨铂是一种治疗癌症的常用化学药物,具有较高疗效。其中的金属Pt(铂元素)是原子序数为78(质量数为195)的原子,则Pt的中子数与质子数之差是
| A.117 | B.78 | C.39 | D.0 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
16. 与 W 相邻的X、Y、Z三种短周期主族元素,其中X、Y、Z三种元素最外层电子数之和为18,Y的最高正价与最低负价的代数和为6,X、W 同主族。下列说法不正确的是
| A.X与 W 可以形成 WX2、WX3 两种常见化合物 |
| B.Z元素最高价氧化物对应水化物的化学式为 H3ZO4 |
| C.Y 的简单氢化物的沸点比X的简单氢化物的沸点高 |
| D.Y、Z、W 的原子半径大小:Z>W>Y |
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
17. 能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,2gC2H2(g)完全燃烧生成液态水时放出的热量是100kJ,则C2H2燃烧的热化学方程式是_________________________ 。
(2)已知:C(石墨,s)+O2(g) = CO2(g) △H = —393.5kJ·mol—1,C(金刚石,s)+ O2(g) =CO2(g) △H =—395.0kJ·mol—1,则反应C(石墨,s) = C(金刚石,s) △H =______ kJ·mol—1。由此可知,石墨和金刚石相比更稳定的是 _______ (填“石墨”或“金刚石”)。
(3)已知H2(g)的燃烧热△H 1=—285.0kJ·mol—1,CO(g)的燃烧热△H 2=—283.0kJ·mol—1, CH3OH(l)的燃烧热△H3=—726.0kJ·mol—1。0.2mol由H2 和CO组成的混合气体在完全燃烧时放出56.8kJ的能量,则混合气体中H2 和CO的质量比为_________ 。工业上在催化剂的作用下,可用H2(g)和CO(g)合成CH3OH(l)。请写出由H2(g)和CO(g)合成CH3OH(l)的热化学方程式:_______________________ 。
(4)强酸和强碱的稀溶液的中和热可表示为 H+ (aq)+OH— (aq) = H2O(l) △H =—57.3kJ·mol—1。已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) △H =—33.1kJ·mol—1。请写出醋酸溶液电离的热化学方程式:_______________ 。
(1)在25℃、101kPa时,2gC2H2(g)完全燃烧生成液态水时放出的热量是100kJ,则C2H2燃烧的热化学方程式是
(2)已知:C(石墨,s)+O2(g) = CO2(g) △H = —393.5kJ·mol—1,C(金刚石,s)+ O2(g) =CO2(g) △H =—395.0kJ·mol—1,则反应C(石墨,s) = C(金刚石,s) △H =
(3)已知H2(g)的燃烧热△H 1=—285.0kJ·mol—1,CO(g)的燃烧热△H 2=—283.0kJ·mol—1, CH3OH(l)的燃烧热△H3=—726.0kJ·mol—1。0.2mol由H2 和CO组成的混合气体在完全燃烧时放出56.8kJ的能量,则混合气体中H2 和CO的质量比为
(4)强酸和强碱的稀溶液的中和热可表示为 H+ (aq)+OH— (aq) = H2O(l) △H =—57.3kJ·mol—1。已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) △H =—33.1kJ·mol—1。请写出醋酸溶液电离的热化学方程式:
您最近一年使用:0次
填空题
|
适中(0.65)
名校
解题方法
18. 现有下列物质,请在横线上按要求归类(填序号)
①H2 ②He ③KOH ④CO2 ⑤H2O2 ⑥CaCl2
(1)只由极性键构成的物质是__________________ ;
(2)只由离子键构成的物质是____________________ ;
(3)只由非极性键构成的物质是_____________ ;
(4)由离子键和极性键构成的物质是____________ ;
(5)由极性键和非极性键构成的物质是______________ ;
(6)不含化学键的是_____________ 。
①H2 ②He ③KOH ④CO2 ⑤H2O2 ⑥CaCl2
(1)只由极性键构成的物质是
(2)只由离子键构成的物质是
(3)只由非极性键构成的物质是
(4)由离子键和极性键构成的物质是
(5)由极性键和非极性键构成的物质是
(6)不含化学键的是
您最近一年使用:0次
2020-04-18更新
|
198次组卷
|
2卷引用:河北省石家庄市新乐第一中学2019-2020学年高一下学期调研化学试题
三、解答题 添加题型下试题
解答题-无机推断题
|
较难(0.4)
名校
解题方法
19. 通过简单地推理或计算填空。
(1)X原子有两个电子层,K 层电子数是L层电子数的一半,X是_______ (写元素符号)元素。
(2)若某元素形成的简单离子的电子层数和最外层电子数与 Ne原子相同,其可能的离子中半径最小的是__________ (填离子符号)。
(3)元素R能够与某非金属元素 W 形成化合物 RWn,已知 RWn 分子中各原子核外最外层电子总数为26,核外电子数总和为66 ,则 W 是___________ (写元素符号)元素,n=_____________ 。
(4)位于三个不同周期的四种短周期主族元素 A、B、C、D,其部分元素特征信息如下表:
①写出常温下D的单质与A、B、C形成的化合物的稀溶液反应的化学方程式:________________ 。
②D的最高价氧化物对应的水化物与 A、B、C形成的化合物的水溶液反应的离子方程式为________________________ 。
(1)X原子有两个电子层,K 层电子数是L层电子数的一半,X是
(2)若某元素形成的简单离子的电子层数和最外层电子数与 Ne原子相同,其可能的离子中半径最小的是
(3)元素R能够与某非金属元素 W 形成化合物 RWn,已知 RWn 分子中各原子核外最外层电子总数为26,核外电子数总和为66 ,则 W 是
(4)位于三个不同周期的四种短周期主族元素 A、B、C、D,其部分元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,其单质是空气的主要成分之一 |
| C | 在短周期主族元素中金属性最强 |
| D | 最高价氧化物对应水化物的酸性最强 |
①写出常温下D的单质与A、B、C形成的化合物的稀溶液反应的化学方程式:
②D的最高价氧化物对应的水化物与 A、B、C形成的化合物的水溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
名校
解题方法
20. 已知X、Y、Z、W 是中学化学中常见的四种不同粒子,其中X、W 为分子,Y、Z为离子它们之间存在如下所示的转化关系:
X+Y→Z+W Z+H+ →X Y+H+ →W
(1)如果X、Y、Z、W 均是10电子的粒子,请写出:
X的电子式:____________ ; W 的电子式:_________________ 。
(2)如果X和Z均是18电子的粒子,Y 和 W 均是10电子的粒子,请写出:
①X与Y(足量)在溶液中反应的离子方程式:______________________ 。
②根据上述离子方程式,可判断Z与 Y 结合质子(H+ )的能力大小是________ >_____ 。(用化学式或离子符号表示)
X+Y→Z+W Z+H+ →X Y+H+ →W
(1)如果X、Y、Z、W 均是10电子的粒子,请写出:
X的电子式:
(2)如果X和Z均是18电子的粒子,Y 和 W 均是10电子的粒子,请写出:
①X与Y(足量)在溶液中反应的离子方程式:
②根据上述离子方程式,可判断Z与 Y 结合质子(H+ )的能力大小是
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
21. 原子序数由小到大排列的四种短周期元素 A、B、C、D,四种元素的原子序数之和为32,B、C元素的常见单质是空气的主要成分,A 的一种同位素无中子
(1)D元素是_____________ (填元素符号)
(2)B、C、D分别与 A组成的最简单化合物中沸点最高的是__________ (填化学式) 。
(3)A、B、C三种元素能组成一种常见强酸,该强酸的稀溶液能与铜反应,写出该反应的离子方程式:____________ 。
(4)由 A、B、C、D四种元素可以组成多种离子化合物
①若离子化合物X(其各元素组成为 A5BC4D)能与足量 NaOH 浓溶液反应写出X的化学式:___________________________ .
在含有X的溶液中滴入几滴 NaOH 溶液并加热无气体生成,其可能的原因是_______________________________________ .
②若离子化合物Y(其各元素组成为 A8B2C3D)既能与盐酸反应,又能与氯水反应,写出Y与氯水反应的离子方程式:__________________ .
(5)由 A、C、D和Fe四种元素组成的相对分子质量为278的化合物Z,1molZ中含有7mol结晶水 Z的化学式为_______________________ 。
(1)D元素是
(2)B、C、D分别与 A组成的最简单化合物中沸点最高的是
(3)A、B、C三种元素能组成一种常见强酸,该强酸的稀溶液能与铜反应,写出该反应的离子方程式:
(4)由 A、B、C、D四种元素可以组成多种离子化合物
①若离子化合物X(其各元素组成为 A5BC4D)能与足量 NaOH 浓溶液反应写出X的化学式:
在含有X的溶液中滴入几滴 NaOH 溶液并加热无气体生成,其可能的原因是
②若离子化合物Y(其各元素组成为 A8B2C3D)既能与盐酸反应,又能与氯水反应,写出Y与氯水反应的离子方程式:
(5)由 A、C、D和Fe四种元素组成的相对分子质量为278的化合物Z,1molZ中含有7mol结晶水 Z的化学式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、化学反应原理、物质结构与性质、认识化学科学
试卷题型(共 21题)
题型
数量
单选题
16
填空题
2
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硫、氮氧化物对人体、环境的危害 酸雨 大气污染来源及危害 | |
| 2 | 0.85 | 能量的相互转化 化学键与化学反应中的能量关系 常见能量转化形式 | |
| 3 | 0.85 | 原子的基本构成 原子中相关数值及其之间的相互关系 | |
| 4 | 0.85 | 化学反应中能量变化的原因 能量的相互转化 化学键与化学反应中的能量关系 | |
| 5 | 0.85 | 强电解质与弱电解质 共价键与离子键的比较 化学键与物质类别关系的判断 | |
| 6 | 0.85 | 吸热反应和放热反应 | |
| 7 | 0.65 | 由元素性质的递变规律进行相关推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 8 | 0.85 | 分子间作用力 氢键 氢键概念及特征 氢键对物质性质的影响 | |
| 9 | 0.85 | 化学键与化学反应中的能量关系 常见能量转化形式 | |
| 10 | 0.65 | 化学键与化学反应中的能量关系 化学键概念理解及判断 化学键与化学反应本质联系 | |
| 11 | 0.85 | 原子的基本构成 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 12 | 0.65 | 表示燃烧热的热化学方程式书写 | |
| 13 | 0.65 | 拟卤素 同主族元素性质递变规律理解及应用 | |
| 14 | 0.65 | 燃烧热的计算 依据热化学方程式的计算 | |
| 15 | 0.85 | 原子的构成 核素 | |
| 16 | 0.65 | 同周期元素性质递变规律理解及应用 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 二、填空题 | |||
| 17 | 0.65 | 化学反应热的计算 化学能与物质稳定性之间的关系 热化学方程式书写及正误判断 盖斯定律的应用 | |
| 18 | 0.65 | 化学键概念理解及判断 离子键概念及判断 共价键概念及判断 | |
| 三、解答题 | |||
| 19 | 0.4 | 氯气与碱溶液反应 元素周期律、元素周期表的推断 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | 无机推断题 |
| 20 | 0.65 | 原子、离子、原子团及其电子式的书写与判断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | 无机推断题 |
| 21 | 0.4 | 同周期元素性质递变规律 同主族元素性质递变规律 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | 有机推断题 |



