铁及其化合物在生产、生活中有广泛应用。
(1)铁原子核外有__________ 种运动状态不同的电子,Fe3+基态核外电子排布式为_______________ 。
(2)实验室常用K3[Fe(CN)6]检验Fe2+,[Fe(CN)6]3-中三种元素电负性由大到小的顺序为________ (用元素符号表示),CN-中σ键与π键的数目比n(σ)∶n(π)=__________ ;HCN中C原子轨道的杂化类型为__________ 。HCN的沸点为25.7℃,既远大于N2的沸点(-195.8℃)也大于HCl的沸点(-85℃)的原因是__________ 。
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子(Fe2Cl6)存在,该双聚分子的结构式为________ ,其中Fe的配位数为_____________ 。
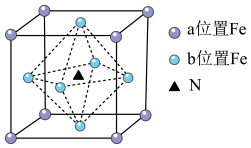
(4)铁氮化合物(Fe4N)在磁记录材料领域有着广泛的应用前景,其晶胞如上图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中b位置Fe原子的坐标为(0, ,
, )、(
)、( ,0,
,0, )和(
)和( ,
, ,0),则a位置Fe原子和N原子的坐标分别为
,0),则a位置Fe原子和N原子的坐标分别为__________ 、__________ 。N与Fe原子之间最短距离a pm。设阿伏加 德罗常数的值为NA,则该铁氮化合物的密度是__________ g·cm-3(列出计算表达式)。
(1)铁原子核外有
(2)实验室常用K3[Fe(CN)6]检验Fe2+,[Fe(CN)6]3-中三种元素电负性由大到小的顺序为
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子(Fe2Cl6)存在,该双聚分子的结构式为

(4)铁氮化合物(Fe4N)在磁记录材料领域有着广泛的应用前景,其晶胞如上图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中b位置Fe原子的坐标为(0,
 ,
, )、(
)、( ,0,
,0, )和(
)和( ,
, ,0),则a位置Fe原子和N原子的坐标分别为
,0),则a位置Fe原子和N原子的坐标分别为
更新时间:2020-04-28 15:41:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W四种元素位于元素周期表前四周期,原子序数依次增大。基态X原子价电子排布式为 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
(1) 分子的空间构型为
分子的空间构型为_______ 。
(2)阴离子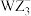 中W原子的杂化类型为
中W原子的杂化类型为_______ 。
(3) 的沸点比Z同主族其他元素氢化物高,原因是
的沸点比Z同主族其他元素氢化物高,原因是_______ 。
(4) 分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为_______ 。
 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。(1)
 分子的空间构型为
分子的空间构型为(2)阴离子
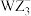 中W原子的杂化类型为
中W原子的杂化类型为(3)
 的沸点比Z同主族其他元素氢化物高,原因是
的沸点比Z同主族其他元素氢化物高,原因是(4)
 分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是___________ 。C60和金刚石都是碳的同素异形体,二者中熔点较高的是____________ 。
(2)化合物A (H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
3CH4+2(HB=NH)3+ 6H2O→3CO2+6H3BNH3制得。下列有关的叙述不正确的是_______ 。(填标号)
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道的电子排布有关。一般地,若为d 0或d10排布时无颜色;若为d1~d9排布时有颜色;如[Cu(H2O)4]2+显蓝色。据此判断25号元素Mn形成的络合离子[Mn(H2O)6]2+________ (填“有”或“无”)颜色 。
(4)H-C≡C-COOH分子内含有的σ键、π键的个数依次为_________ ,其中碳原子的杂化方式为_____ 。
(5)CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(6)某元素的原子的M能层为全充满状态,且N层电子只有一种运动状态,其单质晶体中微粒的堆积方式是下图中________ (选填“甲”、“乙”或“丙”); 若该晶体中晶胞的边长为acm,则该晶体的密度为_____ g /cm3(写出含a的表达式,用NA表示阿伏伽德罗常数)。

(1)O、Si、N元素的电负性由大到小的顺序是
(2)化合物A (H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
3CH4+2(HB=NH)3+ 6H2O→3CO2+6H3BNH3制得。下列有关的叙述不正确的是
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道的电子排布有关。一般地,若为d 0或d10排布时无颜色;若为d1~d9排布时有颜色;如[Cu(H2O)4]2+显蓝色。据此判断25号元素Mn形成的络合离子[Mn(H2O)6]2+
(4)H-C≡C-COOH分子内含有的σ键、π键的个数依次为
(5)CO可以与金属铁形成配合物分子Fe(CO)5。Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是
(6)某元素的原子的M能层为全充满状态,且N层电子只有一种运动状态,其单质晶体中微粒的堆积方式是下图中

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硼是一种重要的非金属元素,在化学中有很重要的地位。
(1)氨硼烷(NH3BH3)是一种具有潜力的固体储氢材料。NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),三种元素电负性由大到小顺序是_______ 。与NH3BH3原子总数相等的等电子体是_______ (写分子式),其熔点比NH3BH3_______ (填“高”或“低”)。
(2)硼酸是一元弱酸,其呈酸性的机理是∶硼酸与水作用时,硼原子与水电离产生的OH-以配位键结合形成Y-,导致溶液中c(H+)>c(OH-)。Y-的结构简式_______ (配位键用“→”表示)。硼酸与水作用时,每生成一个Y-,断裂_______ 个 键。
键。
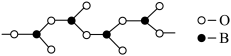
(3)在硼酸盐中,阴离子有链状、环状等多种结构形式。图是一种链状结构的多硼酸根,则多硼酸根离子符号为_______ 。
(1)氨硼烷(NH3BH3)是一种具有潜力的固体储氢材料。NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),三种元素电负性由大到小顺序是
(2)硼酸是一元弱酸,其呈酸性的机理是∶硼酸与水作用时,硼原子与水电离产生的OH-以配位键结合形成Y-,导致溶液中c(H+)>c(OH-)。Y-的结构简式
 键。
键。(3)在硼酸盐中,阴离子有链状、环状等多种结构形式。图是一种链状结构的多硼酸根,则多硼酸根离子符号为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】N元素有多种化合物,它们之间可以发生转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与C第一电离能较大的是________ 。
(2)NaN3的晶体类型是________ 。
(3)N的基态原子的电子排布中,有________ 个运动状态不同的未成对电子。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是____________ 。
(5)HNO2中的N原子的杂化类型是________ 。
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是________ 。
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:______________ 。
(7)N2H4分子中________ (填“含”或“不含”)π键。
(1)N与C第一电离能较大的是
(2)NaN3的晶体类型是
(3)N的基态原子的电子排布中,有
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是
(5)HNO2中的N原子的杂化类型是
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:
(7)N2H4分子中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在国民生产、生活中用途广泛。
(1)向 溶液中加入少量的KSCN溶液,生成红色的
溶液中加入少量的KSCN溶液,生成红色的 。N、C、O元素的第一电离能由大到小的顺序为
。N、C、O元素的第一电离能由大到小的顺序为_______ ,O、N、C、H四种元素电负性最大的是_______ (填元素符号)。
(2) 与
与 溶液混合生成
溶液混合生成 沉淀。配体
沉淀。配体 中C原子的杂化方式为
中C原子的杂化方式为_______ ,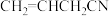 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
(3)用邻二氮菲(phen,结构为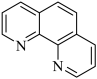 )与琥珀酸亚铁生成稳定的橙色配合物,可测定
)与琥珀酸亚铁生成稳定的橙色配合物,可测定 的浓度,发生反应:
的浓度,发生反应: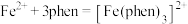 。
。
① 中,存在的化学键有
中,存在的化学键有_______ (填字母)。
a.配位键 b.离子键 c. 键 d.氢键
键 d.氢键
②用邻二氮菲测定 浓度时应控制pH为2~9的适宜范围,请解释原因:
浓度时应控制pH为2~9的适宜范围,请解释原因:_______ 。
(1)向
 溶液中加入少量的KSCN溶液,生成红色的
溶液中加入少量的KSCN溶液,生成红色的 。N、C、O元素的第一电离能由大到小的顺序为
。N、C、O元素的第一电离能由大到小的顺序为(2)
 与
与 溶液混合生成
溶液混合生成 沉淀。配体
沉淀。配体 中C原子的杂化方式为
中C原子的杂化方式为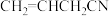 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为(3)用邻二氮菲(phen,结构为
 )与琥珀酸亚铁生成稳定的橙色配合物,可测定
)与琥珀酸亚铁生成稳定的橙色配合物,可测定 的浓度,发生反应:
的浓度,发生反应: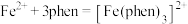 。
。①
 中,存在的化学键有
中,存在的化学键有a.配位键 b.离子键 c.
 键 d.氢键
键 d.氢键②用邻二氮菲测定
 浓度时应控制pH为2~9的适宜范围,请解释原因:
浓度时应控制pH为2~9的适宜范围,请解释原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,[Cu(NH3)4](NO3)2与液氨混合并加入Cu可制得一种黑绿色晶体。
(1)基态Cu核外电子排布式是___________________ 。
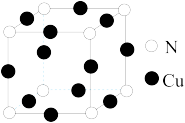
(2)黑绿色晶体的晶胞如图所示,写出该晶体的化学式_________ 。
(3)不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为___________ (用“→”标出其中 的配位键)。
(4) 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是______________ 。 1 mo[Cu(NH3)4](NO3)2中含有的σ键数目为_______ 。
(5)液氨可作制冷剂,汽化时吸收大量热量的原因是______________ 。
(1)基态Cu核外电子排布式是
(2)黑绿色晶体的晶胞如图所示,写出该晶体的化学式

(3)不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为
(4)
 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是(5)液氨可作制冷剂,汽化时吸收大量热量的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氨硼烷( )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为___________ 键,其电子对由___________ 提供。
 )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】比较NH3和[Cu(NH3)4]2+中H-N-H键角的大小:NH3_______ [Cu(NH3)4]2+ (填“>”或“<”),并说明理由:_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)光谱证实单质铝与强碱性溶液反应有[AlOH)4]-生成,则[AlOH)4]-中存在___________ (填序号)。
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(2)Co(NH3)5BrSO4可形成两种钴的配合物。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为___________ ,第二种配合物的结构式可表示为___________ 。若在第二种配合物的溶液中滴加AgNO3溶液,则产生的现象是___________ 。(提示:TiCl(H2O)5Cl2这种配合物的结构可表示为[TiCl(H2O)5]Cl2.)
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是___________(填字母)。
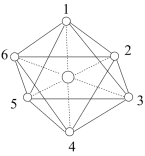
(4)已知CO(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl取代,所形成的[Co(NH3)4Cl2]+的结构的数目为___________ 。
(5)向盛有硫酸铜水溶液的试管中加氨水。先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解,用离子方程式解释原因:___________ 、___________ 。
(1)光谱证实单质铝与强碱性溶液反应有[AlOH)4]-生成,则[AlOH)4]-中存在
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(2)Co(NH3)5BrSO4可形成两种钴的配合物。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是___________(填字母)。
| A.1mol[Ti(NH3)5Cl]Cl2含有σ键的数目为15NA |
| B.中心原子的化合价为+3价 |
| C.中心原子的配位数是6 |
| D.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀 |

(5)向盛有硫酸铜水溶液的试管中加氨水。先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解,用离子方程式解释原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
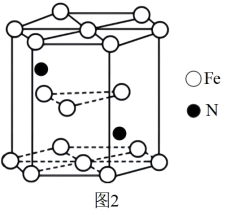
【推荐1】第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。铁和氮组成一种过渡金属氮化物,其结构如图2所示。直六棱柱的底边边长为xcm,高为ycm,阿伏加德罗常数的值为NA,则晶体的密度算式为_______ g·cm-3。

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某离子晶体晶胞的结构如图所示,X(●)位于立方体顶点,Y(○)位于立方体中心。试分析:
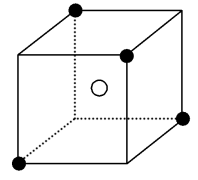
(1)晶体中距离最近的2个X与1个Y形成的夹角∠XYX是___________ 。
(2)设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为___________ cm。

(1)晶体中距离最近的2个X与1个Y形成的夹角∠XYX是
(2)设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮元素及其化合物在生产、生活中用途广泛。回答下列问题:
(1)基态氮原子的价电子排布式为___________ 。
(2)与N同周期的元素中第一电离能比N大的元素有____________ 种。
(3)三硝基胺N(NO2)3(其结构为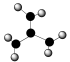 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为___________ ,并且与三个硝基中的N构成___________ 形。
(4)(CN)2、(SCN)2的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则1mol(CN)2分子中含___________ molπ键,SCN-的空间构型为___________ 形。
(5)白磷在氯气中燃烧可以得到PCl3和PCl5,研究发现固态PCl4和PBr5均为离子晶体,但其结构分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的原因:___________ 。
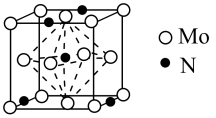
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼(Mo)的氮化物可作将N2还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数为anm,则该晶体的化学式为___________ ,晶体的密度为___________ (列出计算式)g·cm-3。
(1)基态氮原子的价电子排布式为
(2)与N同周期的元素中第一电离能比N大的元素有
(3)三硝基胺N(NO2)3(其结构为
 )是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为
)是一种新型的火箭燃料,因硝基吸电子能力强,中心N原子上无孤电子对,则中心N原子的杂化方式为(4)(CN)2、(SCN)2的性质与卤素单质的相似,称为拟卤素。其分子内各原子均达到8电子稳定结构,则1mol(CN)2分子中含
(5)白磷在氯气中燃烧可以得到PCl3和PCl5,研究发现固态PCl4和PBr5均为离子晶体,但其结构分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的原因:
(6)过渡金属氮化物因其优异的催化性能(加氢处理、光和电化学催化等)受到了广泛关注。贵金属钼(Mo)的氮化物可作将N2还原为氨的反应的催化剂。贵金属钼的氮化物的立方晶胞如图所示。已知晶胞参数为anm,则该晶体的化学式为

您最近一年使用:0次



