室温下,[Cu(NH3)4](NO3)2与液氨混合并加入Cu可制得一种黑绿色晶体。
(1)基态Cu核外电子排布式是___________________ 。
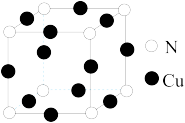
(2)黑绿色晶体的晶胞如图所示,写出该晶体的化学式_________ 。
(3)不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为___________ (用“→”标出其中 的配位键)。
(4) 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是______________ 。 1 mo[Cu(NH3)4](NO3)2中含有的σ键数目为_______ 。
(5)液氨可作制冷剂,汽化时吸收大量热量的原因是______________ 。
(1)基态Cu核外电子排布式是
(2)黑绿色晶体的晶胞如图所示,写出该晶体的化学式

(3)不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为
(4)
 中N原子轨道的杂化类型是
中N原子轨道的杂化类型是(5)液氨可作制冷剂,汽化时吸收大量热量的原因是
2020·江苏泰州·模拟预测 查看更多[3]
更新时间:2020-09-15 12:05:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为___________ 个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为_______________ 。
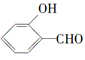 的沸点比
的沸点比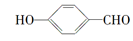 高,原因是
高,原因是______________________ 。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为________________ 。
(4)CaF2离子晶体的晶胞结构如图所示。该离子化合物晶胞的边长为a cm,则晶体的密度是_____________ g/cm3(只要求列出算式)。

(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)H+可与H2O形成H3O+,H3O+中O原子采用
(4)CaF2离子晶体的晶胞结构如图所示。该离子化合物晶胞的边长为a cm,则晶体的密度是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题。
(1)Cu+基态核外电子排布式为___________ 。
(2)基态Fe原子有___________ 个未成对电子,Fe+的电子排布式为___________ 。
(3)S的基态原子核外有___________ 个未成对电子;Si的基态原子核外电子排布式为___________ 。
(4)Cu的价层电子轨道示意图为___________ 。
(5)基态Si原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ 。
(1)Cu+基态核外电子排布式为
(2)基态Fe原子有
(3)S的基态原子核外有
(4)Cu的价层电子轨道示意图为
(5)基态Si原子中,电子占据的最高能层符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据要求回答下列问题:
(1)工业上利用镍与CO形成化合物Ni(CO)4分离提纯镍。C原子能量最高的电子为_______ 轨道上的电子,该轨道呈_______ 形。CO的结构式为_______ ,WgCO中含 键数目为
键数目为_______ 。
(2)硅是重要的半导体材料,构成了现代电子工业的基础。基态Si原子中,电子占据的最高能层的符号为_______ ,核外电子的运动状态有_______ 种,有_______ 种能量不同的电子。
(3)有关碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是_______ 。
(4)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体形分子_______ ,三角锥形分子_______ ,V形分子_______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从原子核外电子结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。
(1)工业上利用镍与CO形成化合物Ni(CO)4分离提纯镍。C原子能量最高的电子为
 键数目为
键数目为(2)硅是重要的半导体材料,构成了现代电子工业的基础。基态Si原子中,电子占据的最高能层的符号为
(3)有关碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
(4)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体形分子
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从原子核外电子结构角度来看,Fe2+易被氧化成Fe3+的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】过渡元素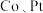 等在生活、科研中有广泛用途和重要研究价值。回答下列问题:
等在生活、科研中有广泛用途和重要研究价值。回答下列问题:
(1) 分子作为配体时,碳原子和氧原子均能够提供孤电子对。
分子作为配体时,碳原子和氧原子均能够提供孤电子对。 与钴形成配位化合物时,提供孤电子对的为
与钴形成配位化合物时,提供孤电子对的为_______ (填元素名称)原子。
(2)高氯酸六氨合钴(Ⅱ)的结构为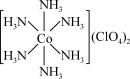 ,其外界离子的空间构型为
,其外界离子的空间构型为_______ 。
(3)下列对 的中心原子采取的杂化类型判断合理的是_______(填标号)。
的中心原子采取的杂化类型判断合理的是_______(填标号)。
 等在生活、科研中有广泛用途和重要研究价值。回答下列问题:
等在生活、科研中有广泛用途和重要研究价值。回答下列问题:(1)
 分子作为配体时,碳原子和氧原子均能够提供孤电子对。
分子作为配体时,碳原子和氧原子均能够提供孤电子对。 与钴形成配位化合物时,提供孤电子对的为
与钴形成配位化合物时,提供孤电子对的为(2)高氯酸六氨合钴(Ⅱ)的结构为
 ,其外界离子的空间构型为
,其外界离子的空间构型为(3)下列对
 的中心原子采取的杂化类型判断合理的是_______(填标号)。
的中心原子采取的杂化类型判断合理的是_______(填标号)。A. | B. | C. | D. |
您最近一年使用:0次
【推荐2】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为_________ ;H、N、O三种元素的电负性由大到小的顺序是_____________
(2)SO2分子的空间构型为_____________
(3)乙二胺分子中氮原子轨道的杂化类型为_________ 乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_____________
(4)②中所形成的配离子中含有的化学键类型有______ (填字母)。
A.配位键 B.极性键 C.离子键 D.非极性键
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O
 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有
A.配位键 B.极性键 C.离子键 D.非极性键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】据报道,四川大学某研究所采用近空间升华技术研究碲化镉薄膜太阳能电池,取得了很好的成绩,电池转化效率已经突破13.38%,进入了世界先进行列。回答下列问题:
(1)基态碲原子中,价层电子的排布式为______ ;其核外电子占据的最高能级的电子云轮廓图形状为______ .
(2)镉的原子序数为48,它处在元素周期表的______ 区(填s、p、d、ds或f)。
(3)碲和镉中,电负性较大的是______ ;碲酸根离子的空间构型是______ ,其中碲原子的杂化方式为________ .
(4)研制碲化镉太阳能电池的主要工艺流程为:衬底清洗 前电极制备
前电极制备 硫化镉沉积
硫化镉沉积 碲化镉沉积
碲化镉沉积 氯化镉后处理
氯化镉后处理 背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是
背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是_______ 。
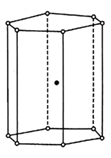
(5)氯化镉晶体的结构如右图所示,图中“。”代表氯原子,“·”代表镉原子,六边形边长为apm,六棱柱高为bpm,则氯化镉晶体的化学式为______ ,晶体密度为______ g/cm3(NA表示阿伏伽德罗常数的值,列出计算式即可)
(1)基态碲原子中,价层电子的排布式为
(2)镉的原子序数为48,它处在元素周期表的
(3)碲和镉中,电负性较大的是
(4)研制碲化镉太阳能电池的主要工艺流程为:衬底清洗
 前电极制备
前电极制备 硫化镉沉积
硫化镉沉积 碲化镉沉积
碲化镉沉积 氯化镉后处理
氯化镉后处理 背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是
背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是(5)氯化镉晶体的结构如右图所示,图中“。”代表氯原子,“·”代表镉原子,六边形边长为apm,六棱柱高为bpm,则氯化镉晶体的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】金属钛被誉为“二十一世纪金属”,有“生物金属、海洋金属、太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)磷酸钛铝锂可用作锂离子电池的正极材料, 的空间结构是
的空间结构是_______ 。
(2) 可以与胺形成配合物,如
可以与胺形成配合物,如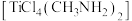 、
、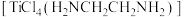 等。
等。
①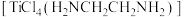 中
中 的配位数是
的配位数是_______ 。
②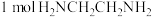 中含有的
中含有的 键的物质的量为
键的物质的量为_______ 。
③配合物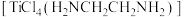 与游离的
与游离的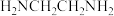 分子相比,其
分子相比,其 键角
键角_______ (填“较大”“较小”或“相同”),原因是_______ 。
(1)磷酸钛铝锂可用作锂离子电池的正极材料,
 的空间结构是
的空间结构是(2)
 可以与胺形成配合物,如
可以与胺形成配合物,如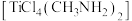 、
、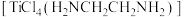 等。
等。①
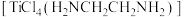 中
中 的配位数是
的配位数是②
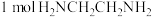 中含有的
中含有的 键的物质的量为
键的物质的量为③配合物
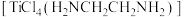 与游离的
与游离的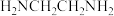 分子相比,其
分子相比,其 键角
键角
您最近一年使用:0次
填空题
|
适中
(0.65)
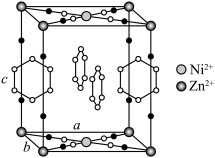
【推荐2】化学式为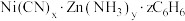 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞中N原子均参与形成配位键,
的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞中N原子均参与形成配位键, 与
与 的配位数之比为
的配位数之比为_______ ;
_______ ;晶胞中有d轨道参与杂化的金属离子是_______ 。
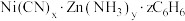 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞中N原子均参与形成配位键,
的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞中N原子均参与形成配位键, 与
与 的配位数之比为
的配位数之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
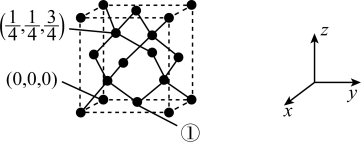
【推荐1】晶体硅的晶胞如下,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。则图中原子①的原子坐标是_______ ,晶体中硅原子的空间利用率为_______ (用含π的式子表示)。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
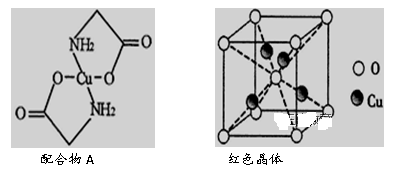
【推荐2】已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图所示:
(1)Cu元素基态原子的外围电子排布式为______________ 。
(2)元素C、N、O的第一电离能由大到小排列顺序为_______________ 。
(3)配合物A中碳原子的轨道杂化类型为_______________________ 。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有 键的数目为
键的数目为____________ mol。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:____________ (写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是_________ 。

(1)Cu元素基态原子的外围电子排布式为
(2)元素C、N、O的第一电离能由大到小排列顺序为
(3)配合物A中碳原子的轨道杂化类型为
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有
 键的数目为
键的数目为(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】石油开采和炼制过程中产生的污水含有溶解性的 以及难溶的硫化物,对污水进行处理的同时可回收化工原料。已知:
以及难溶的硫化物,对污水进行处理的同时可回收化工原料。已知: 在水中溶解度为1∶2.6,易挥发。回答下列问题:
在水中溶解度为1∶2.6,易挥发。回答下列问题:
(1)沉淀法处理含硫废水:
向含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。解释溶液的pH降低的原因:___________ 。
(2)氧化还原法处理含硫废水:
①空气氧化法可将含硫微粒氧化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
②向废水中加入一定浓度的 溶液,加酸将溶液调为
溶液,加酸将溶液调为 ,产生淡黄色沉淀。反应的离子方程式为
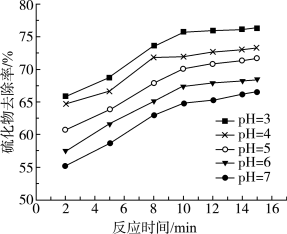
,产生淡黄色沉淀。反应的离子方程式为___________ 。不同pH时,硫化物去除率随时间的变化曲线如下图。选择控制体系的 ,不选择
,不选择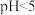 ,从环境保护的角度来分析其主要原因:
,从环境保护的角度来分析其主要原因:___________ 。
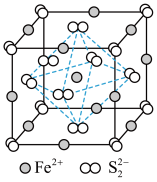
(3) 晶体的晶胞如图所示。晶胞边长为anm,设阿伏加德罗常数的值为
晶体的晶胞如图所示。晶胞边长为anm,设阿伏加德罗常数的值为 。
。 的配位数为
的配位数为___________ ,其晶体密度为___________  ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为___________ nm。
 以及难溶的硫化物,对污水进行处理的同时可回收化工原料。已知:
以及难溶的硫化物,对污水进行处理的同时可回收化工原料。已知: 在水中溶解度为1∶2.6,易挥发。回答下列问题:
在水中溶解度为1∶2.6,易挥发。回答下列问题:(1)沉淀法处理含硫废水:
向含硫废水中加入适量
 的溶液,产生黑色沉淀且溶液的pH降低。解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。解释溶液的pH降低的原因:(2)氧化还原法处理含硫废水:
①空气氧化法可将含硫微粒氧化为
 ,反应的离子方程式为
,反应的离子方程式为②向废水中加入一定浓度的
 溶液,加酸将溶液调为
溶液,加酸将溶液调为 ,产生淡黄色沉淀。反应的离子方程式为
,产生淡黄色沉淀。反应的离子方程式为 ,不选择
,不选择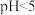 ,从环境保护的角度来分析其主要原因:
,从环境保护的角度来分析其主要原因:
(3)
 晶体的晶胞如图所示。晶胞边长为anm,设阿伏加德罗常数的值为
晶体的晶胞如图所示。晶胞边长为anm,设阿伏加德罗常数的值为 。
。 的配位数为
的配位数为 ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次

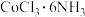 (黄色)、
(黄色)、 (紫红色)、
(紫红色)、 (绿色)和
(绿色)和 分别溶于水,加入足量硝酸银溶液,生成氯化银沉淀的物质的量分别为
分别溶于水,加入足量硝酸银溶液,生成氯化银沉淀的物质的量分别为 、
、 、
、

