下列事实中,不能用勒夏特列原理解释的是( )
A.溴水中存在如下平衡:Br2+H2O HBr+HBrO,当加入NaOH溶液后颜色变浅 HBr+HBrO,当加入NaOH溶液后颜色变浅 |
B.合成氨反应:N2+3H2 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 |
C.反应:CO+NO2 CO2+NO ΔH<0,升高温度,平衡向逆反应方向移动 CO2+NO ΔH<0,升高温度,平衡向逆反应方向移动 |
D.对2H2O2 2H2O+O2↑的反应,使用MnO2可加快制O2的反应速率 2H2O+O2↑的反应,使用MnO2可加快制O2的反应速率 |
更新时间:2020-04-29 18:27:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】研究发现 时,
时, 表面易脱除O原子形成
表面易脱除O原子形成 (氧空穴)。氧空穴越多,催化效果越好,
(氧空穴)。氧空穴越多,催化效果越好, 催化
催化 和
和 合成甲醇的机理如图。下列说法错误的是
合成甲醇的机理如图。下列说法错误的是
 时,
时, 表面易脱除O原子形成
表面易脱除O原子形成 (氧空穴)。氧空穴越多,催化效果越好,
(氧空穴)。氧空穴越多,催化效果越好, 催化
催化 和
和 合成甲醇的机理如图。下列说法错误的是
合成甲醇的机理如图。下列说法错误的是
| A.温度较低时.催化剂的活性降低 |
B.增加 的用量, 的用量, 的平衡转化率不变 的平衡转化率不变 |
C.增大气体流速带走多余的 ,可提高催化效率 ,可提高催化效率 |
D.若 和 和 的混合气中混有 的混合气中混有 的催化效果增强 的催化效果增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实不能用勒夏特列原理来解释的是
| A.用排饱和食盐水的方法收集氯气 |
| B.加入催化剂使N2和H2在一定条件下生成氨气 |
| C.增大压强,有利于SO2和O2反应生成SO3 |
D.在Fe3+ + 3SCN-  Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用 注射器吸入
注射器吸入 由
由 和
和 组成的混合气体[存在平衡:
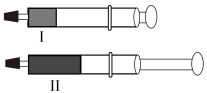
组成的混合气体[存在平衡: 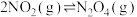 ],此时注射器活塞位于I处,将细口端封闭,然后将注射器活塞拉至II处,如图,下列对产生的现象或原理的描述正确的是
],此时注射器活塞位于I处,将细口端封闭,然后将注射器活塞拉至II处,如图,下列对产生的现象或原理的描述正确的是
 注射器吸入
注射器吸入 由
由 和
和 组成的混合气体[存在平衡:
组成的混合气体[存在平衡: 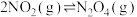 ],此时注射器活塞位于I处,将细口端封闭,然后将注射器活塞拉至II处,如图,下列对产生的现象或原理的描述正确的是
],此时注射器活塞位于I处,将细口端封闭,然后将注射器活塞拉至II处,如图,下列对产生的现象或原理的描述正确的是
| A.把活塞从I处拉到II处,过程中注射器中颜色一直变深,然后保持不变 |
| B.若再把活塞从II处推回I处,则过程中注射器中颜色先变深后变浅 |
C.若将活塞固定在I处,升高温度,注射器中颜色变深,则说明 |
D.当体系处于稳定状态时,混合气体中 的百分含量:I 的百分含量:I II II |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组用新型催化剂对CO、NO催化转化进行研究,测得相同时间内NO的转化率、CO剩余的百分含量随温度变化情况如图所示。已知NO可发生下列反应:
反应Ⅰ: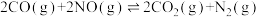

反应Ⅱ: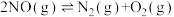

反应Ⅰ:
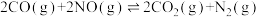

反应Ⅱ:
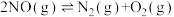

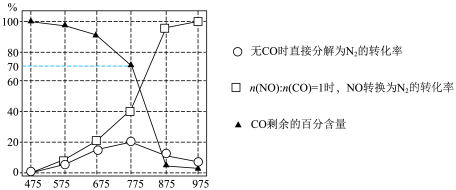
A. |
| B.温度大于775K时,催化剂活性降低 |
C.775K, 条件下,此时 条件下,此时 |
D.775K,无CO参加,只发生反应Ⅱ时的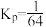 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】恒温密闭容器中,发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H<0。若按照n(CO2):n(H2)=1:3的投料比充入容器,测得平衡时n(H2)和n(H2O)随温度的变化如图所示。下列说法正确的是
C2H4(g)+4H2O(g) △H<0。若按照n(CO2):n(H2)=1:3的投料比充入容器,测得平衡时n(H2)和n(H2O)随温度的变化如图所示。下列说法正确的是
 C2H4(g)+4H2O(g) △H<0。若按照n(CO2):n(H2)=1:3的投料比充入容器,测得平衡时n(H2)和n(H2O)随温度的变化如图所示。下列说法正确的是
C2H4(g)+4H2O(g) △H<0。若按照n(CO2):n(H2)=1:3的投料比充入容器,测得平衡时n(H2)和n(H2O)随温度的变化如图所示。下列说法正确的是
| A.L线表示平衡时n(H2O)随温度的变化 |
| B.由图可知、温度升高,正反应速率减小,逆反应速率增大 |
| C.x=5.16mol |
| D.在等温相同体积下,通入1molCO2、3molH2与通入2molCO2、6molH2达到平衡时,C2H4的体积分数一样 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于化学反应速率和化学平衡的说法正确的是。
| A.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子百分数,从而使反应速率增大 |
B.已知反应: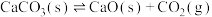 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 的浓度将升高 的浓度将升高 |
C.在一定条件下,可逆反应2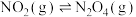 达到平衡后。保持恒温恒容,再通入一定量 达到平衡后。保持恒温恒容,再通入一定量 ,平衡逆向移动,且达到新平衡时 ,平衡逆向移动,且达到新平衡时 的百分含量减小 的百分含量减小 |
D.在一定温度下,容积一定的密闭容器中的反应 ,当混合气体的压强不变时,则表明该反应已达平衡 ,当混合气体的压强不变时,则表明该反应已达平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g)  C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L。下列分析不正确的是
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L。下列分析不正确的是

 C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L。下列分析不正确的是
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H2O)=n(C2H4)=1mol,容器体积为1L。下列分析不正确的是
| A.该反应是放热反应 |
| B.图中压强的大小关系为p1<p2<p3 |
| C.达到平衡状态a、b所需要的时间:b>a |
| D.a、b点对应气体的平均摩尔质量:a=b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、现象、结论均正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向平衡体系FeCl3+3KSCN Fe(SCN)3+3KCl中加入适量KCl固体 Fe(SCN)3+3KCl中加入适量KCl固体 | 溶液的颜色变浅 | 平衡逆向移动 |
| B | 对平衡体系2NO2(g) N2O4(g)压缩体积,增大压强 N2O4(g)压缩体积,增大压强 | 混合气体的颜色变深 | 平衡逆向移动 |
| C | 2mL0.1mol•L-1K2Cr2O7溶液中存在:Cr2O (橙色)+H2O (橙色)+H2O 2CrO 2CrO (黄色)+2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 (黄色)+2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 | 溶液变为橙色 | 平衡逆向移动 |
| D | 分别取5mL0.5mol·L-1H2SO4溶液和5mL0.1mol·L-1H2SO4溶液于两支试管中,然后同时加入5mL0.1mol·L-1Na2S2O3溶液 | 两支试管中的溶液都变浑浊,前者先变浑浊 | 增大H2SO4浓度,可以加快反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列不能用平衡移动原理解释的事实是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.氢气、碘蒸汽、碘化氢气组成的平衡体系加压后颜色变深 |
| C.淡黄绿色的氯水光照后颜色变浅 |
| D.合成氨工业反应过程中适时分离反应产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
A.用排饱和食盐水的方法收集 |
B.硫酸工业中增大氧气的浓度有利于提高 的转化率 的转化率 |
| C.工业合成氨,反应条件选择高温高压 |
| D.实验室将浓氨水滴入到氢氧化钠固体中快速制氨气 |
您最近一年使用:0次



