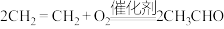某温度下,可逆反应mA(g) + nB(g) ⇌pC(g) ΔH < 0 的化学平衡常数为K,下列说法正确的是
| A.其他条件不变,升高温度,K值增大 |
| B.其他条件不变,恒容条件下,通入稀有气体,正、逆反应速率均增大 |
| C.其他条件不变,减小C(g)的浓度,正反应速率增大,逆反应速率减小 |
| D.其他条件不变,增大压强,活化分子百分数不变,有效碰撞几率增加 |
更新时间:2020-05-19 13:00:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 可活化
可活化 放出
放出 ,其反应历程如下图所示:下列关于活化历程的说法正确的是
,其反应历程如下图所示:下列关于活化历程的说法正确的是

 可活化
可活化 放出
放出 ,其反应历程如下图所示:下列关于活化历程的说法正确的是
,其反应历程如下图所示:下列关于活化历程的说法正确的是
| A.此反应的决速步骤:中间体1→中间体2 |
| B.涉及极性键的形成和非极性键的断裂 |
| C.三种中间体比较,中间体3最稳定 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关影响化学反应速率的因素的说法不正确 的是
| A.能发生有效碰撞的分子,一定是活化分子 |
| B.减小容器体积使压强增大,活化分子百分数不变,单位体积内活化分子数增多 |
| C.升高温度可以增大活化分子百分数,从而增大单位时间内有效碰撞的次数 |
| D.增大反应物浓度,反应物中的活化分子百分数增大,单位体积内活化分子数增多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 两支试管各盛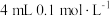 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入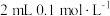 草酸溶液和 草酸溶液和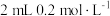 草酸溶液 草酸溶液 | 加入 草酸溶液的试管中溶液紫色消失更快 草酸溶液的试管中溶液紫色消失更快 | 其他条件相同,反应物浓度越大,反应速率越快 |
| B | 向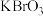 溶液中通入少量氯气,然后再加入少量苯,振荡,静置 溶液中通入少量氯气,然后再加入少量苯,振荡,静置 | 溶液分层,上层呈橙红色 | 氧化性: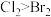 |
| C | 向含相同浓度的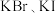 混合溶液中依次加入少量氯水和 混合溶液中依次加入少量氯水和 ,振荡,静置 ,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性: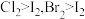 |
| D | 向葡萄糖溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液紫色消失 | 葡萄糖中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示。在下列因素中,若要解释该图象的变化趋势,涉及到的主要因素是
①盐酸的浓度②镁条的表面积③溶液的温度④Cl-的浓度

①盐酸的浓度②镁条的表面积③溶液的温度④Cl-的浓度

| A.①④ | B.①③ | C.①②③ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,在恒压绝热容器中发生反应:N2(g)+3H2(g) 2NH3(g) ∆H=-92.4kJ·mol-1.下列说法正确的是
2NH3(g) ∆H=-92.4kJ·mol-1.下列说法正确的是
 2NH3(g) ∆H=-92.4kJ·mol-1.下列说法正确的是
2NH3(g) ∆H=-92.4kJ·mol-1.下列说法正确的是| A.达到化学平衡状态时,v正(N2)=3v逆(H2) |
| B.容器内的压强不再变化说明反应达到化学平衡状态 |
| C.向容器中充入He气体,正反应速率减小,逆反应速率减小 |
| D.加入1molN2和3molH2,充分反应后放出热量92.4kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】采取下列措施对增大化学反应速率有明显效果的是
| A.Na与水反应时,增加水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.氯化铵固体与熟石灰共热制氨气时,增大压强 |
D.大理石与盐酸反应制取 时,将块状大理石改为粉末状大理石 时,将块状大理石改为粉末状大理石 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g)  2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )| A.提高尾气净化速率的常用方法是降低温度 |
| B.提高尾气净化速率的最佳途径是研制高效催化剂 |
| C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】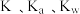 分别表示化学平衡常数、电离常数和水的离子积常数,下列说法正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列说法正确的是
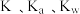 分别表示化学平衡常数、电离常数和水的离子积常数,下列说法正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列说法正确的是| A.某可逆反应达到平衡后,改变某一条件使平衡正向移动,K可能不变 |
| B.氨的催化氧化反应,使用催化剂后K增大 |
C.室温下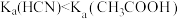 ,说明 ,说明 是强酸 是强酸 |
D.25℃时, 均为4的盐酸和 均为4的盐酸和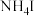 溶液中 溶液中 不相等 不相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】生命过程与化学平衡移动密切相关。血红蛋白(Hb)与O2结合形成氧合血红蛋白分子[Hb(O2)]的过程可表示为Hb+O2 Hb(O2)。下列说法正确的是
Hb(O2)。下列说法正确的是
 Hb(O2)。下列说法正确的是
Hb(O2)。下列说法正确的是| A.吸入新鲜空气,平衡逆向移动 |
| B.体温升高,O2与Hb结合更快,该反应的平衡常数不变 |
C.利用高压氧舱治疗CO中毒的原理是使平衡Hb(CO)+O2 Hb(O2)+CO右移 Hb(O2)+CO右移 |
| D.CO达到一定浓度可使人中毒,是因为CO结合Hb,使Hb(O2)分解速率增大 |
您最近一年使用:0次

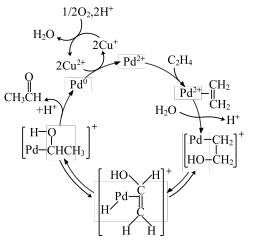
 和
和 能够降低反应的活化能
能够降低反应的活化能