苯甲醇是一种重要的化工原料,广泛用于香料、造纸、制药和印染等行业。实验室制备苯甲醇的反应原理和有关数据如图:
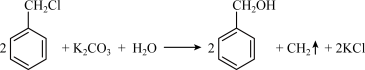
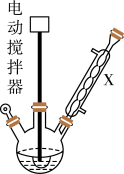
实验步骤:如图所示,在装有电动搅拌器的250mL三颈烧瓶里加入9.0g碳酸钾(过量),70.0mL水,加热溶解,再加入2.0mL四乙基溴化铵[(CH3CH2)4NBr]溶液和10.0mL氯化苄。搅拌加热回流反应1~1.5h。反应结束后冷却,并转入125mL分液漏斗中,分出有机层,水层用萃取剂萃取三次。合并萃取液和有机层,加入无水硫酸镁固体,静置、过滤。最后进行蒸馏纯化,收集200~208℃的馏分,得8.4mL苯甲醇。
回答下列问题:
(1)仪器X的名称是___ ,冷却水应从___ (填“上口”或“下口”)通入。由于苯甲醇的沸点较高,在蒸馏纯化操作中最适宜选用的仪器之一是___ (填字母)。

(2)本实验中加入无水硫酸镁的目的是___ 。从绿色化学角度考虑,萃取剂宜采用___ (填字母)。
A.乙醇 B.乙酸乙酯 C.苯 D.氯仿
(3)某同学认为该装置中的电动搅拌器可以换成沸石,以防暴沸。该说法___ (填“是”或“否”)正确,其理由是___ 。
(4)四乙基溴化铵没有直接参与反应,但大大提高了反应速率,其原因可能是___ 。
(5)本实验苯甲醇的产率为___ %(计算结果保留一位小数)。
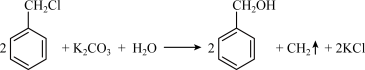
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 水溶性 | |
氯化苄 | 126.5 | -43 | 179.4 | 1.1 | 不溶 |
碳酸钾 | 138 | 891 | — | 2.4 | 易溶 |
四乙基溴化铵 | — | — | — | — | 易溶 |
苯甲醇 | 108 | -15.3 | 205.3 | 1.0 | 易溶 |

回答下列问题:
(1)仪器X的名称是

(2)本实验中加入无水硫酸镁的目的是
A.乙醇 B.乙酸乙酯 C.苯 D.氯仿
(3)某同学认为该装置中的电动搅拌器可以换成沸石,以防暴沸。该说法
(4)四乙基溴化铵没有直接参与反应,但大大提高了反应速率,其原因可能是
(5)本实验苯甲醇的产率为
更新时间:2020-05-27 11:24:38
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】二氯化砜(SO2Cl2)是一种无色液体,主要用于有机物和无机物的氯化等。其熔点为−54.1 ℃,沸点为69.2 ℃;常温下比较稳定,受热易分解,遇水剧烈反应生成硫酸和盐酸。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g) SO2Cl2(g) △H<0。
SO2Cl2(g) △H<0。
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为__________________________ ;溶液A为___________ 。
②上图实框中仪器己的名称为___________ ;反应装置图的虚框中未画出的仪器是___________ (填“己”或“庚”)。
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是______________________ 。
④下列有关说法错误的是___________ (填编号)。
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是______________________ 。
(3)测定。取1.00 g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60 g,则所得蒸馏成分中二氯化砜的质量百分含量为___________ %(精确到0.01)。
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是___________ 。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g)
 SO2Cl2(g) △H<0。
SO2Cl2(g) △H<0。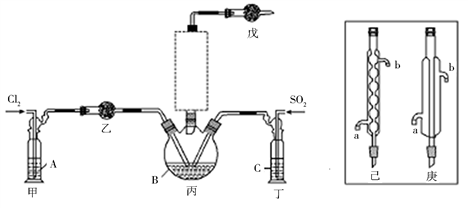
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为
②上图实框中仪器己的名称为
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是
④下列有关说法错误的是
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是
(3)测定。取1.00 g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60 g,则所得蒸馏成分中二氯化砜的质量百分含量为
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】草酸(H2C2O4)是一种重要的有机化工原料。为探究草酸的制取和草酸的性质,进行如下实验。
实验Ⅰ:探究草酸的制备
实验室用硝酸氧化淀粉水解液法制备草酸,装置如下图所示:
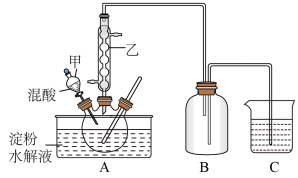
硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3 → 3H2C2O4+9NO2↑+3NO↑+9H2O。
(1)上图实验装置中仪器乙的名称为:____ ,B装置的作用______
(2)检验淀粉是否完全水解所需要的试剂为:______ 。
实验Ⅱ:探究草酸的不稳定性
已知:草酸晶体(H2C2O4·2H2O)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2。草酸的酸性比碳酸强,其钙盐难溶于水。
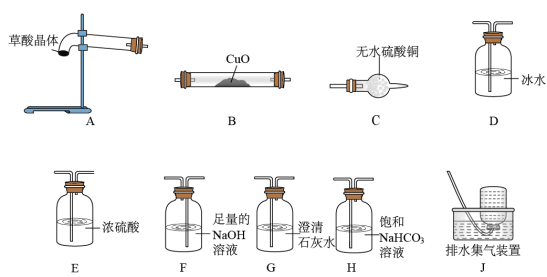
(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:A→___ →____ →____ →___ →E→B→G→____ 。
(4)若实验结束后测得B管质量减轻4.8g,则至少需分解草酸晶体的质量为_____ g(已知草酸晶体的M=126g/mol)。
实验Ⅲ:探究草酸与酸性高锰酸钾的反应
取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
(5)该实验中草酸表现______ 性,离子方程式_______ 该反应的反应速率先慢后快的主要原因可能是_________ 。
(6)设计实验证明草酸是弱酸。实验方案:______________ (提供的药品及仪器:蒸馏水、0.1mol·L-1NaOH溶液、pH计、0.1mol·L-1草酸溶液,其它仪器自选)
实验Ⅰ:探究草酸的制备
实验室用硝酸氧化淀粉水解液法制备草酸,装置如下图所示:

硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3 → 3H2C2O4+9NO2↑+3NO↑+9H2O。
(1)上图实验装置中仪器乙的名称为:
(2)检验淀粉是否完全水解所需要的试剂为:
实验Ⅱ:探究草酸的不稳定性
已知:草酸晶体(H2C2O4·2H2O)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2。草酸的酸性比碳酸强,其钙盐难溶于水。

(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:A→
(4)若实验结束后测得B管质量减轻4.8g,则至少需分解草酸晶体的质量为
实验Ⅲ:探究草酸与酸性高锰酸钾的反应
取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
(5)该实验中草酸表现
(6)设计实验证明草酸是弱酸。实验方案:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】邻苯二甲酸二丁酯(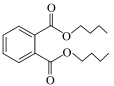 )为无色液体,通过邻苯二甲酸酐(
)为无色液体,通过邻苯二甲酸酐(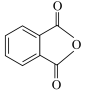 )和正丁醇合成,可作增塑剂,制备邻苯二甲酸二丁酯的反应如下(其中第一步反应会完全进行):
)和正丁醇合成,可作增塑剂,制备邻苯二甲酸二丁酯的反应如下(其中第一步反应会完全进行):
第二步: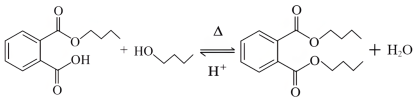 。
。
| 物质 | 相对分子质量 | 沸点/℃ | 溶解性 | 其他性质 |
| 正丁醇 | 74 | 117.6 | 易溶于有机溶剂,在水中溶解度不大 | 密度小于水 |
| 邻苯二甲酸单丁酯 | 222 | 363.5 | 易溶于有机溶剂,难溶于水 | |
| 邻苯二甲酸二丁酯 | 278 | 337 | 易溶于有机溶剂,不溶于水 | 着火点202℃ |
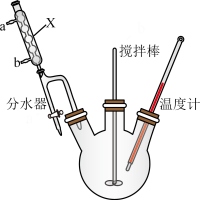
①向三颈烧瓶内加入5.9g(0.04mol)邻苯二甲酸酐,12.5mL(0.12mol)正丁醇,几粒沸石和0.2mL浓硫酸;另在分水器中加入正丁醇至与分水器支管口齐平,后加热三颈烧瓶至微沸。
②待三颈烧瓶内邻苯二甲酸酐完全溶解后,继续升温并搅拌反应2小时,保温至反应结束。
③冷却至室温,将反应混合物倒出,依次用5%Na2CO3溶液、饱和食盐水洗涤得粗产品。
④粗产品用无水硫酸镁处理,取处理后的液体至圆底烧瓶,减压蒸馏,最终得到产品8.34g。
回答下列问题:
(1)仪器X的名称为
(2)分水器使用前需要进行的操作为
(3)制备的第一步是制备邻苯二甲酸单丁酯,涉及反应的化学方程式为
(4)实验中用饱和食盐水洗涤的原因是
(5)本实验中,邻苯二甲酸二丁酯的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】外观与氯化钠相似的亚硝酸钠( )在生活中应用广泛。
)在生活中应用广泛。
已知: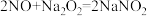 ,
,
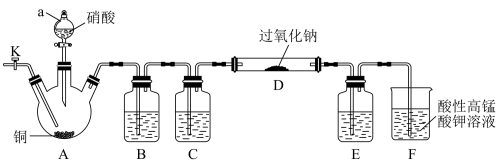
I.某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)
(1)仪器a的名称为________ 。
(2)装量B、C、E中的试制可选择________ 。
A.水、浓硫酸、浓硫酸
B.酸性高锰酸钾溶液、浓硫酸、氢氧化钠溶液
C.水、浓硫酸、氢氧化钠溶液
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是__________ 。
(4)装置D中的实验现象是____________ 。
(5)装置F中发生反应的离子方程式为______________ 。
Ⅱ.工业上可以用烧碱溶液吸收硝酸厂的尾气制得亚硝酸钠。某学习小组设计如下实验方案测定该产品中亚硝酸钠的质量分数。
取1.500 g产品配成250 mL溶液,取25.00 mL溶液于锥形瓶中加入过量的稀硫酸和碘化钾溶液充分反应后,加入适当的指示剂,用 标准溶液进行滴定,记录数据如下表。
标准溶液进行滴定,记录数据如下表。
已知:
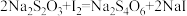
(6)合适的指示剂是________ 。
(7)该产品的纯度为________ 。
(8)经过讨论,同学认为该产品中可能含有硝酸钠,它会使测定结果______ (填“偏高”、“偏低”、“无影响”) 。
 )在生活中应用广泛。
)在生活中应用广泛。已知:
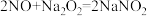 ,
,

I.某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)
(1)仪器a的名称为
(2)装量B、C、E中的试制可选择
A.水、浓硫酸、浓硫酸
B.酸性高锰酸钾溶液、浓硫酸、氢氧化钠溶液
C.水、浓硫酸、氢氧化钠溶液
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是
(4)装置D中的实验现象是
(5)装置F中发生反应的离子方程式为
Ⅱ.工业上可以用烧碱溶液吸收硝酸厂的尾气制得亚硝酸钠。某学习小组设计如下实验方案测定该产品中亚硝酸钠的质量分数。
取1.500 g产品配成250 mL溶液,取25.00 mL溶液于锥形瓶中加入过量的稀硫酸和碘化钾溶液充分反应后,加入适当的指示剂,用
 标准溶液进行滴定,记录数据如下表。
标准溶液进行滴定,记录数据如下表。实验序号 | 1 | 2 | 3 |
| 20.02 | 19.98 | 20.00 |

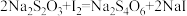
(6)合适的指示剂是
(7)该产品的纯度为
(8)经过讨论,同学认为该产品中可能含有硝酸钠,它会使测定结果
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】CuCl2广泛应用于工业生产,溶于水形成绿色溶液。CuCl晶体呈白色,露置于潮湿空气中易被氧化,实验室用图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。
(1)完成上述实验,气流方向连接各仪器接口的顺序是________ a→______ 、____ →______ 、_____ →______ 、 _________ →________ ;反应时,盛粗铜粉的试管中现象是_______________ 。
(2)实验完毕,取试管中的固体有盐酸溶解后,欲提纯氯化铜,请简述实验方案:_________________ 。(室温,Fe(OH))3 沉淀完全的pH为3.2)
(3)向制得的氯化铜溶液中通入SO2,加热一段时间既可制得CuCl,写出该反应的离子方式:_______ 。
(4)已知:ⅰ.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ⅱ.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
某同学利用如图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成
①D瓶测定__________ ;F洗气瓶中盛放的试剂是__________________ 。
②E瓶中发生反应的离子方程式为____________________ 。
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意__________ 。
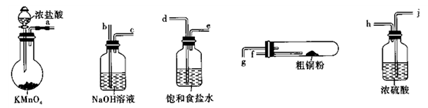
(1)完成上述实验,气流方向连接各仪器接口的顺序是
(2)实验完毕,取试管中的固体有盐酸溶解后,欲提纯氯化铜,请简述实验方案:
(3)向制得的氯化铜溶液中通入SO2,加热一段时间既可制得CuCl,写出该反应的离子方式:
(4)已知:ⅰ.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ⅱ.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
某同学利用如图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成
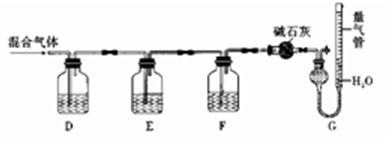
①D瓶测定
②E瓶中发生反应的离子方程式为
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得(已知苯甲酸的酸性强于碳酸),反应装置如图(部分装置省略),反应原理如下:

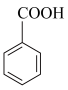 +C2H5OH
+C2H5OH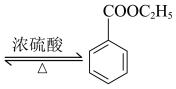 +H2O
+H2O
实验操作步骤:
①向三颈烧瓶内加入12.2 g苯甲酸、25 mL乙醇、20 mL苯及4 mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80 mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25 mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210—213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8 mL。
可能用到的有关数据如下:
回答以下问题:
(1)反应装置中分水器上方的仪器名称是______
(2)步骤①中加浓硫酸的作用是________ ,加沸石的目的是______ 。
(3)步骤②中使用分水器除水的目的是__________ 。
(4)步骤③中加入碳酸钠的目的是____________ 。
(5)步骤④中有机层从分液漏斗的____ (选填“上口倒出”或“下口放出”)。
(6)蒸馏操作中温度计水银球的位置应为下图中________ (填a、b、c、d)所示。
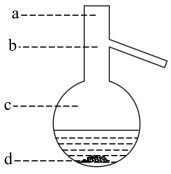
(7)本实验所得到的苯甲酸乙酯产率______ %。

 +C2H5OH
+C2H5OH +H2O
+H2O实验操作步骤:
①向三颈烧瓶内加入12.2 g苯甲酸、25 mL乙醇、20 mL苯及4 mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80 mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25 mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210—213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8 mL。
可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
| 苯甲酸乙酯 | 150 | 1.05 | 211~213 | 微溶于水,溶于乙醇、乙醚 |
| 乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
| 乙醚 | 74 | 0.73 | 34.4 | 微溶于水 |
(1)反应装置中分水器上方的仪器名称是
(2)步骤①中加浓硫酸的作用是
(3)步骤②中使用分水器除水的目的是
(4)步骤③中加入碳酸钠的目的是
(5)步骤④中有机层从分液漏斗的
(6)蒸馏操作中温度计水银球的位置应为下图中

(7)本实验所得到的苯甲酸乙酯产率
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
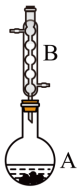
【推荐1】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应装置示意图如图:
反应为: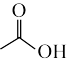 +
+
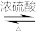
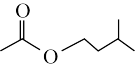 +H2O
+H2O
相关物质性质如表:
实验步骤:在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140-143℃馏分,得乙酸异戊酯3.9g。回答下列问题:
(1)装置B的名称是____ ;主要作用是:____ 。
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作时____ (填序号)。
(3)在洗涤操作中,第一次水洗的主要目的是____ 。
(4)实验中加入少量无水硫酸镁的目的是____ 。
(5)本实验的产率是____ 。
(6)在进行蒸馏操作时,若从130℃开始收集馏分,产率会偏____ (填“高”或“低”)。

反应为:
 +
+
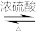
 +H2O
+H2O相关物质性质如表:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
(1)装置B的名称是
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作时
| A.立即补加 | B.冷却后补加 | C.不需补加 | D.重新配料 |
(4)实验中加入少量无水硫酸镁的目的是
(5)本实验的产率是
(6)在进行蒸馏操作时,若从130℃开始收集馏分,产率会偏
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】乙醚在医学上可用作麻醉剂。实验室合成乙醚的原理如下:
(Ⅰ)乙醚的制备
主反应:
副反应: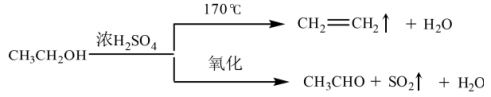


实验装置如图所示(夹持装置和加热装置略)
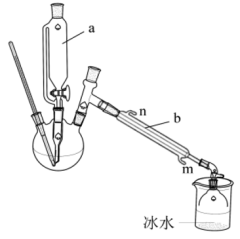
在干燥的三颈烧瓶中先加入12ml无水乙醇(ρ=0.8g/mL),再缓缓加入12ml浓 混合均匀。在滴液漏斗中加入25mL无水乙醇。
混合均匀。在滴液漏斗中加入25mL无水乙醇。
如图连接好装置。
用电热套加热,使反应温度迅速升到140℃。开始由滴液漏斗慢慢滴加乙醇。
控制滴入速度与馏出液速度大致相等(1滴/s)。
维持反应温度在135-145℃内30-45min滴完,再继续加热10min,直到温度升到160℃,停止反应。
(1)仪器b是_______ (写名称),冷却水的通向是_______ (填m进n出或n进m出)。
(2)接受瓶置于冰水中的目的是_______ 。
(3)实验开始后应使反应温度迅速升到并维持在135-145℃,原因是_______ 。
(Ⅱ)乙醚的精制
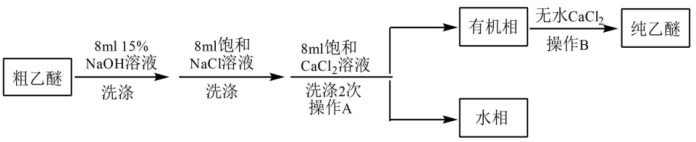
(4)粗乙醚用NaOH溶液洗涤的目的是_______ 。
(5)饱和NaCl溶液洗涤目的是洗去残留在乙醚中的碱,选用饱和NaCl溶液而不用水洗涤的原因是_______ 。
(6)操作B是_______ ,并收集_______ ℃的馏分。
(7)经干燥得到纯乙醚14.8g,则所获产品的产率是_______ (保留3位有效数字)。
(Ⅰ)乙醚的制备
主反应:

副反应:



实验装置如图所示(夹持装置和加热装置略)

| 无水乙醚 微溶于水 熔点-116.2℃ 沸点34.5℃ 摩尔质量74g/mol 空气中遇热易爆炸 |
 混合均匀。在滴液漏斗中加入25mL无水乙醇。
混合均匀。在滴液漏斗中加入25mL无水乙醇。如图连接好装置。
用电热套加热,使反应温度迅速升到140℃。开始由滴液漏斗慢慢滴加乙醇。
控制滴入速度与馏出液速度大致相等(1滴/s)。
维持反应温度在135-145℃内30-45min滴完,再继续加热10min,直到温度升到160℃,停止反应。
(1)仪器b是
(2)接受瓶置于冰水中的目的是
(3)实验开始后应使反应温度迅速升到并维持在135-145℃,原因是
(Ⅱ)乙醚的精制

(4)粗乙醚用NaOH溶液洗涤的目的是
(5)饱和NaCl溶液洗涤目的是洗去残留在乙醚中的碱,选用饱和NaCl溶液而不用水洗涤的原因是
(6)操作B是
(7)经干燥得到纯乙醚14.8g,则所获产品的产率是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室制备环己酮的反应原理:
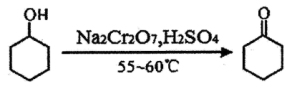


其反应的装置示意图如上(夹持装置、加热装置略去):
环己醇、环己酮、饱和食盐水和水的部分物理性质见下表(注:括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点)
实验步骤:
Ⅰ、实验中通过装置 将酸性
将酸性 溶液分批滴加到盛有
溶液分批滴加到盛有 环己醇的
环己醇的 中,加入第一批
中,加入第一批 溶液后,待反应物的橙红色消失后再加入第二批…依次进行下去,直至反应结束,控制反应在
溶液后,待反应物的橙红色消失后再加入第二批…依次进行下去,直至反应结束,控制反应在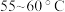 进行。氧化反应结束后,向反应液中加入适量的草酸(
进行。氧化反应结束后,向反应液中加入适量的草酸( )。
)。
Ⅱ、反应完成后,加入适量水,蒸馏,收集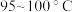 的馏分,得到主要含环己酮粗品和水的混合物。
的馏分,得到主要含环己酮粗品和水的混合物。
Ⅲ、进一步分离提纯得到精环己酮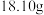 。
。
(1)仪器 的名称是
的名称是_______ 。
(2)为什么要分批次滴加酸性 溶液
溶液_______ 。
(3)蒸馏不能分离环己酮和水的原因是_______ 。
(4)反应要控制在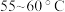 进行,不能过高或过低的原因
进行,不能过高或过低的原因_______ 。
(5)写出草酸与酸性重铬酸钠反应的离子方程式_______ 。
(6)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集 馏分,得到精品
馏分,得到精品
b. 过滤
c. 在收集到的粗品中加 固体至饱和,静置,分液
固体至饱和,静置,分液
d. 加入无水 固体,除去有机物中少量水
固体,除去有机物中少量水
①上述操作的正确顺序是_______ (填序号)。
②在上述操作c中,加入 固体的作用是
固体的作用是_______ 。
(7)环己酮的产率_______ 。
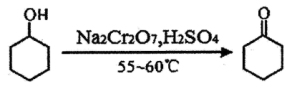


其反应的装置示意图如上(夹持装置、加热装置略去):
环己醇、环己酮、饱和食盐水和水的部分物理性质见下表(注:括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点)
| 物质 | 密度/( ) ) | 沸点/ | 部分性质 |
| 环己醇 | 0.962 | 161.1(97.8) | 能溶于水,具有还原性,易被氧化 |
| 环己酮 | 0.948 | 155.6(95) | 微溶于水,遇氧化剂易发生开环反应 |
| 饱和食盐水 | 1.330 | 108.0 | |
| 水 | 0.998 | 100.0 |
Ⅰ、实验中通过装置
 将酸性
将酸性 溶液分批滴加到盛有
溶液分批滴加到盛有 环己醇的
环己醇的 中,加入第一批
中,加入第一批 溶液后,待反应物的橙红色消失后再加入第二批…依次进行下去,直至反应结束,控制反应在
溶液后,待反应物的橙红色消失后再加入第二批…依次进行下去,直至反应结束,控制反应在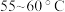 进行。氧化反应结束后,向反应液中加入适量的草酸(
进行。氧化反应结束后,向反应液中加入适量的草酸( )。
)。Ⅱ、反应完成后,加入适量水,蒸馏,收集
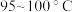 的馏分,得到主要含环己酮粗品和水的混合物。
的馏分,得到主要含环己酮粗品和水的混合物。Ⅲ、进一步分离提纯得到精环己酮
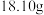 。
。(1)仪器
 的名称是
的名称是(2)为什么要分批次滴加酸性
 溶液
溶液(3)蒸馏不能分离环己酮和水的原因是
(4)反应要控制在
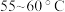 进行,不能过高或过低的原因
进行,不能过高或过低的原因(5)写出草酸与酸性重铬酸钠反应的离子方程式
(6)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集
 馏分,得到精品
馏分,得到精品b. 过滤
c. 在收集到的粗品中加
 固体至饱和,静置,分液
固体至饱和,静置,分液d. 加入无水
 固体,除去有机物中少量水
固体,除去有机物中少量水①上述操作的正确顺序是
②在上述操作c中,加入
 固体的作用是
固体的作用是(7)环己酮的产率
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】1828年,德国化学家弗里德里希·维勒首次使用(NH4)2SO4与氰酸钾KCNO人工合成了尿素CO(NH2)2,打破了有机化合物的"生命力"学说。
(1) (NH4)2SO4与KCNO合成尿素反应的化学方程式为____________ 。
(2)某小组同学在实验室条件下,拟用CO2和NH3,在催化剂的作用下合成尿素。
①用CO2和NH3合成尿素CO(NH2)2反应的化学方程式为____________ 。
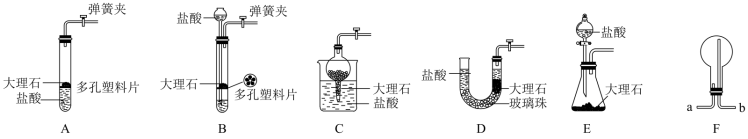
②实验所需的CO2可用多种装置来制备,要想达到“随开随用、随关随停”的目的,下列装置A、B、C、D、E中符和要求的有____________ (填字母)。
③若用F装置收集氨气,则气体应由导管口____________ (填“a”或“b”)进入。
(3)尿素样品中氮含量可以用甲醛法标定,其原理如下:首先用浓硫酸分解试样,使试液中的胺生成硫酸铵并放出二氧化碳;将过量的硫酸中和后得到中性铵盐,再用甲醛(HCHO)与硫酸铵作用生成六次甲基四铵盐离子(CH2)6N4 H+和硫酸;最后用标准氢氧化钠溶液滴定。
①甲醛与硫酸铵反应的离子方程式为____________ ;
②滴定选用的指示剂为____________ 。滴定终点的现象为____________ 。
③若称取样品m g,溶解后配成250mL溶液。取25.00mL样品溶液于250 mL锥形瓶中,加入10mL w%的甲醛溶液,充分反应后,加入1~2滴指示剂,用浓度为a mol/L的NaOH标准溶液滴定至终点(已知滴定时,1 mol六次甲基四铵盐离子(CH2)6N4H+消耗OH﹣的能力与1mol H+相当)。重复2次,消耗NaOH标准溶液的体积平均值为b mL。则该样品中氮的质量分数为____________ 。
(1) (NH4)2SO4与KCNO合成尿素反应的化学方程式为
(2)某小组同学在实验室条件下,拟用CO2和NH3,在催化剂的作用下合成尿素。
①用CO2和NH3合成尿素CO(NH2)2反应的化学方程式为
②实验所需的CO2可用多种装置来制备,要想达到“随开随用、随关随停”的目的,下列装置A、B、C、D、E中符和要求的有
③若用F装置收集氨气,则气体应由导管口

(3)尿素样品中氮含量可以用甲醛法标定,其原理如下:首先用浓硫酸分解试样,使试液中的胺生成硫酸铵并放出二氧化碳;将过量的硫酸中和后得到中性铵盐,再用甲醛(HCHO)与硫酸铵作用生成六次甲基四铵盐离子(CH2)6N4 H+和硫酸;最后用标准氢氧化钠溶液滴定。
①甲醛与硫酸铵反应的离子方程式为
②滴定选用的指示剂为
③若称取样品m g,溶解后配成250mL溶液。取25.00mL样品溶液于250 mL锥形瓶中,加入10mL w%的甲醛溶液,充分反应后,加入1~2滴指示剂,用浓度为a mol/L的NaOH标准溶液滴定至终点(已知滴定时,1 mol六次甲基四铵盐离子(CH2)6N4H+消耗OH﹣的能力与1mol H+相当)。重复2次,消耗NaOH标准溶液的体积平均值为b mL。则该样品中氮的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】处理含铬[Cr(Ⅵ)]废水的方法有化学沉淀法、铝还原回收法等。已知 在溶液中存在如下平衡:
在溶液中存在如下平衡: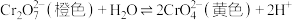 。
。
(1)钡盐沉铬法:向含 的酸性废水中加入钡盐,生成难溶于水的
的酸性废水中加入钡盐,生成难溶于水的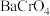 沉淀。使用
沉淀。使用 的沉铬效果要优于
的沉铬效果要优于 的原因是
的原因是_______ ,
(2)亚硫酸氢钠-石灰乳还原沉淀法:向初始pH不等的几份酸性含铬废水中加入等量 ,使
,使 还原成
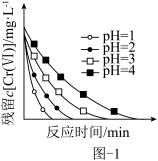
还原成 。测得废水中残留
。测得废水中残留 与反应时间的关系变化关系如图-1所示。
与反应时间的关系变化关系如图-1所示。
①写出 将
将 还原为
还原为 的离子方程式:
的离子方程式:_______ ,
②实际生产中,还原反应控制 为2.5左右的原因是
为2.5左右的原因是_______ 。
(3)还原回收 法:
法:
步骤I:向含 的酸性溶液中加入一定量的铝粉,充分反应,过滤。
的酸性溶液中加入一定量的铝粉,充分反应,过滤。
步骤Ⅱ:利用步骤I过滤后得到的溶液(含有 、
、 、
、 )制备
)制备 晶体。
晶体。
①研究发现,若步骤I中 偏低将会导致
偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是_______ 。
②步骤获得 晶体的实验方案为,向过滤后的溶液中
晶体的实验方案为,向过滤后的溶液中_______ ,冰水洗涤,干燥。(实验中须用到的试剂: 溶液、
溶液、 溶液、稀硫酸)
溶液、稀硫酸)
已知:i.碱性条件下 能被
能被 氧化为
氧化为 ;酸性条件下
;酸性条件下 能将
能将 还原为
还原为 。
。
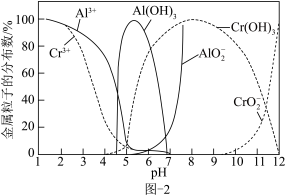
ii.常温下,体系中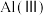 、
、 微粒的分布分数随溶液pH的变化如图-2所示(部分无关粒子已略去)。
微粒的分布分数随溶液pH的变化如图-2所示(部分无关粒子已略去)。
iii.不同温度下 和
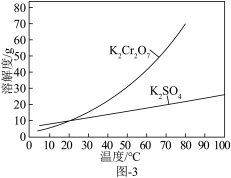
和 的溶解度如图-3所示。
的溶解度如图-3所示。
 在溶液中存在如下平衡:
在溶液中存在如下平衡: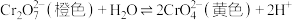 。
。(1)钡盐沉铬法:向含
 的酸性废水中加入钡盐,生成难溶于水的
的酸性废水中加入钡盐,生成难溶于水的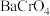 沉淀。使用
沉淀。使用 的沉铬效果要优于
的沉铬效果要优于 的原因是
的原因是(2)亚硫酸氢钠-石灰乳还原沉淀法:向初始pH不等的几份酸性含铬废水中加入等量
 ,使
,使 还原成
还原成 。测得废水中残留
。测得废水中残留 与反应时间的关系变化关系如图-1所示。
与反应时间的关系变化关系如图-1所示。
①写出
 将
将 还原为
还原为 的离子方程式:
的离子方程式:②实际生产中,还原反应控制
 为2.5左右的原因是
为2.5左右的原因是(3)还原回收
 法:
法:步骤I:向含
 的酸性溶液中加入一定量的铝粉,充分反应,过滤。
的酸性溶液中加入一定量的铝粉,充分反应,过滤。步骤Ⅱ:利用步骤I过滤后得到的溶液(含有
 、
、 、
、 )制备
)制备 晶体。
晶体。①研究发现,若步骤I中
 偏低将会导致
偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是②步骤获得
 晶体的实验方案为,向过滤后的溶液中
晶体的实验方案为,向过滤后的溶液中 溶液、
溶液、 溶液、稀硫酸)
溶液、稀硫酸)已知:i.碱性条件下
 能被
能被 氧化为
氧化为 ;酸性条件下
;酸性条件下 能将
能将 还原为
还原为 。
。ii.常温下,体系中
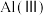 、
、 微粒的分布分数随溶液pH的变化如图-2所示(部分无关粒子已略去)。
微粒的分布分数随溶液pH的变化如图-2所示(部分无关粒子已略去)。
iii.不同温度下
 和
和 的溶解度如图-3所示。
的溶解度如图-3所示。
您最近一年使用:0次
【推荐3】废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
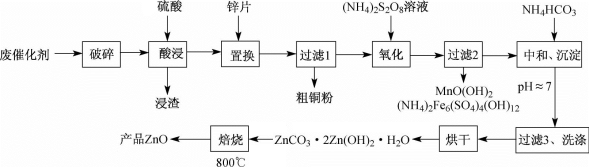
(1)为提高酸浸的速率,还可采取的措施为___ 。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___ 。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___ 。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___ (填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___ 。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___ %,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___ (填“偏大”“偏小”或“无影响”)。

(1)为提高酸浸的速率,还可采取的措施为
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得
(5)“焙烧”过程中化学方程式为
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为
您最近一年使用:0次

 标准溶液体积/mL
标准溶液体积/mL

