根据下列要求,回答问题:
(1)现有下列物质:①氢氧化钾固体;②稀硫酸;③铜片;④蔗糖(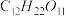 )固体;⑤熔融的氯化钠。其中属于电解质的是
)固体;⑤熔融的氯化钠。其中属于电解质的是__________ (填序号)。
(2)下列装置能构成原电池的是__________ (填写字母序号)。
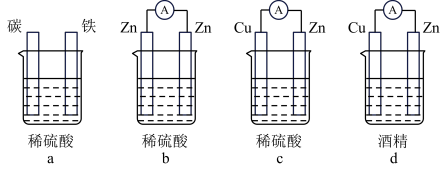
(3)在2A+B 2C+D反应中,表示该反应最快的是
2C+D反应中,表示该反应最快的是__________ (填写字母序号)。
a.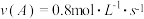 b.
b.
c.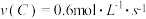 d.
d.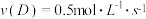
(4)甲烷的燃烧热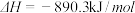 ,则甲烷燃烧的热化学方程式可表示为
,则甲烷燃烧的热化学方程式可表示为_______ 。
(5)90℃时,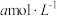 一元酸HA与
一元酸HA与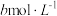 NaOH溶液等体积混合后,混合液的pH为7,则溶液中所有离子的浓度由大到小的顺序是
NaOH溶液等体积混合后,混合液的pH为7,则溶液中所有离子的浓度由大到小的顺序是_________________________________ 。
(1)现有下列物质:①氢氧化钾固体;②稀硫酸;③铜片;④蔗糖(
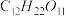 )固体;⑤熔融的氯化钠。其中属于电解质的是
)固体;⑤熔融的氯化钠。其中属于电解质的是(2)下列装置能构成原电池的是

(3)在2A+B
 2C+D反应中,表示该反应最快的是
2C+D反应中,表示该反应最快的是a.
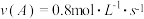 b.
b.
c.
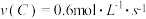 d.
d.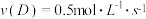
(4)甲烷的燃烧热
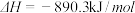 ,则甲烷燃烧的热化学方程式可表示为
,则甲烷燃烧的热化学方程式可表示为(5)90℃时,
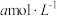 一元酸HA与
一元酸HA与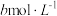 NaOH溶液等体积混合后,混合液的pH为7,则溶液中所有离子的浓度由大到小的顺序是
NaOH溶液等体积混合后,混合液的pH为7,则溶液中所有离子的浓度由大到小的顺序是
更新时间:2020-06-23 23:30:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下列物质中,属于强电解质的是(填序号,下同)_____ ,属于弱电解质的是____ ,属于非电解质____ ;
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列十种物质:①CH3COOH ②铝 ③CaCO3固体 ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水 ⑨FeCl3 溶液 ⑩Na HSO4固体
(1)以上物质属于电解质的是__________ (填序号,下同),在熔融态不导电而水溶液中导电的电解质是__________ 。
(2)写出⑩在水溶液中的电离方程式_____________________________________
(3)将⑨的饱和溶液滴入沸水中可以制得⑦,写出该化学方程式____________ 是否制备成功可以用 _____________________________________ 方法检验,
(4)⑤的稀溶液与⑥反应,写出该反应的离子方程式______________________________
(5)少量④与澄清石灰水反应的离子反应方程式:_________________________________
(1)以上物质属于电解质的是
(2)写出⑩在水溶液中的电离方程式
(3)将⑨的饱和溶液滴入沸水中可以制得⑦,写出该化学方程式
(4)⑤的稀溶液与⑥反应,写出该反应的离子方程式
(5)少量④与澄清石灰水反应的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下物质:①碳酸钠 ②KOH溶液 ③Fe(OH)3固体 ④甲烷 ⑤铁或石墨 ⑥盐酸⑦CO2 ⑧熔融CuSO4。
(1)①属于电解质的有___ (填序号,下同)。
②属于非电解质的有___ 。
③能导电的有___ 。
④既不是电解质又不是非电解质的是___ 。
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3:___ 。
②KOH:___ 。
③CuSO4:___ 。
④HCl:___ 。
(3)制备Fe(OH)3胶体的化学方程式是___ 。
(4)写出实验室检验CO2的离子方程式:___ 。
(1)①属于电解质的有
②属于非电解质的有
③能导电的有
④既不是电解质又不是非电解质的是
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3:
②KOH:
③CuSO4:
④HCl:
(3)制备Fe(OH)3胶体的化学方程式是
(4)写出实验室检验CO2的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有人利用碳还原法将氮氧化物(以NO为例)转化为无毒无害的气体。回答下列问题:
(1)碳还原法发生反应的化学方程式为C(s)+2NO(g) N2(g)+CO2(g)。能使化学反应速率加快的措施有
N2(g)+CO2(g)。能使化学反应速率加快的措施有___ (填序号,下同),其中属于增大活化分子百分含量的是___ 。
①增加C的物质的量②定容密闭容器中继续充入NO③在反应器中加入NaOH溶液④升高反应温度⑤缩小容器体积
(2)向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如表所示:
①10~20min内,N2的平均反应速率v(N2)=___ 。
②在30min时向容器中加入合适催化剂,v(正)___ ,v(逆)___ 。(填“增大”“减小”或“不变”)
(1)碳还原法发生反应的化学方程式为C(s)+2NO(g)
 N2(g)+CO2(g)。能使化学反应速率加快的措施有
N2(g)+CO2(g)。能使化学反应速率加快的措施有①增加C的物质的量②定容密闭容器中继续充入NO③在反应器中加入NaOH溶液④升高反应温度⑤缩小容器体积
(2)向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如表所示:
| 时间/min 浓度/(mol•L-1) 物质 | 0 | 10 | 20 | 30 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 |
| N2 | 0 | 0.16 | 0.25 | 0.25 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 |
②在30min时向容器中加入合适催化剂,v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】近日IPCC发布了由来自40个国家的91位科学家编写的《全球升温1.5℃特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,CO2的减排和综合利用是解决温室及能源问题的有效途径。
(1)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)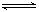 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
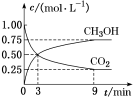
① 从3 min到9 min,v(H2)=_____ mol·L-1·min-1。
② 该反应的平衡常数为_______ 。
③ 下列说法正确的的是____ (填字母)。
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时CO2的转化率为75%
C.平衡时混合气体中CH3OH(g)的体积分数是30%
D.该条件下,第9 min时v逆(CH3OH)大于第3 min时v正(CH3OH)。
(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g)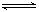 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+H2(g)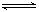 CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。
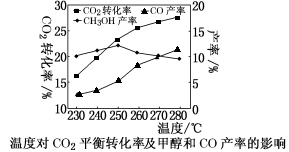
① 由图可知温度升高CO的产率上升,其主要原因可能是________ 。
② 由图可知获取CH3OH最适宜的温度是________ 。下列措施有利于提高CO2转化为CH3OH的平衡转化率的有___________ (填字母)。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
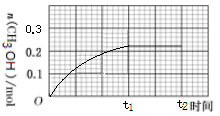
(3)250 ℃下CH3OH物质的量随时间的变化曲线如图所示。画出280 ℃下0~t2时刻CH3OH物质的量随时间的变化曲线示意图__________ 。
(1)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)
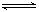 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
① 从3 min到9 min,v(H2)=
② 该反应的平衡常数为
③ 下列说法正确的的是
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时CO2的转化率为75%
C.平衡时混合气体中CH3OH(g)的体积分数是30%
D.该条件下,第9 min时v逆(CH3OH)大于第3 min时v正(CH3OH)。
(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g)
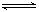 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)反应B:CO2(g)+H2(g)
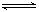 CO(g)+H2O(g)
CO(g)+H2O(g)控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。

① 由图可知温度升高CO的产率上升,其主要原因可能是
② 由图可知获取CH3OH最适宜的温度是
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(3)250 ℃下CH3OH物质的量随时间的变化曲线如图所示。画出280 ℃下0~t2时刻CH3OH物质的量随时间的变化曲线示意图

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.(1)25℃时, 的醋酸和
的醋酸和 的氢氧化钠溶液等体积混合后,溶液呈
的氢氧化钠溶液等体积混合后,溶液呈___________ (填“酸性”、“中性”或“碱性”),请写出溶液中离子浓度间的一个等式关系:___________ 。
(2)25℃时,将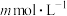 的醋酸和
的醋酸和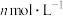 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中
___________  ,m与n的大小关系是m
,m与n的大小关系是m___________ n(填“>”“=”或“<”)。
Ⅱ.化工原料异丁烯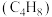 可由异丁烷
可由异丁烷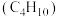 直接催化脱氢制备:
直接催化脱氢制备: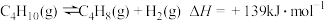

(1)该反应的化学平衡常数的表达式为___________ 。
(2)一定条件下,以异丁烷为原料生产异丁烯,温度、压强改变对异丁烷平衡转化率的影响如图所示。
①判断x___________ 0.1(填“大于”或“小于”),理由是___________ 。
②若异丁烷的平衡转化率为45%,则平衡混合气中异丁烯的物质的量分数为___________ %(保留小数点后1位)。
 的醋酸和
的醋酸和 的氢氧化钠溶液等体积混合后,溶液呈
的氢氧化钠溶液等体积混合后,溶液呈(2)25℃时,将
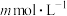 的醋酸和
的醋酸和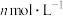 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中
 ,m与n的大小关系是m
,m与n的大小关系是mⅡ.化工原料异丁烯
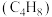 可由异丁烷
可由异丁烷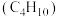 直接催化脱氢制备:
直接催化脱氢制备: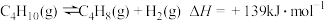

(1)该反应的化学平衡常数的表达式为
(2)一定条件下,以异丁烷为原料生产异丁烯,温度、压强改变对异丁烷平衡转化率的影响如图所示。
①判断x
②若异丁烷的平衡转化率为45%,则平衡混合气中异丁烯的物质的量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室(室温下)存放着如下几种试剂:
①0.1mol/LCH3COOH溶液②0.1mol/LCH3COONa溶液③0.1mol/LNaOH溶液④0.1mol/L盐酸⑤0.1mol/L氨水⑥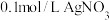 溶液⑦
溶液⑦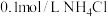 溶液⑧
溶液⑧ 溶液
溶液
回答下列问题:
(1)溶液的 ,且促进水的电离的试剂是
,且促进水的电离的试剂是___________ (填序号,下同)。
(2)试剂①、④、⑥中由水电离的氢离子浓度 由大到小的顺序是
由大到小的顺序是___________ 。
(3)试剂⑤、⑦、⑧溶液中 由大到小的顺序是
由大到小的顺序是___________ 。
(4)将试剂⑤和试剂⑦等体积混合后测得混合溶液显碱性,则混合溶液中离子浓度由大到小的顺序是___________ 。试剂⑦中某离子M的浓度为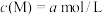 ,将试剂④和试剂⑦等体积混合后测得
,将试剂④和试剂⑦等体积混合后测得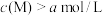 ,则该离子M是
,则该离子M是___________ (填序号)。
A. B.
B. C.
C. D.
D.
(5)试剂⑧中电荷守恒的表达式是___________ 。
(6)已知醋酸的电离常数 ,将试剂①和试剂②等体积混合后,
,将试剂①和试剂②等体积混合后, 的水解常数
的水解常数
___________ 。已知亚硫酸的电离常数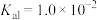 ,
,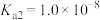 。向
。向 溶液中加入过量试剂①发生反应的离子方程式是
溶液中加入过量试剂①发生反应的离子方程式是___________ 。
①0.1mol/LCH3COOH溶液②0.1mol/LCH3COONa溶液③0.1mol/LNaOH溶液④0.1mol/L盐酸⑤0.1mol/L氨水⑥
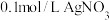 溶液⑦
溶液⑦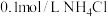 溶液⑧
溶液⑧ 溶液
溶液回答下列问题:
(1)溶液的
 ,且促进水的电离的试剂是
,且促进水的电离的试剂是(2)试剂①、④、⑥中由水电离的氢离子浓度
 由大到小的顺序是
由大到小的顺序是(3)试剂⑤、⑦、⑧溶液中
 由大到小的顺序是
由大到小的顺序是(4)将试剂⑤和试剂⑦等体积混合后测得混合溶液显碱性,则混合溶液中离子浓度由大到小的顺序是
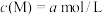 ,将试剂④和试剂⑦等体积混合后测得
,将试剂④和试剂⑦等体积混合后测得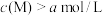 ,则该离子M是
,则该离子M是A.
 B.
B. C.
C. D.
D.
(5)试剂⑧中电荷守恒的表达式是
(6)已知醋酸的电离常数
 ,将试剂①和试剂②等体积混合后,
,将试剂①和试剂②等体积混合后, 的水解常数
的水解常数
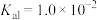 ,
,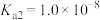 。向
。向 溶液中加入过量试剂①发生反应的离子方程式是
溶液中加入过量试剂①发生反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)已知:25℃时NH3·H2O的Kb=1.0×10-5。
①求0.10mol·L-1的NH3·H2O溶液中c(OH-)=___________ mol·L-1。
②25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,若混合后所得溶液的pH=7,用含a的代数式表示的电离常数Kb=___________ 。
(2)25℃时,H2SO3 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=___________ ,若向NaHSO3溶液中加入少量的Cl2,则溶液中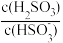 将
将___________ (填“增大”“减小”或“不变”)。
(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH___________ NaOH溶液的pH(填“>”“=”或“<”)。
(4)常温时,取0.1mol·L-1HX溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为___________ 。
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH___________ 7(填“>”“<”或“=”)。
(1)已知:25℃时NH3·H2O的Kb=1.0×10-5。
①求0.10mol·L-1的NH3·H2O溶液中c(OH-)=
②25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,若混合后所得溶液的pH=7,用含a的代数式表示的电离常数Kb=
(2)25℃时,H2SO3
 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=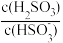 将
将(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH
(4)常温时,取0.1mol·L-1HX溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是某同学设计的一个简易的原电池装置,请回答下列问题。
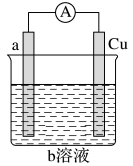
(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为___________________ ,当有3.2g的负极材料溶解时,导线中转移的电子的数目为________ 。
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为_________________ ,该燃料电池的优点是_______________________ 。
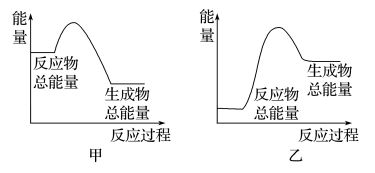
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可________ (填“吸收”或“放出”)热量________ kJ;该反应的能量变化可用图______ (填“甲“或“乙”)表示。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ、根据氧化还原反应:2Ag+(aq)+ Cu(s) = Cu2+(aq)+ 2Ag(s) 设计的原电池如下图所示,其中盐桥为琼脂–饱和KNO3盐桥。请回答下列问题:
(1)电极X的材料是___________ ;电解质溶液Y是 ____________________ 。
(2)银电极为电池的__________ 极,其电极反应式为:___________________________________ 。
(3)盐桥中向CuSO4溶液中迁移的离子是___________ 。

A、K+ B、NO3― C、Ag+ D、SO42―
Ⅱ、酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料。回答下列问题:
(1)该电池的正极反应式为________________________ ,电池反应的离子方程式为________________________________________
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过___________________________________ 分离回收。
(3)滤渣的主要成分是MnO2、碳粉和MnOOH,欲从中得到较纯的MnO2,最简便的方法是_________________________________________ 。
(1)电极X的材料是
(2)银电极为电池的
(3)盐桥中向CuSO4溶液中迁移的离子是

A、K+ B、NO3― C、Ag+ D、SO42―
Ⅱ、酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料。回答下列问题:
(1)该电池的正极反应式为
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过
(3)滤渣的主要成分是MnO2、碳粉和MnOOH,欲从中得到较纯的MnO2,最简便的方法是
您最近一年使用:0次




