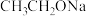室温下的四种溶液:①pH=9的 NaOH 溶液 ②pH=9的CH3COONa溶液 ③pH=5的H2SO4溶液 ④pH=5的NaHSO4 溶液,溶液中由水电离产生的c(OH-)相同的是( )
| A.①② | B.①③ | C.③④ | D.①③④ |
更新时间:2020-06-30 22:16:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知:pOH=−lg c(OH−)。298 K时,在20.00 mL 0.10 mol·L−1盐酸中滴入0.10 mol·L−1的氨水,溶液中的pH和pOH与加入氨水体积的关系如图所示。下列有关叙述正确的是


| A.曲线MJQ表示溶液中pH的变化 |
| B.M、P两点的数值之和pH+pOH=14 |
| C.N点水的电离程度比P点大 |
| D.pH与pOH交叉点J表示V(氨水)=20.00 mL |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++ 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是| A.该温度下加入等体积pH=10的NaOH溶液可使反应后的溶液恰好呈中性 |
| B.水电离出来的c(H+)=1×10-12mol/L |
C.c(H+)=c(OH-)+c( ) ) |
| D.该温度高于25℃ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.[H+]水•[OH-]水=1×10-24的溶液:Al3+、Fe3+、Cl-、SO |
B. =0.1的溶液:K+、NH3•H2O、SO =0.1的溶液:K+、NH3•H2O、SO 、NO 、NO |
C.能使甲基橙变红色的溶液:Na+、NH 、MnO 、MnO 、HCO 、HCO |
D.和Al反应放出H2的溶液:Mg2+、Cu2+、NO 、SO 、SO |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于溶液酸碱性说法不正确的是
A.某温度下,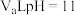 的 的 溶液,与 溶液,与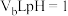 的 的 溶液混合呈中性,则 溶液混合呈中性,则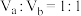 |
B.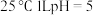 的氯化铵溶液, 的氯化铵溶液,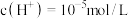 ,由水电离出 ,由水电离出 |
C.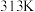 时, 时,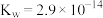 ,则 ,则 ,溶液呈碱性 ,溶液呈碱性 |
D. 时,纯水的 时,纯水的 ,呈中性 ,呈中性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知在100℃的温度下,水的离子积KW=1×10-12.下列说法中正确的是
| A.0.005 mol•L-1的硫酸溶液,pH=2 |
| B.0.001 mol•L-1的氢氧化钠溶液,pH=11 |
| C.0.005mol•L-1的硫酸溶液与0.01mol•L-1的氢氧化钠溶液等体积混合,混合溶液的pH为6,溶液显酸性 |
| D.完全中和pH=3的硫酸溶液50mL,需要pH=11的NaOH溶液50mL |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】298K时,用0.1 mol·L⁻¹的NaOH标准溶液滴定20.0 mL 0.1 mol·L⁻¹ ,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是
,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是

 ,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是
,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是
A.由水电离出来的 :M>N :M>N |
| B.该滴定过程中可以选择石蕊或酚酞为指示剂 |
C. 的 的 大约等于 大约等于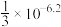 |
D.N点的溶液中: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NA代表阿伏加德罗常数的值。下列说法正确的是
| A.3.9gNa2O2晶体中阴离子的数目为0.1NA |
| B.100mL1mol•L−1FeCl3溶液中所含Fe3+的数目为0.1NA |
| C.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA |
| D.密闭容器中,2molSO2和1molO2催化反应后分子总数为2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】制备[Cu(NH3)4]SO4·H2O的实验操作如下:

设NA为阿伏加德罗常数,下列说法不正确的是

设NA为阿伏加德罗常数,下列说法不正确的是
| A.1L0.1mol·L-1CuSO4溶液中所含的Cu2+数目小于0.1NA |
B.生成蓝色沉淀的离子方程式为: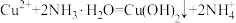 |
| C.0.5 mol NH3·H2O所含的电子数目为10NA |
| D.制得的配合物[Cu(NH3)4]SO4·H2O中由Cu2+提供孤电子对形成配位键 |
您最近半年使用:0次

 时,某溶液中由水电离产生的
时,某溶液中由水电离产生的 的乘积为
的乘积为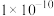 ,则该溶液的溶质可能为
,则该溶液的溶质可能为