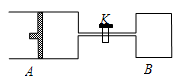
1L恒容密闭容器中充入2molNO和1molCl2反应:2NO(g)+Cl2(g) 2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
 2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是| t/min 温度/℃ | 0 | 5 | 8 | 13 |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
| A.T1>T2 |
| B.T1时,反应前5min的平均速率为v(Cl2)=0.5mol·L-1·min-1 |
| C.反应达平衡时,升高温度促进反应向正反应方向进行 |
| D.T2时,向反应后的容器中充入2molNOCl(g),再次平衡时,c(NOCl)>2mol·L-1 |
2020·浙江宁波·模拟预测 查看更多[3]
浙江省宁波市五校(奉化中学、宁波中学、北仑中学等)2020届高三适应性考试化学试题(已下线)专题09 反应速率、化学平衡-2020年高考真题和模拟题化学分项汇编浙江省瑞安市上海新纪元高级中学2019-2020学年高二下学期期末考试化学试题
更新时间:2020-07-02 10:37:27
|
相似题推荐
单选题
|
较难
(0.4)
名校
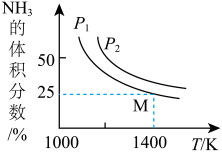
【推荐1】在一体积不变的密闭容器中发生化学反应:Fe2O3(s) +2NH3(g) 2Fe(s)+N2(g)+3H2O(g) △H,实验测得化学平衡时的有关变化曲线如图所示。已知:平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。下列说法不正确的是
2Fe(s)+N2(g)+3H2O(g) △H,实验测得化学平衡时的有关变化曲线如图所示。已知:平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。下列说法不正确的是
 2Fe(s)+N2(g)+3H2O(g) △H,实验测得化学平衡时的有关变化曲线如图所示。已知:平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。下列说法不正确的是
2Fe(s)+N2(g)+3H2O(g) △H,实验测得化学平衡时的有关变化曲线如图所示。已知:平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。下列说法不正确的是
| A.该反应的△H>0 |
| B.气体压强P2 >P1 |
| C.平衡后再加入Fe2O3,则NH3转化率增大 |
D.M点的平衡常数Kp=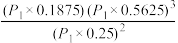 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g)  PCl3(g)+Cl2(g),下列说法正确的是
PCl3(g)+Cl2(g),下列说法正确的是
 PCl3(g)+Cl2(g),下列说法正确的是
PCl3(g)+Cl2(g),下列说法正确的是| 编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡 所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A.平衡常数K:容器Ⅱ>容器Ⅲ |
| B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ |
| C.反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol•L-1•s-1 |
| D.容器Ⅲ中平衡后,等温条件下充入一定量He,平衡不发生移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应1: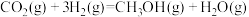

反应2:
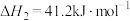
恒压下,将起始 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
的选择性[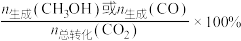 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法不 正确的是
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应1:
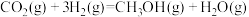

反应2:

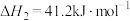
恒压下,将起始
 的混合气体以一定流速通过装有催化剂的反应管,测得出口处
的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及
的转化率及 和
和 的选择性[
的选择性[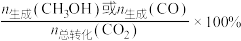 ]随温度的变化如下图所示。下列说法
]随温度的变化如下图所示。下列说法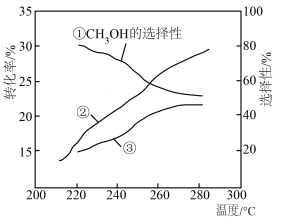
A.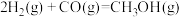 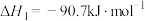 |
| B.曲线③表示CO的选择性 |
C.280℃时出口处 的物质的量分数比220℃时小 的物质的量分数比220℃时小 |
D.为提高 生产效率,需研发单位时间 生产效率,需研发单位时间 转化率高和 转化率高和 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】CO还原 的化学方程式为
的化学方程式为 。在体积均为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入
。在体积均为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入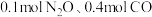 和相同催化剂。实验测得A、B容器中
和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示。该反应的反应速率
的转化率随时间的变化关系如图所示。该反应的反应速率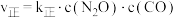 ,
, 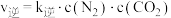 。
。 分别是正、逆反应速率常数。下列说法错误的是
分别是正、逆反应速率常数。下列说法错误的是
 的化学方程式为
的化学方程式为 。在体积均为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入
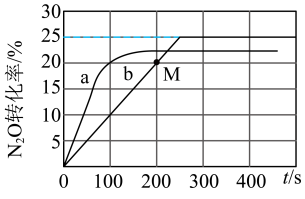
。在体积均为1L的密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入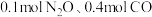 和相同催化剂。实验测得A、B容器中
和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示。该反应的反应速率
的转化率随时间的变化关系如图所示。该反应的反应速率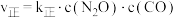 ,
, 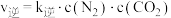 。
。 分别是正、逆反应速率常数。下列说法错误的是
分别是正、逆反应速率常数。下列说法错误的是
A.A容器中 的转化率随时间的变化关系是b曲线 的转化率随时间的变化关系是b曲线 |
B.要缩短b曲线对应容器达到平衡的时间,但不改变 的平衡转化率,在催化剂一定的情况下可采取缩小容器体积的措施 的平衡转化率,在催化剂一定的情况下可采取缩小容器体积的措施 |
| C.该反应正向为放热反应 |
D.M点处的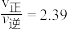 |
您最近一年使用:0次

 时,在两个容积均为2L的恒容密闭容器中仅发生反应
时,在两个容积均为2L的恒容密闭容器中仅发生反应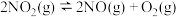 (正反应吸热)。实验测得:v(正)
(正反应吸热)。实验测得:v(正)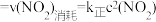 ,v(逆)
,v(逆) ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
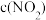



 ,且
,且 ,则
,则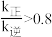
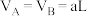 ,在相同温度和催化剂的条件下,两容器中各自发生下列反应:
,在相同温度和催化剂的条件下,两容器中各自发生下列反应: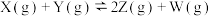
 ;达到平衡时,
;达到平衡时,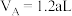 ,则下列说法不正确的是
,则下列说法不正确的是