将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:| 压强/Mpa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | e | f | 83.0 |
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
| A.4个 | B.3个 | C.2个 | D.1个 |
更新时间:2020-08-19 22:52:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)⇌pC(g)(m+n≠p)的速率和平衡的影响,图象如图,下列判断正确的是

| A.图d中,曲线a一定增加了催化剂 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.由图a可知,T1>T2,该反应的逆反应为放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实能用勒夏特列原理来解释的是
A.实验室采用排饱和食盐水的方法收集氯气: |
B.500℃温度比室温更有利于合成氨反应:  |
C.H2、I2、HI平衡混合气体加压后颜色加深: |
D.SO2被氧化为SO3,往往需要使用催化剂: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图为一带可移动隔板的密闭容器,某温度下,左、右两侧反应均达到平衡,此时隔板处于容器中央。若保持温度不变,向左侧容器中充入一定量的H2,下列说法正确的是
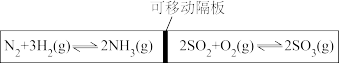
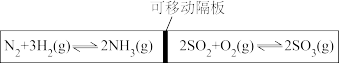
| A.两侧平衡均向正反应方向移动 |
| B.左侧平衡向逆反应方向移动 |
| C.右侧平衡向逆反应方向移动 |
| D.两侧平衡均向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】对于可逆反应:2A(g)+B(g) 2C(g) ΔH<0,下列各图中正确的是
2C(g) ΔH<0,下列各图中正确的是
 2C(g) ΔH<0,下列各图中正确的是
2C(g) ΔH<0,下列各图中正确的是A. | B. |
C.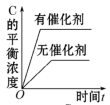 | D.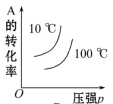 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应A(g)+B(g) 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是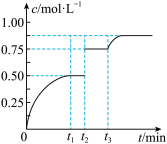
| A.若t1=2min,则v(D)=0.125mol/(L·min) |
| B.t2时刻改变的条件是增加等物质的量的A和B |
| C.t1时刻后向体系中再充入A、B、C各1mol,则v正>v逆 |
| D.若t3时刻改变的条件是升温,则该反应是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将一定量的X加入某密闭容器中,发生反应: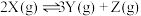 ,平衡时混合气体中X的物质的量分数与温度关系如图所示。下列推断正确的是
,平衡时混合气体中X的物质的量分数与温度关系如图所示。下列推断正确的是
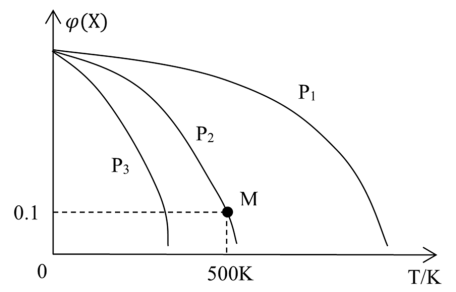
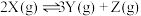 ,平衡时混合气体中X的物质的量分数与温度关系如图所示。下列推断正确的是
,平衡时混合气体中X的物质的量分数与温度关系如图所示。下列推断正确的是
| A.平衡后加入高效催化剂可使混合气体的平均摩尔质量增大 |
B.压强大小有: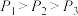 |
| C.升高温度,该反应平衡常数K减小 |
D.在该条件下M点X平衡转化率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在2L恒容密闭容器中充入2 mol SO2和1 mol O2发生反应: ,其他条件相同,混合体系中SO2的体积分数(x)随温度变化的关系如图所示。下列推断正确的是
,其他条件相同,混合体系中SO2的体积分数(x)随温度变化的关系如图所示。下列推断正确的是
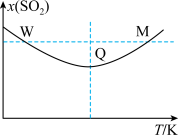
 ,其他条件相同,混合体系中SO2的体积分数(x)随温度变化的关系如图所示。下列推断正确的是
,其他条件相同,混合体系中SO2的体积分数(x)随温度变化的关系如图所示。下列推断正确的是
| A.Q点时,SO2的转化率最大 |
| B.W点与M点SO2的反应速率相等 |
| C.Q点时,充入:2 mol SO2和1 mol O2,重新平衡后SO2的平衡转化率与原平衡相等 |
D.M点时,充入SO3气体,重新平衡后SO2的体积分数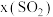 比原平衡大 比原平衡大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“碳达峰·碳中和”是我国社会发展的重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关主要反应有:
Ⅰ:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
下列说法正确的是
Ⅰ:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
CO(g)+H2O(g) ΔH2=+41kJ/mol,K2下列说法正确的是
A.反应Ⅰ的平衡常数K1=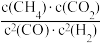 |
| B.反应Ⅱ的ΔS<0 |
| C.有利于提高CO2平衡转化率的条件是高温低压 |
| D.该工艺每转化0.2mol CO2可获得0.4molCO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2M(k1、k2为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法不正确 的是
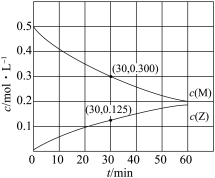

| A.反应①的活化能比反应②的活化能大 |
| B.反应开始后,体系中Y和Z的浓度之比保持不变 |
| C.如果反应能进行到底,反应结束时62.5%的M转化为Z |
| D.0~30min时间段内,Y的平均反应速率为6.67×10-8mol·L-1·min-1 |
您最近一年使用:0次


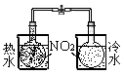


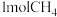 和一定量的
和一定量的  ,发生反应
,发生反应 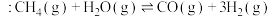 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比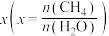 随温度的变化曲线如图所示。下列说法
随温度的变化曲线如图所示。下列说法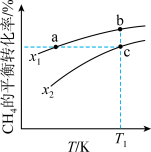

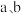 两点对应的混合气体的平均相对分子质量:
两点对应的混合气体的平均相对分子质量:
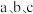 对应的平衡常数:
对应的平衡常数:
 ,当容器内密度不变时,反应达到平衡状态
,当容器内密度不变时,反应达到平衡状态

