MnS 纳米粒子被广泛应用于除去重金属离子中的隔离子。
(1) 锰的价层电子排布式为_____________ ,Mn2+中未成对电子数为_______ 。
(2) 磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子 的半径大小 :__________ ,常温下H2O是液态 而H2S是气态的原因是__________ 。
(3)Mn 可以形成多种配合物,[Mn(CO )(H2O)2(NH3)3] Cl2• H2O中第二周期元素第一电离能大小关系为_____________ ,配体H2O、NH3中心原子杂化类型均为_________ 。
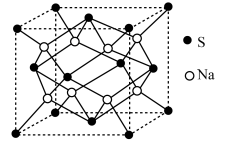
(4) S 和 Na 形成的晶体晶胞如图所示 ,该晶体的化学式为_____________ ,设晶胞的 棱长为a c m 。试计算 R 晶体的密度:_____________ (阿伏加 德罗常数的值用 NA表示 ) 。
(1) 锰的价层电子排布式为
(2) 磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子 的半径大小 :
(3)Mn 可以形成多种配合物,[Mn(CO )(H2O)2(NH3)3] Cl2• H2O中第二周期元素第一电离能大小关系为
(4) S 和 Na 形成的晶体晶胞如图所示 ,该晶体的化学式为

更新时间:2020-09-03 14:15:41
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。请回答下列问题:
(1)基态Br原子核外电子占据最高能级的轨道形状为___________ 。
(2) 的酸性
的酸性___________ (填“大于”或“小于”) 的酸性。HF、
的酸性。HF、 、
、 的熔点由大到小的顺序为
的熔点由大到小的顺序为___________ ,原因是___________ 。
(3)卤化物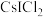 受热发生非氧化还原反应,生成一种无色晶体
受热发生非氧化还原反应,生成一种无色晶体 和一种红棕色液体
和一种红棕色液体 。解释无色晶体的熔点比红棕色液体高的原因:
。解释无色晶体的熔点比红棕色液体高的原因:___________ 。
(4) 晶胞与
晶胞与 晶胞的结构类似,其立方晶胞结构如图所示。
晶胞的结构类似,其立方晶胞结构如图所示。

① 周围最近且等距的
周围最近且等距的 数目为
数目为___________ 。
②设 为阿佛加德罗常数的值,晶体密度为
为阿佛加德罗常数的值,晶体密度为 ,则晶胞边长为
,则晶胞边长为___________ nm。
(1)基态Br原子核外电子占据最高能级的轨道形状为
(2)
 的酸性
的酸性 的酸性。HF、
的酸性。HF、 、
、 的熔点由大到小的顺序为
的熔点由大到小的顺序为(3)卤化物
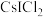 受热发生非氧化还原反应,生成一种无色晶体
受热发生非氧化还原反应,生成一种无色晶体 和一种红棕色液体
和一种红棕色液体 。解释无色晶体的熔点比红棕色液体高的原因:
。解释无色晶体的熔点比红棕色液体高的原因:(4)
 晶胞与
晶胞与 晶胞的结构类似,其立方晶胞结构如图所示。
晶胞的结构类似,其立方晶胞结构如图所示。
①
 周围最近且等距的
周围最近且等距的 数目为
数目为②设
 为阿佛加德罗常数的值,晶体密度为
为阿佛加德罗常数的值,晶体密度为 ,则晶胞边长为
,则晶胞边长为
您最近一年使用:0次
【推荐2】铜元素在化合物中其化合价可以呈现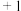 、
、 价。
价。 和
和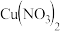 是常见的
是常见的 价铜的化合物,
价铜的化合物, 是较为常见的
是较为常见的 价铜的化合物。
价铜的化合物。
(1)铜元素位于周期表的_______ 区。属于________ 族。
(2)请写出 的电子排布式
的电子排布式__________________ ,S的价层电子排布图______________
(3)向 溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________ 。比较 和
和 中
中 中键角的大小:
中键角的大小:
___________  (填“
(填“ ” “
” “ ” 或“=”)。
” 或“=”)。
(4)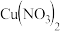 中阴离子的空间构型为
中阴离子的空间构型为_______
(5) 的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。

①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________ 。
②若以铜原子为顶点构成晶胞,面心原子为________ (Cu、Cl)
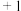 、
、 价。
价。 和
和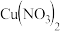 是常见的
是常见的 价铜的化合物,
价铜的化合物, 是较为常见的
是较为常见的 价铜的化合物。
价铜的化合物。(1)铜元素位于周期表的
(2)请写出
 的电子排布式
的电子排布式(3)向
 溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式 和
和 中
中 中键角的大小:
中键角的大小:
 (填“
(填“ ” “
” “ ” 或“=”)。
” 或“=”)。(4)
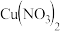 中阴离子的空间构型为
中阴离子的空间构型为(5)
 的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为
②若以铜原子为顶点构成晶胞,面心原子为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碳元素的单质有多种形式,不同单质结构不同。
(1)石墨和金刚石的结构图如下。___________ ,石墨属于___________ 晶体。
②金刚石中,碳原子杂化类型为___________ 。
③已知金刚石晶胞的棱长为acm,阿伏加德罗常数的值为NA,则金刚石晶体密度
___________ 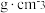 (用代数式表示)。
(用代数式表示)。
④石墨烯一定条件下,可转化为C60.某金属M与C60可制备一种低温超导材料,晶胞如图所示。M原子位于晶胞的棱上与内部,该材料的化学式为___________ 。___________ (填字母)。
b.C60熔点高于金刚石
c.一个C60分子中,σ键数目为120个
d.“纳米车”的诞生,说明人类已经可以在分子层面进行组装操作
(1)石墨和金刚石的结构图如下。

②金刚石中,碳原子杂化类型为
③已知金刚石晶胞的棱长为acm,阿伏加德罗常数的值为NA,则金刚石晶体密度

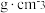 (用代数式表示)。
(用代数式表示)。④石墨烯一定条件下,可转化为C60.某金属M与C60可制备一种低温超导材料,晶胞如图所示。M原子位于晶胞的棱上与内部,该材料的化学式为


b.C60熔点高于金刚石
c.一个C60分子中,σ键数目为120个
d.“纳米车”的诞生,说明人类已经可以在分子层面进行组装操作
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素A、B、C、D、E、F、G在元素周期表中的位置如图所示,回答下列问题:

(1) 的基态原子核外电子排布式为
的基态原子核外电子排布式为___________ 。原子的第一电离能:D___________ E(填“>”或“<”)。
(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序: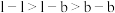 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。
(3)化合物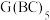 中存在的化学键类型有
中存在的化学键类型有___________ ,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为___________ 。
(4)化合物 的立体构型为
的立体构型为___________ ,其中B原子的杂化轨道类型是___________ ,写出两个与 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子___________ 。

(1)
 的基态原子核外电子排布式为
的基态原子核外电子排布式为(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序:
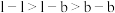 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。A. | B.接近 ,但小于 ,但小于 |
C.接近 ,但大于 ,但大于 | D.接近 ,但小于 ,但小于 |
(3)化合物
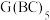 中存在的化学键类型有
中存在的化学键类型有(4)化合物
 的立体构型为
的立体构型为 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】研究人员提出利用含硫物质热化学循环实现太阳能转化与存储。过程如下:

(1)S原子最外层有_______ 种能量不同的电子,SO2为V型分子,则SO2为_______ 分子(填“极性”或“非极性”)。
(2)写出与硫同周期,有1个未成对电子的原子的电子排布式(任写两个)_______ 、_______ 。
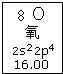
(3)氧与硫同主族,依据如图判断,说法正确的是_______。
(4)反应Ⅰ:2H2SO4(l)→2SO2(g)+2H2O(g)+O2(g)-551kJ;反应Ⅲ:S(s)+O2(g)→SO2(g)+297kJ。写出反应Ⅱ的热化学方程式_______ 。
(5)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整:
i.SO2+4I-+4H+→S↓+2H2O+2I2
ii.I2+2H2O+_______ →_______ +_______ +2I-
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)。
(6)B是A的对比实验,则a=_______ 。
(7)比较A、B、C,可得出的结论是_______ 。
(8)实验表明:SO2的歧化反应速率D>A,结合i、ii反应速率解释原因_______ 。

(1)S原子最外层有
(2)写出与硫同周期,有1个未成对电子的原子的电子排布式(任写两个)
(3)氧与硫同主族,依据如图判断,说法正确的是_______。

| A.氧元素的质量数是16 |
| B.氧元素的相对原子质量是16.00 |
| C.氧原子最外层的电子云有4种不同的伸展方向 |
| D.氧原子最外层有6个能量相同的电子 |
(5)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整:
i.SO2+4I-+4H+→S↓+2H2O+2I2
ii.I2+2H2O+
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)。
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol·L-1KI | a mol·L-1KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色成黄色,出现浑浊较A快 |
(7)比较A、B、C,可得出的结论是
(8)实验表明:SO2的歧化反应速率D>A,结合i、ii反应速率解释原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】中国科学家参与的国际阿伏加德罗组织以高纯单晶 为样品高精度地测定了
为样品高精度地测定了 。
。
Ⅰ.高纯单晶 的制备流程如下
的制备流程如下

(1)写出基态 原子的电子排布式
原子的电子排布式___________ 。
(2) 分子的空间构型是
分子的空间构型是___________ 。
(3)③中发生分解反应,判断 的分解温度
的分解温度___________ (填“大于”或“小于”) 的分解温度,理由是
的分解温度,理由是___________ 。
Ⅱ. 的测定
的测定
(4)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为apm。 以及缺陷修正值
以及缺陷修正值 (晶胞内实际原子数=理论原子数
(晶胞内实际原子数=理论原子数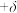 )。用上述物理量列出
)。用上述物理量列出 的计算表达式
的计算表达式___________ 。
 为样品高精度地测定了
为样品高精度地测定了 。
。Ⅰ.高纯单晶
 的制备流程如下
的制备流程如下
(1)写出基态
 原子的电子排布式
原子的电子排布式(2)
 分子的空间构型是
分子的空间构型是(3)③中发生分解反应,判断
 的分解温度
的分解温度 的分解温度,理由是
的分解温度,理由是Ⅱ.
 的测定
的测定(4)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为apm。
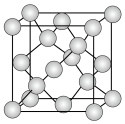
 以及缺陷修正值
以及缺陷修正值 (晶胞内实际原子数=理论原子数
(晶胞内实际原子数=理论原子数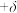 )。用上述物理量列出
)。用上述物理量列出 的计算表达式
的计算表达式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】《化学世界》刊载了我国科学家的研究成果:在钴锰氧化物 的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:
的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:________ 。
(2)中间体M分子中,碳原子的杂化类型是________ 。
(3)Co和Ni都属于第Ⅷ族元素,均能与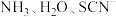 等配体组成配合物。
等配体组成配合物。
②写出与SCN-互为等电子体的一种分子_______ ,SCN-的结构式_______ ,SCN-与金属离子形成的配合物中配位原子一般是S而不是N,其原因是_______ 。
(4)CoO熔点高于MnO的原因是_______ 。
(5)KMnF3晶体有钻钛矿型的立方结构,晶胞结构如图1所示。 ,则C原子的坐标参数为
,则C原子的坐标参数为________ 。
②若阿伏加德罗常数的值为NA,晶胞参数为anm,则晶体密度为_____ g∙cm-3。
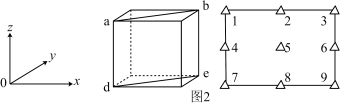
③在KMnF3晶胞结构的另一种表示中,Mn处于各顶角位置。该晶胞结构中,沿立方格子对角面取得的截图如图2所示。F在晶胞中的位置为_______ (填阿拉伯数字序号)。
 的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题:
的催化作用下,偶氮桥联二呋咱高能炸药也可作固体火箭推进剂,M是合成该推进剂的中间体,M的结构简式如图所示。回答下列问题: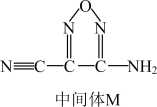
(2)中间体M分子中,碳原子的杂化类型是
(3)Co和Ni都属于第Ⅷ族元素,均能与
 等配体组成配合物。
等配体组成配合物。①一种Ni2+配离子的结构如图所示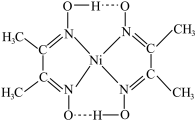 ,该配离子中存在的化学键类型有
,该配离子中存在的化学键类型有
②写出与SCN-互为等电子体的一种分子
(4)CoO熔点高于MnO的原因是
(5)KMnF3晶体有钻钛矿型的立方结构,晶胞结构如图1所示。
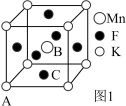
 ,则C原子的坐标参数为
,则C原子的坐标参数为②若阿伏加德罗常数的值为NA,晶胞参数为anm,则晶体密度为
③在KMnF3晶胞结构的另一种表示中,Mn处于各顶角位置。该晶胞结构中,沿立方格子对角面取得的截图如图2所示。F在晶胞中的位置为
您最近一年使用:0次
【推荐2】根据元素在体内含量的不同,可将体内元素分为常量元素和微量元素。其中H、C、O、N、S、P等为常量元素,Fe、Zn等为微量元素。回答下列问题:
(1)基态Fe原子的核外电子排布式为[Ar]_______ ,有_______ 组相同能量的电子。
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是___________ 。
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
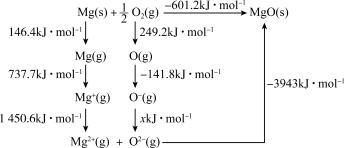
由图可知,Mg原子的第一电离能为___________ kJ·mol-1;O=O键键能为___________ kJ·mol-1;氧原子的第二电子亲和能为___________ kJ·mol-1。
(1)基态Fe原子的核外电子排布式为[Ar]
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
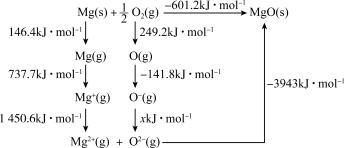
由图可知,Mg原子的第一电离能为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。镉Cd在周期表中位于第五周期与Zn同族,则Cd的价电子排布式为:_______ ,第一电离能:Ga_______ As(填“大于”或“小于 ”或“等于”);H2S分子的VSEPR模型为_______ 。
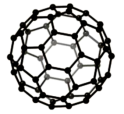
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图所示,分子中碳原子轨道的杂化类型为_______ ;1个C60分子中σ键的数目为_______ 个。
(3)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。NF3的沸点比NH3_______ (填“高”或“低”),原因是_______ 。
(1)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。镉Cd在周期表中位于第五周期与Zn同族,则Cd的价电子排布式为:
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图所示,分子中碳原子轨道的杂化类型为

(3)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。NF3的沸点比NH3
您最近一年使用:0次
【推荐1】LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如下:
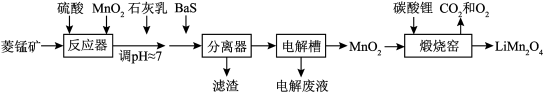
已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为___________ 。
(2)加入MnO2的作用是___________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=___________ mol·L-1;用石灰乳调节至pH≈7,除去的金属离子是___________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有NiS和___________ 。
(5)在电解槽中,发生电解反应的离子方程式为___________ 。随着电解反应进行,为保持电解液成分稳定,应不断___________ 。电解废液可在反应器中循环利用。
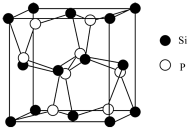
(6)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________ ,该化合物的化学式为___________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有NiS和
(5)在电解槽中,发生电解反应的离子方程式为
(6)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】资源化利用碳及其化合物具有重要意义。
(1)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
Ⅰ.

Ⅱ.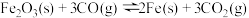
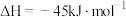
Ⅲ.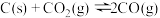
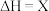 试计算,
试计算,
_______ ;
反应Ⅱ中,正反应的活化能_______ (填“>”、“<”或“=”)逆反应的活化能。
(2)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1molCO2与足量的碳发生反应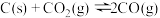 ,平衡时体系中气体体积分数与温度关系如图所示。
,平衡时体系中气体体积分数与温度关系如图所示。
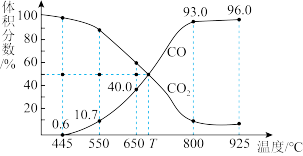
①650℃时,反应达平衡后CO2的转化率为_______ ;
②T℃时,在1L恒容密闭容器中加入3molCO2与足量的碳,10min后测得V(CO)为11.2L(标况下),则反应速率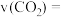
_______ ;上述反应达到平衡状态时,下列说法正确的是_______ :
a.单位时间内生成的CO2的物质的量是CO的两倍
b.容器中气体的压强不随时间而变化
c.升高温度,再次达到平衡时,C的质量减少
d.保持其它条件不变,充入惰性气体,反应速率减小,平衡移动
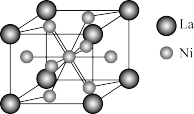
(3)镍及其化合物在工业生产和科研领域有重要的用途。请回答下列问题:
基态Ni原子价层电子的电子排布图(轨道表达式)为_______ 。金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。若阿伏加德罗常数的值为 ,晶胞边长为apm,则该晶胞的密度为
,晶胞边长为apm,则该晶胞的密度为_______  。(
。( )
)
(1)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
Ⅰ.


Ⅱ.
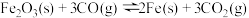
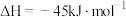
Ⅲ.
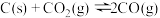
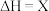 试计算,
试计算,
反应Ⅱ中,正反应的活化能
(2)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1molCO2与足量的碳发生反应
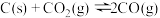 ,平衡时体系中气体体积分数与温度关系如图所示。
,平衡时体系中气体体积分数与温度关系如图所示。
①650℃时,反应达平衡后CO2的转化率为
②T℃时,在1L恒容密闭容器中加入3molCO2与足量的碳,10min后测得V(CO)为11.2L(标况下),则反应速率
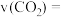
a.单位时间内生成的CO2的物质的量是CO的两倍
b.容器中气体的压强不随时间而变化
c.升高温度,再次达到平衡时,C的质量减少
d.保持其它条件不变,充入惰性气体,反应速率减小,平衡移动
(3)镍及其化合物在工业生产和科研领域有重要的用途。请回答下列问题:
基态Ni原子价层电子的电子排布图(轨道表达式)为
 ,晶胞边长为apm,则该晶胞的密度为
,晶胞边长为apm,则该晶胞的密度为 。(
。( )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_______ ,Li原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(2)As 的卤化物的熔点如下:
表中卤化物熔点差异的原因是_______ ,AsCl3分子的立体构型为_______ 。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是_______ g/cm3(用含a、NA的式子表示)。
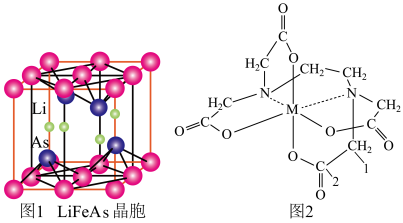
(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______ 个σ键,2号碳原子采取_______ 杂化方式;Fe3+与氮原子之间形成的化学键是_______ ,Fe3+的配位数为_______ ;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_______ 。
(1)Fe原子的核外电子排布式为[Ar]
(2)As 的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是

(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有
您最近一年使用:0次



