二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(1)方法一的离子方程式是_______ ;氧化产物是______ (填化学式);
(2)方法二中被还原的物质是____ ,若反应中产生的ClO2气体在标准状况下的体积为2.24L,则电子转移数为____ NA。
(3)现在许多城市自来水仍采用氯气消毒,则用该自来水不易配置下列试剂的是______ 。
A.硝酸银溶液 B.食盐溶液 C.碘化钾溶液 D.氯化铁溶液
用离子方程式表示不易配置原因_____ (只需写出一个)。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与 的物质的量之比为1:1,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比为
的物质的量之比为1:1,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比为___ 。
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(1)方法一的离子方程式是
(2)方法二中被还原的物质是
(3)现在许多城市自来水仍采用氯气消毒,则用该自来水不易配置下列试剂的是
A.硝酸银溶液 B.食盐溶液 C.碘化钾溶液 D.氯化铁溶液
用离子方程式表示不易配置原因
(4)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与
 的物质的量之比为1:1,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比为
的物质的量之比为1:1,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比为
更新时间:2020-09-08 08:11:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为___________ 。
(2)含等物质的量的 和
和 的溶液物料守恒式为
的溶液物料守恒式为___________ 。
(3)向2 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:___________ 。
(4)向 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知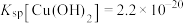 ,则溶液中
,则溶液中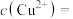
______  。
。
(5)某溶液只含 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入_________ ,然后再加入________ ,调节pH范围为_______ 。
(1)泡沫灭火剂包括
 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为(2)含等物质的量的
 和
和 的溶液物料守恒式为
的溶液物料守恒式为(3)向2
 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:(4)向
 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知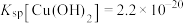 ,则溶液中
,则溶液中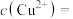
 。
。(5)某溶液只含
 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入| 金属离子 |  |  |  | |
 | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列方程式
(1)磁性氧化铁与足量的稀硝酸反应的离子方程式:________
(2)铜与硫共热的化学方程式:_________
(3)二氧化氮通入水中的化学方程式:________
(4)氨的催化氧化的化学方程式:___________
(5)往Ba(OH)2溶液中滴加NaHSO4溶液使溶液呈中性的离子方程式:________
(1)磁性氧化铁与足量的稀硝酸反应的离子方程式:
(2)铜与硫共热的化学方程式:
(3)二氧化氮通入水中的化学方程式:
(4)氨的催化氧化的化学方程式:
(5)往Ba(OH)2溶液中滴加NaHSO4溶液使溶液呈中性的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
Ⅰ.单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时可以生成盐,某同学构建了如图所示的知识网络图。
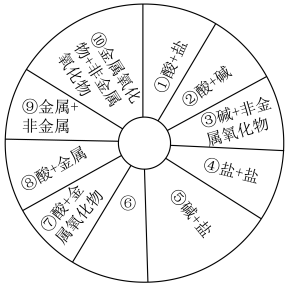
(1)请写一种符合图中组合⑥关系的化学方程式(要求组合⑥不能与图中已有组合重复,为四大基本反应类型)___________ 。
(2) 可看成由
可看成由 和FeO组成,请写出
和FeO组成,请写出 与盐酸反应的离子方程式:
与盐酸反应的离子方程式:___________ 。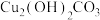 可看成由
可看成由 和
和 组成,请写出
组成,请写出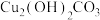 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:___________ 。
(3)一种阳离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙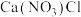 ;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如
;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如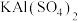 ,据此下列各化合物中属于混盐的是
,据此下列各化合物中属于混盐的是___________ (填序号,下同),属于复盐的是___________ 。
A. B.
B.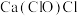
C. D.
D.
Ⅱ.铁是人类较早使用的金属之一,回答下列问题。
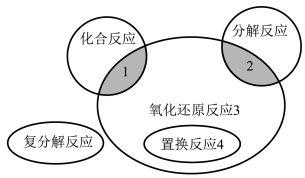
(4)氧化还原反应与四大基本反应类型的关系如图所示,请写出一个属于区域3的有铁单质生成的化学方程式:___________ 。
(5)已知氧化性: ,若向
,若向 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
(6)水热法制备直径为1-100nm的颗粒Y(化合物),反应原理为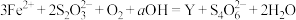 ,下列说法中正确的___________。
,下列说法中正确的___________。
(7) 主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾(
主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
Ⅰ.单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时可以生成盐,某同学构建了如图所示的知识网络图。

(1)请写一种符合图中组合⑥关系的化学方程式(要求组合⑥不能与图中已有组合重复,为四大基本反应类型)
(2)
 可看成由
可看成由 和FeO组成,请写出
和FeO组成,请写出 与盐酸反应的离子方程式:
与盐酸反应的离子方程式: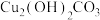 可看成由
可看成由 和
和 组成,请写出
组成,请写出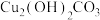 与盐酸反应的化学方程式:
与盐酸反应的化学方程式:(3)一种阳离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙
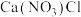 ;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如
;而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如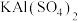 ,据此下列各化合物中属于混盐的是
,据此下列各化合物中属于混盐的是A.
 B.
B.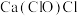
C.
 D.
D.
Ⅱ.铁是人类较早使用的金属之一,回答下列问题。
(4)氧化还原反应与四大基本反应类型的关系如图所示,请写出一个属于区域3的有铁单质生成的化学方程式:

(5)已知氧化性:
 ,若向
,若向 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列说法中正确的是___________。| A.固体中一定有铜 | B.固体中一定有铁 |
C.溶液中一定有 | D.溶液中一定有 |
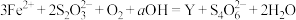 ,下列说法中正确的___________。
,下列说法中正确的___________。A. |
B. 、 、 都发生还原反应 都发生还原反应 |
| C.将Y均匀分散到水中形成的体系具有丁达尔效应 |
D.每有3个 参加反应,反应中转移电子总数目为6个 参加反应,反应中转移电子总数目为6个 |
 主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾(
主要用于饮用水消毒净化、城市生活污水和工业污水处理。湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】双氧水、84消毒液、高铁酸钠是生活中常用的消毒剂,请回答下列问题:
(1)某同学设计如表实验研究H2O2的性质
已知:I2遇淀粉溶液变蓝
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明H2O2具有氧化性的实验是________ (填序号“i”或“ii”)。
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO________ O2(填“>”或“<”)。
②当有3个氧气分子生成时,转移________ 个电子。
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是________ 。
②用双线桥法标出该反应电子转移的方向和数目______ 。
(1)某同学设计如表实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| i | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
①从化合价改变上看H2O2,既有氧化性又有还原性,具有还原性的原因是
②能证明H2O2具有氧化性的实验是
(2)2016年巴西奥运会期间,由于工作人员将84消毒液(有效成分为NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
已知:NaClO具有强氧化性,易被还原为NaCl
①该反应说明氧化性:NaClO
②当有3个氧气分子生成时,转移
(3)湿法制备Na2FeO4,反应为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O。
①该反应的氧化产物是
②用双线桥法标出该反应电子转移的方向和数目
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)铁钉在氯气中被锈蚀为棕褐色物质FeCl3,而在盐酸中生成浅绿色的FeCl2溶液。在Cl2、Cl-、H+中,具有氧化性的是____________ ,其中氧化性最强的是____________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑____________________ ;
②NaOH+HCl===NaCl+H2O__________________ ;
③2HCl H2↑+Cl2↑
H2↑+Cl2↑________________________ 。
(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、 中,
中,__________________ 氧化性最强。
(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是________________ 。若消耗15.8 g氧化剂,则被氧化的还原剂的质量是______________ g。HBr的作用是____________________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑
②NaOH+HCl===NaCl+H2O
③2HCl
 H2↑+Cl2↑
H2↑+Cl2↑(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、
 中,
中,(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.已知2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
(1)氧化剂与还原剂的物质的量之比是_________ ,HCl在反应中表现的性质有____________ 。
(2)单线桥标明该反应电子转移方向和数目:________________________ 。
(3)写出以软锰矿为原料制备Cl2的化学方程式___________________ 。
Ⅱ.(1)VLFe2(SO4)3溶液中含Fe3+ag,则该溶液中溶质的物质的量浓度为______________ 。
(2)为了供学生课外活动,要求把SO42-、CO32-、H+、OH-、NH4+、Fe3+、Na+七种离子根据共存原理分为两组混合溶液,分配结果是:
第一组:_______________ ;第二组:______________________ 。
(1)氧化剂与还原剂的物质的量之比是
(2)单线桥标明该反应电子转移方向和数目:
(3)写出以软锰矿为原料制备Cl2的化学方程式
Ⅱ.(1)VLFe2(SO4)3溶液中含Fe3+ag,则该溶液中溶质的物质的量浓度为
(2)为了供学生课外活动,要求把SO42-、CO32-、H+、OH-、NH4+、Fe3+、Na+七种离子根据共存原理分为两组混合溶液,分配结果是:
第一组:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】在酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+)。请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式___________ ;
(2)在酸性条件下(足量),各取1 L浓度为1 mol·L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3)∶n(H2O2)∶n(FeCl3)∶n(K2Cr2O7)=____________ 。
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式
(2)在酸性条件下(足量),各取1 L浓度为1 mol·L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3)∶n(H2O2)∶n(FeCl3)∶n(K2Cr2O7)=
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为
和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为 
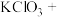
 HCl(浓)→
HCl(浓)→ KCl+
KCl+
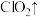 +
+
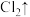 +
+

(1)请配平该化学方程式_______ (未知系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是_______ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)若改变温度至70℃,发现 和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:
和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:_______ 。
 和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为
和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为 
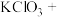
 HCl(浓)→
HCl(浓)→ KCl+
KCl+
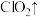 +
+
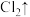 +
+

(1)请配平该化学方程式
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)该反应中氧化剂与还原剂的物质的量之比为
(4)若改变温度至70℃,发现
 和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:
和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)下列物质能导电的是___________ ,属于电解质的是___________ ,属于非电解质的是___________ 。
①NaCl晶体,②液态 ,③液态醋酸,④铜,⑤
,③液态醋酸,④铜,⑤ 固体,⑥蔗糖(
固体,⑥蔗糖(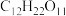 ),⑦氨水。
),⑦氨水。
(2) 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
①请配平上述化学方程式:___________ ;
②浓盐酸在反应中显示出来的性质是___________ (填编号)
A.还原性 B.酸性 C.氧化性
③氧化剂是___________ ,氧化产物是___________ ;
④每产生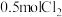 ,则转移的电子的物质的量为
,则转移的电子的物质的量为___________ mol。
(1)下列物质能导电的是
①NaCl晶体,②液态
 ,③液态醋酸,④铜,⑤
,③液态醋酸,④铜,⑤ 固体,⑥蔗糖(
固体,⑥蔗糖(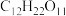 ),⑦氨水。
),⑦氨水。(2)
 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
①请配平上述化学方程式:
②浓盐酸在反应中显示出来的性质是
A.还原性 B.酸性 C.氧化性
③氧化剂是
④每产生
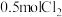 ,则转移的电子的物质的量为
,则转移的电子的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】反应孕育着能量和物质变化,有些反应风驰电掣,流光溢彩,体现了化学之美。
(1)氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。若化学计量数b=3,d=4,则c=_______ 。
(2)将含lmol的H2O2溶液和含0.2molKMnO4的酸性溶液混合,紫色褪去,产生气泡。
①该气体是_______ 。
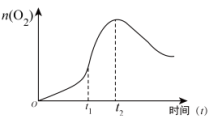
②产生气泡的速率与时间关系如图所示:推测t1~t2产生气泡的速率加快的原因_______ (只答一条即可);最终共产生气体_______ mol。
(3)在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有表中的若干种离子:
取该溶液100mL进行如表实验(气体体积在标准状况下测定):
将一定含有的离子及其物质的量浓度填入表中。
(4)已知固体Na2SO3受热易分解。实验流程和结果如图:
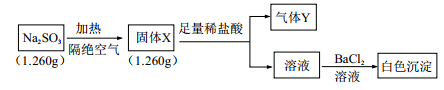
气体Y是一种纯净物,在标准状况下的密度为1.518g•L-1,请回答:
①气体Y分子式_______ ,白色沉淀的化学式_______ 。
②该流程中Na2SO3受热分解的化学方程式_______ 。
(1)氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。若化学计量数b=3,d=4,则c=
(2)将含lmol的H2O2溶液和含0.2molKMnO4的酸性溶液混合,紫色褪去,产生气泡。
①该气体是
②产生气泡的速率与时间关系如图所示:推测t1~t2产生气泡的速率加快的原因

(3)在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有表中的若干种离子:
| 阳离子 | K+、Ag+、Ba2+ |
| 阴离子 | CO 、SiO 、SiO 、SO 、SO |
| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| II | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称重得固体质量 | 固体质量为2.4g |
| III | 在II的溶液中滴加BaCl2溶液 | 无明显现象 |
| 一定含有的离子 | Na+ | |||
| c/(mol•L-1) | 0.5 |

气体Y是一种纯净物,在标准状况下的密度为1.518g•L-1,请回答:
①气体Y分子式
②该流程中Na2SO3受热分解的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用。硫酸的性质有:A.高沸点;B.强酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
①硫酸可用作气体干燥剂___________ ;
②往晶体硫酸铜中加液硫酸,晶体变白___________ ;
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑___________ ;
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生___________ ;
⑤浓硫酸与FeO反应____________ ;
⑥运用铁制槽车和铝制槽车送输浓硫酸___________ 。
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
___ C1O2-+__NO+____=Cl-+____NO3-+______。
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:_____________________ 。
①硫酸可用作气体干燥剂
②往晶体硫酸铜中加液硫酸,晶体变白
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生
⑤浓硫酸与FeO反应
⑥运用铁制槽车和铝制槽车送输浓硫酸
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】含氮化合物的处理对环境保护意义重大。
(1)用H2或CO催化还原NO均能达到消除污染的目的,反应的还原产物为_______ 。
(2)实验室常用NaOH溶液吸收NOx(NO和NO2的混合气体),反应的化学方程式如下:(已知NO不能与NaOH溶液反应,不考虑NO2与N2O4的转化)
NO+NO2+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
①若NOx能被NaOH溶液完全吸收,则x的取值范围为_______ 。
②若用100mL5mol/LNaOH吸收NOx,NaOH恰好完全反应,则被吸收的NOx的体积为_______ (标准状况)。
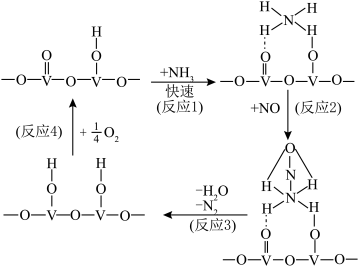
(3)用V2O5作催化剂,NH3将NO还原成N2的一种反应历程如图所示,则总反应方程式为_______ 。
(4)一种将氨氮( )废水中的氮元素转变为N2脱除的机理如图:
)废水中的氮元素转变为N2脱除的机理如图:

已知:氧气浓度越高,厌氧氨氧化菌活性越低。
①参与I中反应的n( )∶n(O2)=
)∶n(O2)=_______ 。
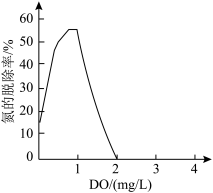
②废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当1mg/L<DO<2mg/L时,随着DO的增大氮的脱除率下降,其原因可能是_______ 。
(1)用H2或CO催化还原NO均能达到消除污染的目的,反应的还原产物为
(2)实验室常用NaOH溶液吸收NOx(NO和NO2的混合气体),反应的化学方程式如下:(已知NO不能与NaOH溶液反应,不考虑NO2与N2O4的转化)
NO+NO2+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
①若NOx能被NaOH溶液完全吸收,则x的取值范围为
②若用100mL5mol/LNaOH吸收NOx,NaOH恰好完全反应,则被吸收的NOx的体积为
(3)用V2O5作催化剂,NH3将NO还原成N2的一种反应历程如图所示,则总反应方程式为

(4)一种将氨氮(
 )废水中的氮元素转变为N2脱除的机理如图:
)废水中的氮元素转变为N2脱除的机理如图:
已知:氧气浓度越高,厌氧氨氧化菌活性越低。
①参与I中反应的n(
 )∶n(O2)=
)∶n(O2)=②废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当1mg/L<DO<2mg/L时,随着DO的增大氮的脱除率下降,其原因可能是

您最近半年使用:0次



