含氮化合物的处理对环境保护意义重大。
(1)用H2或CO催化还原NO均能达到消除污染的目的,反应的还原产物为_______ 。
(2)实验室常用NaOH溶液吸收NOx(NO和NO2的混合气体),反应的化学方程式如下:(已知NO不能与NaOH溶液反应,不考虑NO2与N2O4的转化)
NO+NO2+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
①若NOx能被NaOH溶液完全吸收,则x的取值范围为_______ 。
②若用100mL5mol/LNaOH吸收NOx,NaOH恰好完全反应,则被吸收的NOx的体积为_______ (标准状况)。
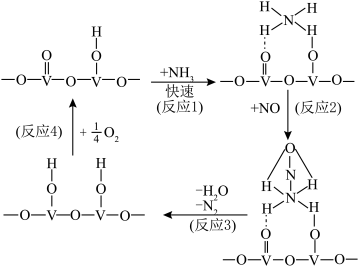
(3)用V2O5作催化剂,NH3将NO还原成N2的一种反应历程如图所示,则总反应方程式为_______ 。 )废水中的氮元素转变为N2脱除的机理如图:
)废水中的氮元素转变为N2脱除的机理如图:

已知:氧气浓度越高,厌氧氨氧化菌活性越低。
①参与I中反应的n( )∶n(O2)=
)∶n(O2)=_______ 。
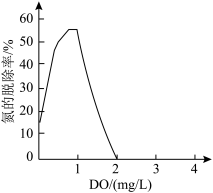
②废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当1mg/L<DO<2mg/L时,随着DO的增大氮的脱除率下降,其原因可能是_______ 。
(1)用H2或CO催化还原NO均能达到消除污染的目的,反应的还原产物为
(2)实验室常用NaOH溶液吸收NOx(NO和NO2的混合气体),反应的化学方程式如下:(已知NO不能与NaOH溶液反应,不考虑NO2与N2O4的转化)
NO+NO2+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
①若NOx能被NaOH溶液完全吸收,则x的取值范围为
②若用100mL5mol/LNaOH吸收NOx,NaOH恰好完全反应,则被吸收的NOx的体积为
(3)用V2O5作催化剂,NH3将NO还原成N2的一种反应历程如图所示,则总反应方程式为
 )废水中的氮元素转变为N2脱除的机理如图:
)废水中的氮元素转变为N2脱除的机理如图:
已知:氧气浓度越高,厌氧氨氧化菌活性越低。
①参与I中反应的n(
 )∶n(O2)=
)∶n(O2)=②废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当1mg/L<DO<2mg/L时,随着DO的增大氮的脱除率下降,其原因可能是
更新时间:2023-04-29 09:57:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列变化中,涉及氧化还原反应的是_______ (填序号)。
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为 ,该反应所属基本反应类型是
,该反应所属基本反应类型是_______ (填4种基本反应类型中的一种),在反应中铁元素的化合价_______ (填“升高”或“降低”),该元素的原子_______ (填“失去”或“得到”)电子。该反应还原剂是_______ (填化学式,下同),氧化剂是_______ 。
(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作_______ 剂(填“氧化”或“还原”)。
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具_______ 性。(填“氧化”或“还原”)
(1)下列变化中,涉及氧化还原反应的是
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为
 ,该反应所属基本反应类型是
,该反应所属基本反应类型是(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具
您最近半年使用:0次
【推荐2】I.对于反应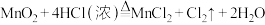 。
。
(1) 在反应中
在反应中___________ 电子,发生___________ 反应。
(2) 在反应中
在反应中___________ 电子,发生___________ 反应。
(3)用单线桥法标出该反应中电子转移的方向和数目:___________ 。
II. 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: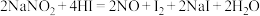 。
。
(4)反应中___________ 发生氧化反应(填化学式),___________ 是氧化剂(填化学式);
(5)用双线桥标出电子转移方向和数目:___________ 。
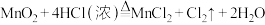 。
。(1)
 在反应中
在反应中(2)
 在反应中
在反应中(3)用单线桥法标出该反应中电子转移的方向和数目:
II.
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: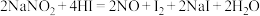 。
。(4)反应中
(5)用双线桥标出电子转移方向和数目:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】以黄铜矿[主要成分是二硫化亚铁铜( )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
Ⅰ.火法炼铜: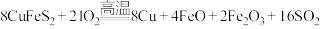
(1)反应中被还原的元素是_______ (填元素符号),氧化产物有_______ (填化学式)。
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为_______ ,冶炼过程中产生大量 ,下列处理方案中合理的是
,下列处理方案中合理的是_______ (填字母)。
A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(3)配平该反应方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______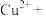 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是_______ 。
 )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。Ⅰ.火法炼铜:
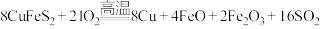
(1)反应中被还原的元素是
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为
 ,下列处理方案中合理的是
,下列处理方案中合理的是A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(3)配平该反应方程式:
_______
 _______
_______ _______
_______ _______
_______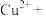 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
完成下列填空:
(1)上述反应中的还原剂为___ ,还原产物有___ ,当有1molKNO3参加反应时,转移电子的数目为___ 。
(2)KNO3晶体类型是___ ,其晶体中存在的化学键有___ 。
(3)硫原子的核外电子排布式为___ ,原子核外有___ 种不同能量的电子。将SO2和Cl2分别通入品红溶液中,产生的现象是___ ;若将SO2和Cl2等体积混合后再缓缓通入品红溶液,发现品红溶液___ ,其原因是___ 。
(4)S、C和N三种元素的原子半径从小到大的顺序是___ ;K2S溶液中除OH-外其它各离子物质的量浓度的大小顺序为___ 。
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___ 。
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
 K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑完成下列填空:
(1)上述反应中的还原剂为
(2)KNO3晶体类型是
(3)硫原子的核外电子排布式为
(4)S、C和N三种元素的原子半径从小到大的顺序是
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯及其化合物在生产、生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式:_______ 。
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化_______ molHCl。
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ ;用双线桥表示该反应电子转移的方向和数目:_______ 。
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:_______ (用离子方程式表示,已知酸性:H2CO3>HClO> )。
)。
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:_______ 。
(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的_______ 倍(保留两位小数)。
(1)①写出实验室中制取氯气的离子方程式:
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:
 )。
)。②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与
 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ca(NO2)2(亚硝酸钙)是易溶于水的无色晶体,可用作混凝土中钢筋的防护剂。
(1)Ca(NO2)2的制备方法很多。
①实验室可用反应Ca(NO3)2+2CaFe2O4+4NO 3Ca(NO2)2+2Fe2O3制备Ca(NO2)2,该反应中被氧化的N原子与被还原的N原子的物质的量之比为
3Ca(NO2)2+2Fe2O3制备Ca(NO2)2,该反应中被氧化的N原子与被还原的N原子的物质的量之比为_____ 。
②用石灰乳吸收硝酸工业尾气中氮氧化物制备Ca(NO2)2,其中NO2与Ca(OH)2反应生成Ca(NO2)2和Ca(NO3)2的化学方程式为_____ ,经过滤得到含Ca(NO2)2的溶液为液态产品。
(2)测定某液态产品中NO3-含量的步骤如下:

已知:步骤4中的反应为NO3—+3Fe2++4H+=3Fe3++NO↑+2H2O,
步骤5中的反应为6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O。
若步骤5滴定至终点时消耗K2Cr2O7溶液20.00mL,计算液态产品中NO3-的含量(单位g·L-1,最后结果保留一位小数,写出计算过程)___________ 。
(1)Ca(NO2)2的制备方法很多。
①实验室可用反应Ca(NO3)2+2CaFe2O4+4NO
 3Ca(NO2)2+2Fe2O3制备Ca(NO2)2,该反应中被氧化的N原子与被还原的N原子的物质的量之比为
3Ca(NO2)2+2Fe2O3制备Ca(NO2)2,该反应中被氧化的N原子与被还原的N原子的物质的量之比为②用石灰乳吸收硝酸工业尾气中氮氧化物制备Ca(NO2)2,其中NO2与Ca(OH)2反应生成Ca(NO2)2和Ca(NO3)2的化学方程式为
(2)测定某液态产品中NO3-含量的步骤如下:

已知:步骤4中的反应为NO3—+3Fe2++4H+=3Fe3++NO↑+2H2O,
步骤5中的反应为6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O。
若步骤5滴定至终点时消耗K2Cr2O7溶液20.00mL,计算液态产品中NO3-的含量(单位g·L-1,最后结果保留一位小数,写出计算过程)
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】目前,能较稳定存在的氯的氧化物有 、
、 、
、 等。有关数据见表:请回答下列问题:
等。有关数据见表:请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是_______ 。
(2) 属于酸性氧化物,它与水反应的离子方程式为
属于酸性氧化物,它与水反应的离子方程式为_______ 。
(3) 是一种常用的消毒剂,我国从2000年起逐步用
是一种常用的消毒剂,我国从2000年起逐步用 代替氯气对饮用水进行消毒。在消毒水时,
代替氯气对饮用水进行消毒。在消毒水时, 还可将水中的
还可将水中的 、
、 等转化成
等转化成 和
和 等难溶物除去,说明
等难溶物除去,说明 具有
具有_______ 性,试写出用 (
( 反应后的产物为
反应后的产物为 )氧化除去
)氧化除去 生成
生成 的离子方程式:
的离子方程式:_______ 。
(4)工业上可以用下列反应制备 :
: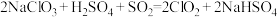 ,请用单线桥法表示出该反应电子转移的方向和数目
,请用单线桥法表示出该反应电子转移的方向和数目_______ 。
(5)工业上也可以用制备 的反应原理为:
的反应原理为: (浓)
(浓)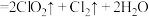
 。
。
①浓盐酸在反应中显示出来的性质是_______ (填序号)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生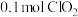 ,则转移的电子数为
,则转移的电子数为_______ 。
 、
、 、
、 等。有关数据见表:请回答下列问题:
等。有关数据见表:请回答下列问题:| 化学式 |  |  |  |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
(1)常温、常压下,三种氧化物中属于气体的是
(2)
 属于酸性氧化物,它与水反应的离子方程式为
属于酸性氧化物,它与水反应的离子方程式为(3)
 是一种常用的消毒剂,我国从2000年起逐步用
是一种常用的消毒剂,我国从2000年起逐步用 代替氯气对饮用水进行消毒。在消毒水时,
代替氯气对饮用水进行消毒。在消毒水时, 还可将水中的
还可将水中的 、
、 等转化成
等转化成 和
和 等难溶物除去,说明
等难溶物除去,说明 具有
具有 (
( 反应后的产物为
反应后的产物为 )氧化除去
)氧化除去 生成
生成 的离子方程式:
的离子方程式:(4)工业上可以用下列反应制备
 :
: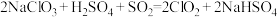 ,请用单线桥法表示出该反应电子转移的方向和数目
,请用单线桥法表示出该反应电子转移的方向和数目(5)工业上也可以用制备
 的反应原理为:
的反应原理为: (浓)
(浓)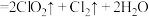
 。
。①浓盐酸在反应中显示出来的性质是
A.还原性 B.氧化性 C.酸性
②若上述反应中产生
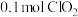 ,则转移的电子数为
,则转移的电子数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(2)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①发生反应的离子方程式为___________ 。
②为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为_________
③欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要___________ (选填字母)。
(3)纳米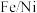 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:

①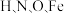 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是___________ 。
②反应ⅱ的离子方程式为___________ 。
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为___________ 。
(4)在 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。
已知:
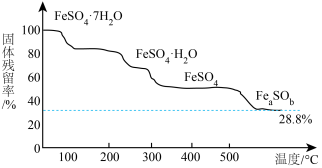
通过计算后,写出 受热分解的化学方程式
受热分解的化学方程式___________ 。
(1)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(2)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①发生反应的离子方程式为
②为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为③欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要
溶液循环利用,现有下列试剂:a.浓硝酸B.铁粉C.氯气D.烧碱E.浓氨水,需要用到的试剂除盐酸外还需要(3)纳米
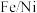 复合材料,可有效去除酸性废水中的
复合材料,可有效去除酸性废水中的 ,其反应过程(
,其反应过程( 不参与反应)如图所示:
不参与反应)如图所示:
①
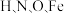 四种元素的电负性从大到小的顺序是
四种元素的电负性从大到小的顺序是②反应ⅱ的离子方程式为
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为
(4)在
 气氛中,
气氛中, 的热分解过程如图所示。
的热分解过程如图所示。已知:


通过计算后,写出
 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】完成以下反应的填空。
(1)我国的铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出。氧化浸出法是主要方法之一,氧化浸出法即是在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成,该反应的离子方程式为
生成,该反应的离子方程式为__________ 。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
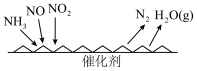
当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应。该反应的化学方程式为_____________ 。
(1)我国的铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出。氧化浸出法是主要方法之一,氧化浸出法即是在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成,该反应的离子方程式为
生成,该反应的离子方程式为(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应。该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)写出氨气发生催化氧化反应的方程式______________ 。
(2)用一支试管收集干燥的 NO 气体 13mL,间歇而又缓慢地通入 8mL 的 O2,按图进行实验,下列是最终状态的描述:①试管内气体呈棕色 ②试管内气体呈无色③试管内液面上升 ④试管内液面不变 ⑤试管内气体是 NO ⑥试管内气体是 O2,其中描述正确的是:_________________ 。

(3)如果将一支试管中充入 20mLNO2 和 O2 的混合气体,倒扣在水槽中,待反应停止后,试管内剩余 5mL 无色气体。若剩余气体为 NO,则原混合气体中:V(NO2)=_______ mL;V(O2)=__________ mL。
(2)用一支试管收集干燥的 NO 气体 13mL,间歇而又缓慢地通入 8mL 的 O2,按图进行实验,下列是最终状态的描述:①试管内气体呈棕色 ②试管内气体呈无色③试管内液面上升 ④试管内液面不变 ⑤试管内气体是 NO ⑥试管内气体是 O2,其中描述正确的是:

(3)如果将一支试管中充入 20mLNO2 和 O2 的混合气体,倒扣在水槽中,待反应停止后,试管内剩余 5mL 无色气体。若剩余气体为 NO,则原混合气体中:V(NO2)=
您最近半年使用:0次
填空题
|
适中
(0.65)
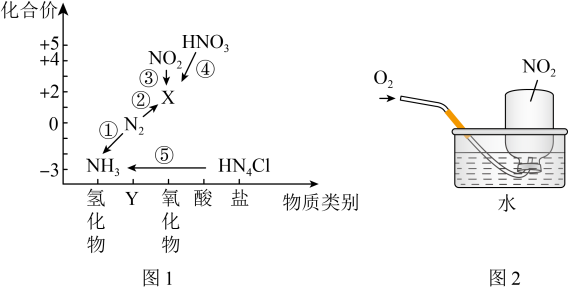
【推荐2】氮元素是高中化学学习的一种重要非金属元素,其价类二维图如图1所示。________ ,反应①~⑤中不属于氧化还原反应的是________ (填序号)。
(2)反应①中每消耗1mol氢气,转移电子________ mol。
(3)除去X中混有的少量 的方法是
的方法是________ 。
(4)工业以氨气为原料制备硝酸的第一步反应为氨的催化氧化,写出该反应的化学方程式________ 。
(5)用集气瓶收集 气体并倒置在水槽中,然后缓慢通入适量
气体并倒置在水槽中,然后缓慢通入适量 ,如图2所示。一段时间后,集气瓶中充满溶液。
,如图2所示。一段时间后,集气瓶中充满溶液。
①写出该过程总反应的化学方程式________ 。该实验对工业上生产硝酸的启示是________ 。
②假设该实验条件下,气体摩尔体积为 ,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为________ mol/L。
(2)反应①中每消耗1mol氢气,转移电子
(3)除去X中混有的少量
 的方法是
的方法是(4)工业以氨气为原料制备硝酸的第一步反应为氨的催化氧化,写出该反应的化学方程式
(5)用集气瓶收集
 气体并倒置在水槽中,然后缓慢通入适量
气体并倒置在水槽中,然后缓慢通入适量 ,如图2所示。一段时间后,集气瓶中充满溶液。
,如图2所示。一段时间后,集气瓶中充满溶液。①写出该过程总反应的化学方程式
②假设该实验条件下,气体摩尔体积为
 ,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
,瓶内液体不扩散,则集气瓶中溶液的物质的量浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】以NO和NO2为主的氮氧化物是造成光化学烟雾、雾霾和酸雨的一个重要原因。
I.为防止氮的氧化物(NO、NO2)污染空气,可用活性炭或一氧化碳还原氮氧化物。
(1)在一定条件下,CO与NO反应生成CO2和N2,反应的化学方程式: 。为提高此反应的速率,下列措施不可行的是___________(填标号)。
。为提高此反应的速率,下列措施不可行的是___________(填标号)。
(2)恒温条件下,向2L恒容密闭容器中加入活性炭(足量)和1.0molNO,发生反应: 。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=
。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=___________ mol·L-1·min-1。
II.氨气在一定条件下也可以还原氮氧化物,其反应为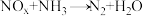 (未配平)。
(未配平)。
(3)下列有关NH3的说法中,错误的是___________ (填标号)。
A.工业合成NH3需要在高温、高压、催化剂下进行
B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥
(4)硝酸工业排放的废气中常含有NO、NO2等,为消除它们对环境的破坏作用,工业上可采用氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ ;若用通式NOx表示氮氧化物,则每摩尔氨可将___________ mol的NOx转化为N2。
III.工业上也常用Na2CO3溶液吸收法处理氮氧化物(NOX)。
已知:①NO不能与Na2CO3溶液反应。
② ;
;
(5)①当NOx被Na2CO3溶液完全吸收时,x的值不可能是___________ (填标号)。
A.1.3 B.1.6 C.1.8 D.2.0
②若用溶质质量分数为21.2%的Na2CO3溶液完全吸收1molNOx,则需要Na2CO3溶液至少______ g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液的质量就增加44g,则NOx中的x值为___________ 。
(6)氨转化法和Na2CO3溶液吸收法处理NOx尾气共同的优点是___________ 。
I.为防止氮的氧化物(NO、NO2)污染空气,可用活性炭或一氧化碳还原氮氧化物。
(1)在一定条件下,CO与NO反应生成CO2和N2,反应的化学方程式:
 。为提高此反应的速率,下列措施不可行的是___________(填标号)。
。为提高此反应的速率,下列措施不可行的是___________(填标号)。| A.及时转移出CO2 |
| B.使用合适的催化剂 |
| C.升高温度 |
| D.恒温恒容条件下,通入稀有气体增大压强 |
 。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=
。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=II.氨气在一定条件下也可以还原氮氧化物,其反应为
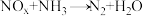 (未配平)。
(未配平)。(3)下列有关NH3的说法中,错误的是
A.工业合成NH3需要在高温、高压、催化剂下进行
B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥
(4)硝酸工业排放的废气中常含有NO、NO2等,为消除它们对环境的破坏作用,工业上可采用氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
III.工业上也常用Na2CO3溶液吸收法处理氮氧化物(NOX)。
已知:①NO不能与Na2CO3溶液反应。
②
 ;
;
(5)①当NOx被Na2CO3溶液完全吸收时,x的值不可能是
A.1.3 B.1.6 C.1.8 D.2.0
②若用溶质质量分数为21.2%的Na2CO3溶液完全吸收1molNOx,则需要Na2CO3溶液至少
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液的质量就增加44g,则NOx中的x值为
(6)氨转化法和Na2CO3溶液吸收法处理NOx尾气共同的优点是
您最近半年使用:0次



