已知: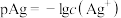 ,
,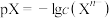 。
。 时,几种物质的
时,几种物质的 的值如下表:
的值如下表:
 、
、 、
、 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
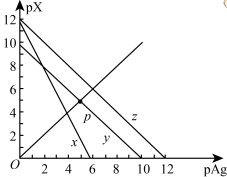
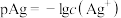 ,
,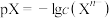 。
。 时,几种物质的
时,几种物质的 的值如下表:
的值如下表:| 化学式 |  |  |  |
| 颜色 | 白 | 浅黄 | 红 |
 |  |  |  |
 、
、 、
、 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
A.图中x代表 曲线,z代表 曲线,z代表 曲线 曲线 |
B.298K时,在 和 和 的物质的量浓度均为 的物质的量浓度均为 的溶液中,滴入少量 的溶液中,滴入少量 的 的 溶液,首先产生的是红色沉淀 溶液,首先产生的是红色沉淀 |
| C.298K时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 |
D.298K时, 的平衡常数 的平衡常数 |
19-20高三上·重庆沙坪坝·阶段练习 查看更多[20]
广西 南宁市第三中学2021-2022学年高二下学期期中考试化学试题吉林省通化市辉南县第六中学2022-2023学年高二上学期第一次月考化学试题陕西省西安中学2022届高三下学期五月全仿真模拟考试(一)理综化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期中考试化学试题(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)选择性必修1 专题3 第四单元综合训练福建省莆田二中2020-2021学年高三上学期期中检测化学试题陕西省汉中市部分高中2020-2021学年高二上学期12月月考化学试题(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节综合训练鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节综合训练陕西省西安中学2020届高三第六次模拟考试化学试题内蒙古赤峰市赤峰二中2019-2020学年高二下学期第一次月考化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】2020届高三《新题速递·化学》12月第01期(考点07-11)2019年秋高三化学复习强化练习—— 难溶电解质的沉淀溶解平衡黑龙江省哈尔滨市第六中学2020届高三上学期第三次调研考试化学试题贵州省铜仁市第一中学2020届高三上学期第三次月考化学试题重庆市第一中学2020届高三10月月考理综化学试题
更新时间:2020-09-13 21:48:14
|
相似题推荐
【推荐1】已知:AgA、Ag2B都是难溶盐。室温下,向体积均为10mL、浓度均为0.1mol·L-1的NaA溶液、Na2B溶液中分别滴加0.1mol·L-1的AgNO3溶液,溶液中pX与AgNO3溶液体积的关系如图所示[已知:pX=-lgc(A-)或一lgc(B2-)]。下列推断错误的是


| A.室温下,Ksp(Ag2B)=4×10-3a |
| B.对应溶液中c(Ag+):e>f |
| C.室温下,在等量的水中,AgA溶解的物质的量更多 |
| D.若c(AgNO3)变为0.05mol·L-1,则NaA溶液中的反应终点移至d点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】20℃时,将足量的BaSO4固体溶于50mL水中,充分搅拌,慢慢加入Na2CO3固体,搅拌,溶液中随c(CO32-)增大时c(Ba2+)变化曲线如下图。则下列说正确的是
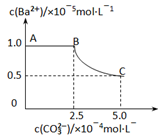

| A.20℃时Ksp(BaSO4)>Ksp(BaCO3) |
| B.加入Na2CO3固体立即有BaCO3固体生成 |
| C.BaCO3的Ksp=2.5×10-10 |
| D.曲线BC段内,c(CO32-):c(SO42-)=25 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:
则下列说法不正确的是
| CaSO4 | CaCO3 | MgCO3 | Mg(OH)2 | CuS | BaSO4 | H2S | H2CO3 | |
| Ksp或Ka | 9.1×10﹣6 | 2.8×10﹣9 | 6.8×10﹣6 | 1.8×10﹣11 | 6.3×10﹣36 | 1.1×10﹣10 | K1=1.3×10﹣7 K2=7.1×10﹣15 | K1=4.4×10﹣7 K2=4.7×10﹣11 |
| A.相同温度、相同浓度的钠盐溶液的pH:Na2S>Na2CO3>NaHS>NaCl>NaHSO4 |
| B.在NaHS溶液中滴加硫酸铜溶液,生成黑色沉淀:HS﹣+Cu2+=CuS↓+H+ |
| C.除去锅炉中水垢时,通常先加入足量硫酸钠溶液,将碳酸钙转化成硫酸钙,然后再用酸液处理 |
| D.在Mg(HCO3)2溶液中滴加足量澄清石灰水发生反应的离子方程式为:Mg2++2HCO3﹣+2Ca2++4OH﹣=Mg(OH)2↓+2CaCO3↓+2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】如图,M、N为常温下单一体系中 的溶解平衡曲线(M代表
的溶解平衡曲线(M代表 、N代表CO
、N代表CO ),P、Q为常温下单一体系中
),P、Q为常温下单一体系中 溶解平衡曲线(P代表
溶解平衡曲线(P代表 、Q代表
、Q代表 )。
)。
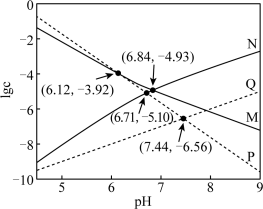
向含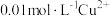 的碳酸—碳酸盐废水的混合体系中加入NaOH(s),调节pH使
的碳酸—碳酸盐废水的混合体系中加入NaOH(s),调节pH使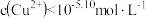 达排放标准。下列说法错误的是
达排放标准。下列说法错误的是
 的溶解平衡曲线(M代表
的溶解平衡曲线(M代表 、N代表CO
、N代表CO ),P、Q为常温下单一体系中
),P、Q为常温下单一体系中 溶解平衡曲线(P代表
溶解平衡曲线(P代表 、Q代表
、Q代表 )。
)。
向含
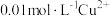 的碳酸—碳酸盐废水的混合体系中加入NaOH(s),调节pH使
的碳酸—碳酸盐废水的混合体系中加入NaOH(s),调节pH使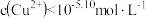 达排放标准。下列说法错误的是
达排放标准。下列说法错误的是A.pH=6.12时, 与 与 共沉淀 共沉淀 |
B.pH>6.71时,含 废水达排放标准 废水达排放标准 |
C.常温下 为 为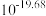 |
D.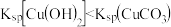 ,故 ,故 不能转化为 不能转化为 |
您最近一年使用:0次
【推荐3】25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是
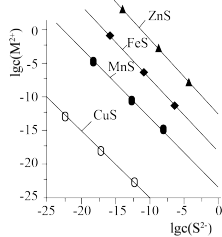

| A.25℃时Ksp(CuS)约为1×10-35 |
| B.向含有ZnS和Na2S的浊液中滴加CuSO4溶液,生成黑色沉淀,可证明:Ksp(CuS)<Ksp(ZnS) |
| C.向Cu2+浓度为10-5mol/L的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| D.向100mLZn2+、Cu2+浓度均为10-5mol•L-1的混合溶液中逐滴加入10-4mol•L-1的Na2S溶液,Cu2+先沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某废水中含有 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且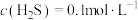 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是
 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且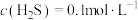 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是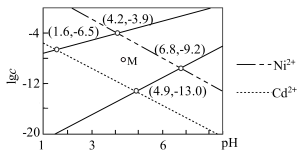
A. |
B.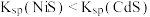 |
C.调节pH同时沉淀 和 和 时, 时,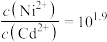 |
D.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】对某难溶电解质AnBm的饱和溶液中,下列说法正确的是
| A.加同温度的水,其溶度积减小、溶解度增大 |
| B.升高温度,它的溶解度和溶度积都增大 |
| C.饱和溶液中c(Am+)=c(Bn﹣) |
| D.加同温度的水,其溶度积、溶解度均不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下表是三种难溶金属硫化物的溶度积常数(25 ℃):下列有关说法中正确的是
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
| A.25 ℃时,将CuS固体用含Mn2+的饱和溶液浸泡可溶解CuS固体 |
| B.25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1 |
| C.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
| D.因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
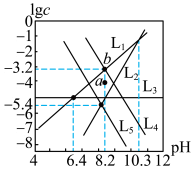
【推荐2】将CaCO3(s)或ZnCO3(s)悬浊液置于分压固定的CO2气相中,体系中pH与lgc关系如图所示,c为H2CO3、HCO 、CO
、CO 、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
 、CO
、CO 、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
| A.Kal(H2CO3)=10-6.4,Ksp(ZnCO3)=10-10.8 |
B.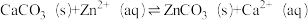 ,平衡常数: ,平衡常数: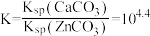 |
C.L1表示lgc(CO )-pH曲线 )-pH曲线 |
| D.向a点溶液中加入ZnCl2,可以达到b点溶液 |
您最近一年使用:0次

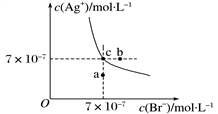
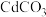 和
和 在25℃时的沉淀溶解平衡曲线,图2为向两份等体积等浓度的
在25℃时的沉淀溶解平衡曲线,图2为向两份等体积等浓度的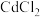 溶液中分别滴加等浓度的NaOH溶液和
溶液中分别滴加等浓度的NaOH溶液和 溶液滴定关系图(图1中横坐标为阴离子浓度的负对数,
溶液滴定关系图(图1中横坐标为阴离子浓度的负对数,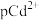 为
为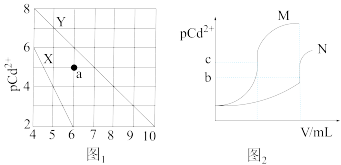
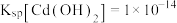
 ,
,
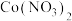 、
、 和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表
和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表 、
、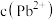 或
或 ,
, 。
。
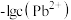 、
、 与 pH 的关系
与 pH 的关系
 和
和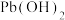 共存时:
共存时:


