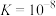20℃时,将足量的BaSO4固体溶于50mL水中,充分搅拌,慢慢加入Na2CO3固体,搅拌,溶液中随c(CO32-)增大时c(Ba2+)变化曲线如下图。则下列说正确的是

| A.20℃时Ksp(BaSO4)>Ksp(BaCO3) |
| B.加入Na2CO3固体立即有BaCO3固体生成 |
| C.BaCO3的Ksp=2.5×10-10 |
| D.曲线BC段内,c(CO32-):c(SO42-)=25 |
更新时间:2017-12-13 17:08:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
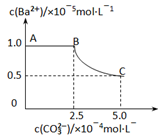
【推荐1】T℃时,CdCO3和Cd(OH)2的沉淀溶解平衡曲线如图所示,已知pCd2+为Cd2+浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是

A.X点:c(Cd2+)<c(OH-);Z点:c(CO )<c(Cd2+) )<c(Cd2+) |
| B.溶度积的负对数:pKsp(CdCO3)<pKsp[Cd(OH)2] |
| C.Y点对应的CdCO3溶液为不饱和溶液,可以继续溶解CdCO3 |
D.T℃时,Cd(OH)2(s)+ (aq)⇌CdCO3(s)+2OH-(aq)的平衡常数K为102 (aq)⇌CdCO3(s)+2OH-(aq)的平衡常数K为102 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
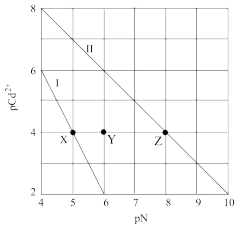
【推荐2】常温时,碳酸钙和硫酸钙的沉淀溶解平衡关系如图所示,已知 ,
, (酸根离子)
(酸根离子) (酸根离子)。下列说法
(酸根离子)。下列说法不正确 的是
 ,
, (酸根离子)
(酸根离子) (酸根离子)。下列说法
(酸根离子)。下列说法
A.曲线Ⅱ为 沉淀溶解曲线 沉淀溶解曲线 |
| B.加入适量的氯化钙固体,可使溶液由c点变到a点 |
| C.b点对应的硫酸钙溶液不饱和 |
D.向碳酸钙饱和溶液中通入 气体,溶液中 气体,溶液中 不变 不变 |
您最近一年使用:0次
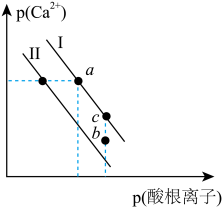
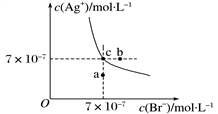
【推荐1】MB是一种难溶盐,H2B是一种二元弱酸(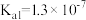 ,
, ),M2+不发生水解。室温下,将MB溶于一定浓度的一元强酸HA溶液中,直到不再溶解,所得溶液中
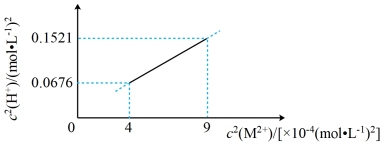
),M2+不发生水解。室温下,将MB溶于一定浓度的一元强酸HA溶液中,直到不再溶解,所得溶液中 有如图所示线性关系,下列说法错误的是(已知:
有如图所示线性关系,下列说法错误的是(已知: ,忽略溶液体积的变化)
,忽略溶液体积的变化)
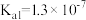 ,
, ),M2+不发生水解。室温下,将MB溶于一定浓度的一元强酸HA溶液中,直到不再溶解,所得溶液中
),M2+不发生水解。室温下,将MB溶于一定浓度的一元强酸HA溶液中,直到不再溶解,所得溶液中 有如图所示线性关系,下列说法错误的是(已知:
有如图所示线性关系,下列说法错误的是(已知: ,忽略溶液体积的变化)
,忽略溶液体积的变化)
A.在图示实线对应的pH范围内,溶液中 |
B.MB的溶度积 |
C.溶液中存在 |
D.将 溶于 溶于 溶液中,所需HA的最低浓度为 溶液中,所需HA的最低浓度为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度下,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),形成沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法不正确的是
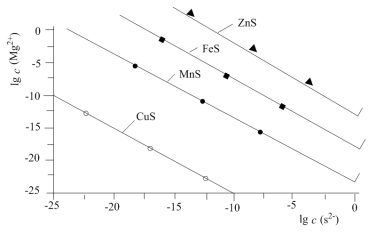

| A.若向沉淀剂Na2S溶液通入HCl气体至中性,存在关系: c(HS-)+2c(H2S)=c(Cl-) |
| B.该温度下,Ksp(MnS)大于1.0×10-35 |
| C.若将MnS、FeS的饱和溶液等体积混合,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS |
| D.向l00mL浓度均为10-5mol·L-1Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol·L-1Na2S溶液,ZnS先沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
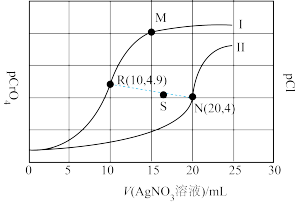
【推荐1】某温度下,分别向体积均为10 mL、浓度均为0.1 mol·L-1的KCl溶液和K2CrO4溶液中滴加0.1 mol·L-1的AgNO3溶液,滴加过程中pCl和pCrO4随加入AgNO3溶液的体积(V)的变化关系如图所示。已知:pCl=-lgc(Cl-),pCrO4=-lgc( )。下列说法不正确的是
)。下列说法不正确的是
 )。下列说法不正确的是
)。下列说法不正确的是
| A.曲线I表示pCl与V(AgNO3溶液)的变化关系 |
| B.若仅增大KCl的浓度,平衡点由R点沿虚线移向S点 |
C.M点溶液中:c( )>c(Ag+)>c(H+)>c(OH-) )>c(Ag+)>c(H+)>c(OH-) |
| D.该温度下,Ksp(Ag2CrO4)=4.0×10-12 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向20 mL 0.1 mol·L-1Na2CO3溶液中滴加0.1 mol·L-1 CaCl2溶液,碳酸根离子浓度与氯化钙溶液体积的关系如图所示。已知:pC=-lg c(CO ),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9.下列说法正确的是
),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9.下列说法正确的是

 ),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9.下列说法正确的是
),Ksp(CdCO3)=1.0×10-12,Ksp(CaCO3)=3.6×10-9.下列说法正确的是
| A.图象中V0=20,m=5 |
B.a点溶液:c(OH-)>2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
| C.若Na2CO3溶液的浓度变为0.05 mol·L-1,则n点向c点方向迁移 |
| D.若用CdCl2溶液替代CaCl2溶液,则n点向b点方向迁移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,CaCO3和CaF2的沉淀溶解平衡曲线如图[ pX=-lgc(Xn-)、pCa=-lgc( Ca2+)],已知Ksp( CaCO3)>Ksp( CaF2),下列说法正确的是
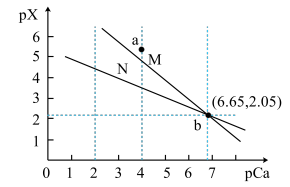

| A.曲线M为CaF2的沉淀溶解平衡曲线 |
B.常温下,CaCO3(s) +2F-(aq)  CaF2(s) + CaF2(s) +  (aq)的化学平衡常数K= 10-2.05 (aq)的化学平衡常数K= 10-2.05 |
C.在CaCl2溶液中加碳酸钠溶液,当溶液中c( )的浓度大于1. 0 ×10-3时,可以确定Ca2+沉淀完全 )的浓度大于1. 0 ×10-3时,可以确定Ca2+沉淀完全 |
| D.a点为悬浊液,过滤可得固体 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,向含少量盐酸的0.1mol/L的CrCl3溶液中逐滴滴加NaOH溶液,所加NaOH溶液的体积与溶液pH变化如图所示。

已知:Cr(OH)3为灰绿色的沉淀,当Cr3+浓度为10-5mol/L时,可认为沉淀完全,碱过量时生成[Cr(OH)4]-离子。下列说法正确的是

已知:Cr(OH)3为灰绿色的沉淀,当Cr3+浓度为10-5mol/L时,可认为沉淀完全,碱过量时生成[Cr(OH)4]-离子。下列说法正确的是
A.AB段发生反应的离子方程式为: |
| B.A到D过程中,溶液中水的电离程度先减小后增大 |
C.当溶液pH=5时,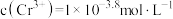 |
D.D点溶液中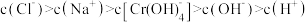 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】用0.1000mol/LNa2SO4标准溶液滴定20.00mLBaCl2溶液,测得溶液电导率σ及-lgc(Ba2+)随滴入Na2SO4标准溶液的体积V(Na2SO4)的变化关系如图所示。下列说法不正确的是
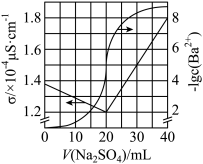
| A.BaCl2溶液的浓度为0.1000mol/L |
| B.Ksp(BaSO4)=10-10 |
| C.等浓度的Na+比Ba2+导电能力差 |
| D.若实验所用BaCl2溶液是用粗产品配制得来,则0.5000g粗产品中BaCl2•2H2O的质量分数为97.6% |
您最近一年使用:0次

 、
、 和
和 在水中达沉淀溶解平衡时的pM―pH关系。
在水中达沉淀溶解平衡时的pM―pH关系。
 的负对数,即
的负对数,即 ,
, 表示
表示 、
、 、
、 。
。 时,可认为金属离子沉淀全。
时,可认为金属离子沉淀全。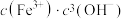 不相等
不相等 ,
, ,溶液中均无沉淀生成
,溶液中均无沉淀生成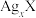 、
、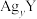 的饱和溶液中
的饱和溶液中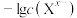 或
或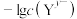 与
与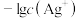 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
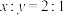
 ,
,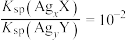
 平衡常数
平衡常数