例1 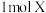 气体和
气体和 气体在一容积可变的密闭容器中发生反应
气体在一容积可变的密闭容器中发生反应 。反应达到平衡时,测得X的转化率为50%,且在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的
。反应达到平衡时,测得X的转化率为50%,且在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的 ,则a和b的数值可能是( )
,则a和b的数值可能是( )
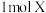 气体和
气体和 气体在一容积可变的密闭容器中发生反应
气体在一容积可变的密闭容器中发生反应 。反应达到平衡时,测得X的转化率为50%,且在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的
。反应达到平衡时,测得X的转化率为50%,且在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的 ,则a和b的数值可能是( )
,则a和b的数值可能是( )A. | B.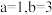 | C.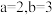 | D. |
更新时间:2020-09-16 21:12:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】顺—1,2—二甲基环丙烷和反—1,2—二甲基环丙烷可发生如图转化,该反应的速率方程可表示为v正=k正•c顺和v逆=k逆•c反,k正和k逆分别是正、逆反应速率常数,它们受温度的影响。下列有关说法正确的是


| A.该反应的平衡常数K可能为0 |
B.某温度时,该反应的平衡常数可表示为K= |
| C.正、逆反应速率常数改变,平衡常数也一定会随之改变 |
| D.温度降低,k正增大,k逆减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在体积均为2 L的恒温恒容密闭容器1、2中,同时充入1 mol Cl2(g)和1 mol PCl3(g),初始反应温度不同的条件下发生反应:PCl3(g)+Cl2(g)  PCl5(g)。下列叙述错误的是
PCl5(g)。下列叙述错误的是

 PCl5(g)。下列叙述错误的是
PCl5(g)。下列叙述错误的是
| A.平衡时压强:容器1>容器2 | B.初始反应温度:容器1>容器2 |
| C.容器1中0~3 min内v(PCl3)=0.2 mol·L-1·min-1 | D.容器2中达到平衡时PCl5产率为80% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】100℃时,把0.5molN2O4通入容积为5L的真空密闭容器中,发生N2O4(g)⇌2NO2(g),立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L−1,60s时,体系已达到平衡状态,此时容器内的压强为开始时的1.6倍。下列说法正确的是
| A.0~2s内用N2O4的浓度变化表示的反应速率为0.01mol·L−1·s−1 |
| B.在2s时容器内的压强为开始时的1.1倍 |
| C.平衡时,c(NO2)=0.6mol·L−1 |
| D.若压缩容器体积减小,达新平衡时的红棕色比原平衡时的浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向相同体积的甲、乙两容器中,甲容器中充入1molSO2和1 molO2,乙容器中充入2mol SO2和2 molO2且保持体积不变,在相同温度下,下列叙述中错误的是
| A.化学反应速率:乙>甲 | B.平衡时SO2的体积分数:乙>甲 |
| C.平衡时SO2的转化率:乙>甲 | D.平衡时O2的浓度:乙>甲 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g) +H2(g),反应过程中测定的部分数据见下表(表中t1>t2)
CO2(g) +H2(g),反应过程中测定的部分数据见下表(表中t1>t2)
下列说法正确的是
 CO2(g) +H2(g),反应过程中测定的部分数据见下表(表中t1>t2)
CO2(g) +H2(g),反应过程中测定的部分数据见下表(表中t1>t2)| 反应时间/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A.反应在t1min内的平均速率为v(H2)=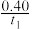 mol·L-1·min-1 mol·L-1·min-1 |
| B.保持其他条件不变,起始时向容器中充入0.60mol CO和1.20 mol H2O,到达平衡时,n(CO2)=0.40 mol |
| C.保持其他条件不变,向平衡体系中再通入0.20mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小 |
| D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
您最近一年使用:0次